СИНТЕЗ СУЛЬФАМИДОВ
Известно, что сульфаниламиды были первыми противомикробными препаратами, которые применялись системно. Его химическая структура представляет собой бензольное ядро с аминогруппами, которые придают ему активность. Аминогруппа ацетилируется в печени, инактивируя ее. В зависимости от заместителя в указанном секторе лекарство более активно.
Учитывая его сходство с парааминобензойной кислотой, он ведет себя как конкурентный ингибитор этого вещества, которое необходимо вместе с дигидроптеридином для синтеза дигидрофолиевой кислоты, промежуточного соединения в пути синтеза фолиевой кислоты.
В отличие от более продвинутых организмов, бактериям необходимо синтезировать собственные фолаты [они не приобретают их из окружающей среды], поэтому сульфаниламиды, угнетая этот процесс, угнетают процессы синтеза нуклеиновых кислот и являются БАКТЕРИОСТАТИЧЕСКИМИ.
ТРИМЕТРОПРИМ
Триметоприм является производным 2,4-диаминопиримидинов, таких как | Это соединение ИНГИБИРУЕТ фермент дигидрофолатредуктазу и препятствует образованию тетрагидрофолиевой кислоты, то есть действуют по тому же метаболическому пути, что и сульфаниламиды, но в последующей ферментативной реакции. Триметоприм никогда не используется сам по себе, но в сочетании с сульфаниламидами они потенцируются таким образом, что становятся БАКТЕРИЦИДНЫМИ, снижают возможность возникновения резистентности и увеличивают спектр антимикробного действия. Связь между сульфаметоксазолом и триметопримом зафиксирована: 1:5. Например, коммерческие препараты Котримоксазол [форте или нет] поставляются с этой целью. |
сульфаниламиды, обычно их классифицируют по продолжительности действия и способу применения препарата, а также по другим характеристикам. В зависимости от механизма действия сульфаниламиды бывают:
к)
Сульфаниламиды короткого или среднего действия.
к. Сульфонамиды общего назначения
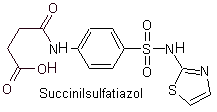
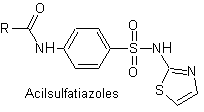
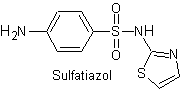
Эй. сульфатиазол
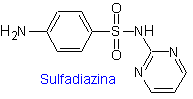
II. сульфадиазин
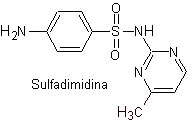
III. сульфадимидин
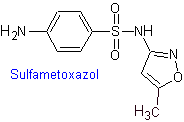
IV. Сульфаметоксазол (отдельно или в комбинации с триметопримом: котримоксазол)
б. Хорошо растворимые соединения первоначально применялись при лечении инфекций мочевыводящих путей.
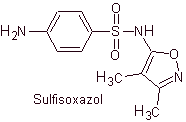
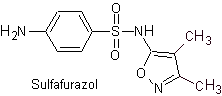
Эй. сульфизоксазол
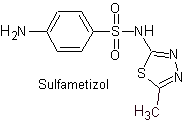
II. сульфаметизол
III. сульфазомидин
б)
Сульфаниламиды длительного действия.
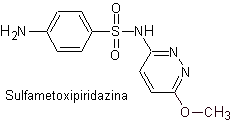
IV. сульфаметоксипиридазин
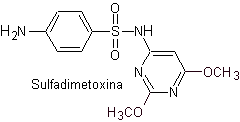
в. сульфадиметоксин
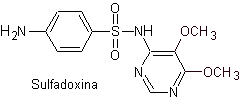
пила. сульфадоксин
в)
Сульфаниламиды ограничены желудочно-кишечным трактом
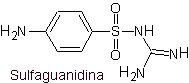
vii. сульфагуанидин
VIII. сульфаталидин
икс. сульфасуксидин
Икс. Сульфазолазин
г) Местные сульфаниламиды.
xi. мафенида ацетат
xii. сульфадиазин серебра
xiii. сульфацетамид натрия
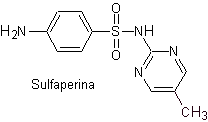
Основные сульфаты:
| ……… |
|
|
|
| …….. |
|
|
|
| …….. |
|
|
|
| …….. |
|
|
| |
|
|
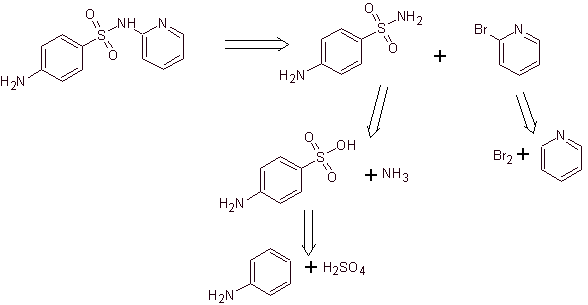
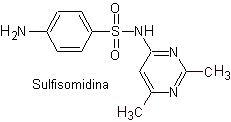
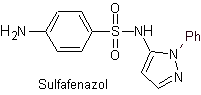
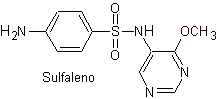
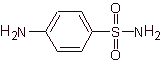
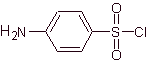
Структуры, которые представляют сульфаты, обычно состоят из двух частей, одна из которых соответствует 4-аминобензолсульфамид или 4-аминобензолсульфохлорид, в зависимости от реакции, используемой для образования сульфамида, а другая часть обычно представляет собой гетероцикл, который, конечно, варьируется в зависимости от конкретной рассматриваемой сульфамида.
4-аминобензолсульфамид | …. |
4-аминобензолсульфохлорид |
Синтез 4-аминобензолсульфамида и
4-аминобензолсульфохлорид :
Ретросинтетический анализ:
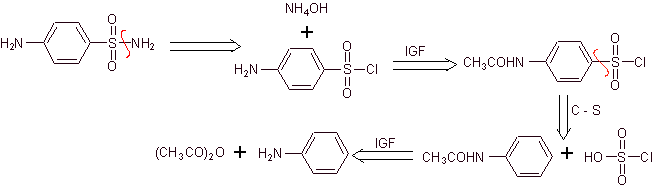
Синтез:
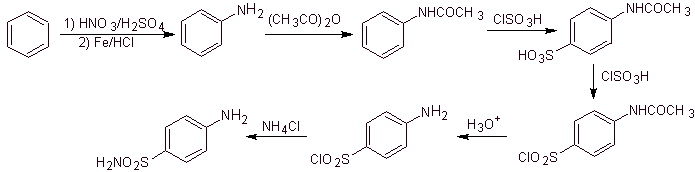
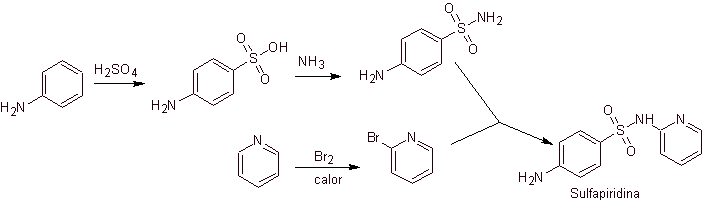
С другой стороны, также можно прибегнуть к любой из следующих реакций для образования субстратов (синтетических эквивалентов): которые необходимы для синтеза различных сульфаниламидов, в зависимости от обстоятельств:
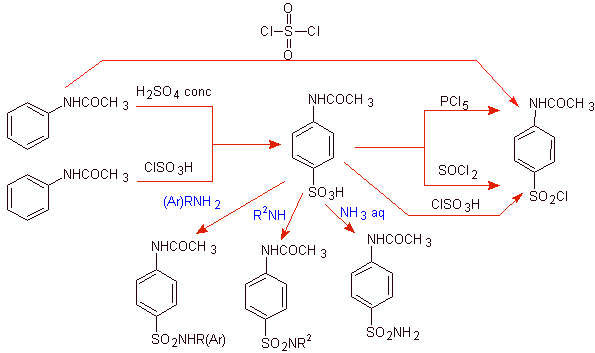
Периодически используемые аспекты стратегии связаны со следующими критериями:
![]() Аминогруппу анилина защищают ацилированием, чтобы избежать образования сульфоамида, с помощью реагентов, используемых для сульфирования бензола: H 2 SO 4 , ClSO 3 H или SO 2 Cl 2 и
Аминогруппу анилина защищают ацилированием, чтобы избежать образования сульфоамида, с помощью реагентов, используемых для сульфирования бензола: H 2 SO 4 , ClSO 3 H или SO 2 Cl 2 и
![]() Ацетамидогруппа (ацетанилида) может быть гидролизована перед реакцией с гетероциклом с образованием сульфаниламида. В качестве альтернативы можно перейти к стереоселективно контролируемому гидролизу в конце с разбавленной HCl, поскольку амидная группа ацетанилида гидролизуется первой.
Ацетамидогруппа (ацетанилида) может быть гидролизована перед реакцией с гетероциклом с образованием сульфаниламида. В качестве альтернативы можно перейти к стереоселективно контролируемому гидролизу в конце с разбавленной HCl, поскольку амидная группа ацетанилида гидролизуется первой.
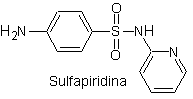
Пример. Синтезируйте сульфадиазин (MOb 10), сульфатиазол (MOb 11) и сульфизоксазол (MOb 12) из простых и доступных материалов.
MOb 10, Ретросинтетический анализ. Разъединение инициируется сульфонамидной связью, в результате чего образуются два простых синтетических эквивалента. Один из них — 4-аминобензолсульфохлорид, другой — 2-аминопиримидин, гетероцикл, синтез которого не представляет особых трудностей.
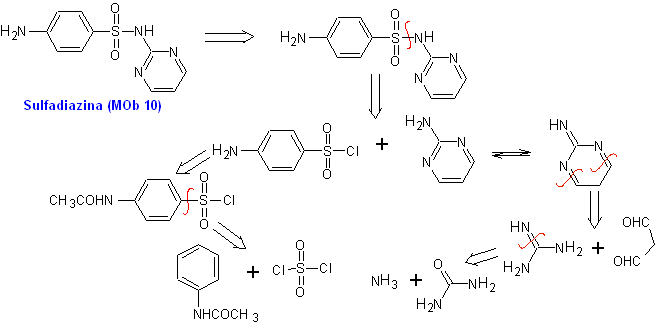
Синтез
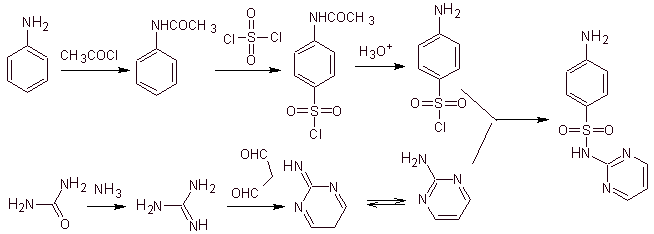
MOb 11. Ретросинтетический анализ: при разъединении образуется п-аминобензолсульфохлорид и 2-амино-1,3,тиазольный гетероцикл.
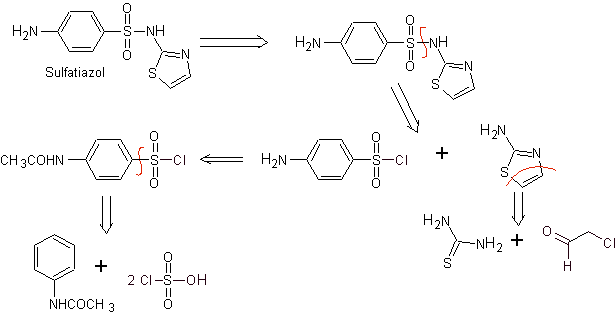
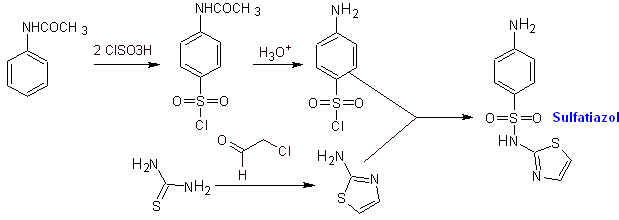
Синтез
MOb 12. Ретросинтетический анализ: отсоединение дает новый гетероцикл, 5-амино-3,4-диметил-1,2-оксазол.
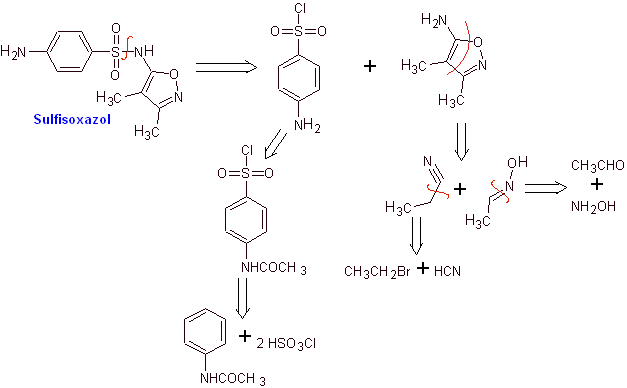
Синтез
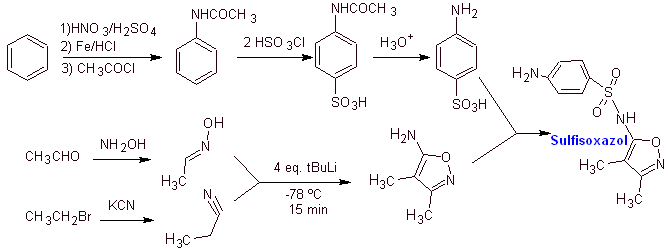
МОБ 13. Синтез
ретросинтетический анализ