Synthese von Heterocyclen mit mehreren Heteroatomen
Heterocyclische Verbindungen haben, wie bereits erwähnt, ein breites Anwendungsspektrum: Sie überwiegen unter den Verbindungen, die als Pharmazeutika, Agrochemikalien und für die Veterinärmedizin verwendet werden; sie werden als Polierzusätze, Antioxidantien, Korrosionsinhibitoren, als Farbstoffe und Pigmente verwendet; und in vielen weiteren Anwendungen.
Daher ist es vernünftig, dass sich derzeit ein Großteil der Forschung in der Chemie mit der Synthese und den Eigenschaften von heterocyclischen Verbindungen befasst. Daran orientiert sich dieser Artikel, der Chemiestudenten grundlegende Retrosynthese-Werkzeuge an die Hand geben soll.
Der Trennungsprozess für Moleküle mit mehreren Heteroatomen kann für jede Kohlenstoff-Heteroatom-Bindung gemäß den zuvor untersuchten Modellen oder gleichzeitig durchgeführt werden, wofür erschwingliche Polyheteroatom-Reagenzien verwendet werden.
1. Abstand Heteroatome (1, 2)
Die repräsentativsten und gebräuchlichsten Reagenzien sind Hydrazine und substituierte Hydrazine sowie Hydroxylamine.
Hydrazin |
Hydroxylamin |
Schlagen Sie ein Synthesedesign aus einfachen Materialien für die folgenden Moleküle vor:
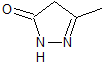
Mob 77
Pyrazole | MB 78
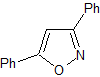
Isoxazole | MB 79
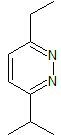
Pyridazine |
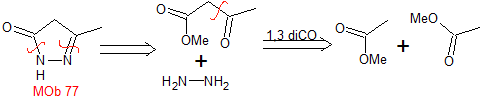
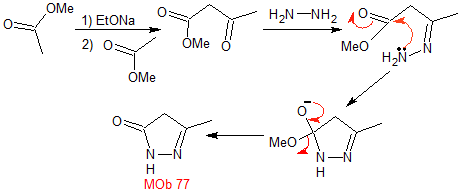
MOB 77 . Retrosynthetische Analyse. MOb ist ein Pyrazolderivat und wird direkt durch CN-Bindungen getrennt, um einfache Vorstufen wie Hydrazin und eine 1,3-diCO-Verbindung zu erzeugen.
|
Synthese . Methylacetat ist eine gute Vorstufe zur Bildung der Verbindung 1,3-diCO, die sich mit Hydrazin verbindet, um MOb 77 zu erzeugen. |
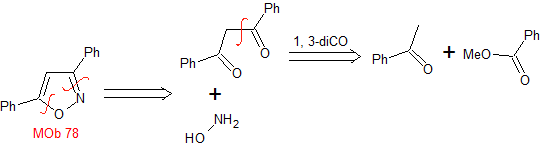
MOb 78 – Retrosynthetische Analyse .
|
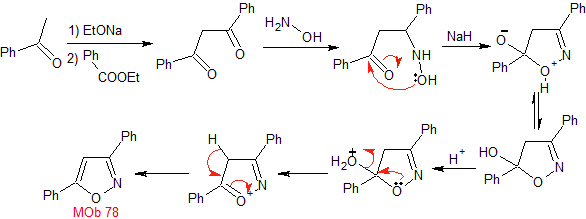
Synthese. Benzophenon und Ethylbenzoat ermöglichen es, das benötigte 1,3-diCO zu bilden, in leicht saurem Medium mit Hydroxylamin zu reagieren und nach Zugabe von NaH erfolgt eine Cyclisierung, die mehr Säure erfordert
dehydrieren und schließlich produzieren
|
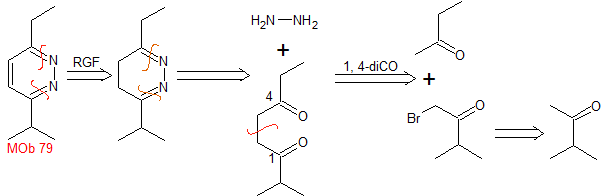
Mb 79 . Retrosynthetische Analyse. MOb ist ein Derivat von Diazin, das es durch gleichzeitige CN-Spaltung ermöglicht sicherzustellen, dass die Cycloaddition zwischen Hydrazin und einer 1,4-diCO-Verbindung stattgefunden hat.
|
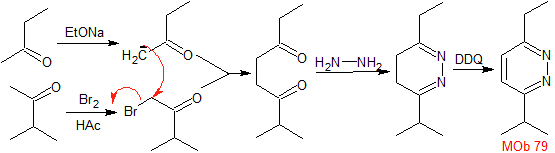
Synthese : Butanon ermöglicht die Bildung der 1,4-diCO-Verbindung, die dann mit Hydrazin kombiniert wird, um ein Hydrodiazin zu bilden, das, oxidiert mit DDQ, entsteht
|
1. Abstand Heteroatome (1,3)
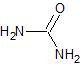
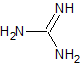
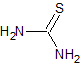
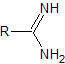
Die wichtigsten Reagenzien, die Heteroatome im Abstand von 1,3 enthalten oder zueinander interkaliert sind, sind: Harnstoff und seine Derivate, Guanidin und Derivate, Thioharnstoff und Derivate, Amidine und Derivate und schließlich Natriumcyanamid.
Harnstoff |
Guanidin |
Thioharnstoff |
Amidine |
Natriumcyanamid |
Schlagen Sie eine Synthese für die folgenden Moleküle vor:
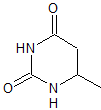
Mob 80
| MB: 81
| MB: 82
|
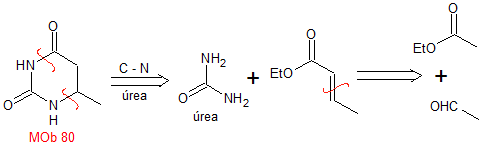
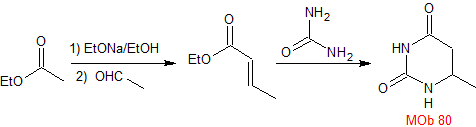
MB 80 . Retrosynthetische Analyse. Im MOb kann die Struktur von Harnstoff visualisiert werden, was uns einlädt, zwei simultane CN-Unterbrechungen vorzuschlagen.
|
Synthese. Es beginnt mit einer Claisen-Schmidt-Kondensation zwischen einem Ester und einem Aldehyd, um dann das Produkt mit Harnstoff durch die Michael-Reaktion zu kombinieren, um zu gelangen
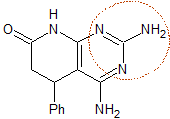
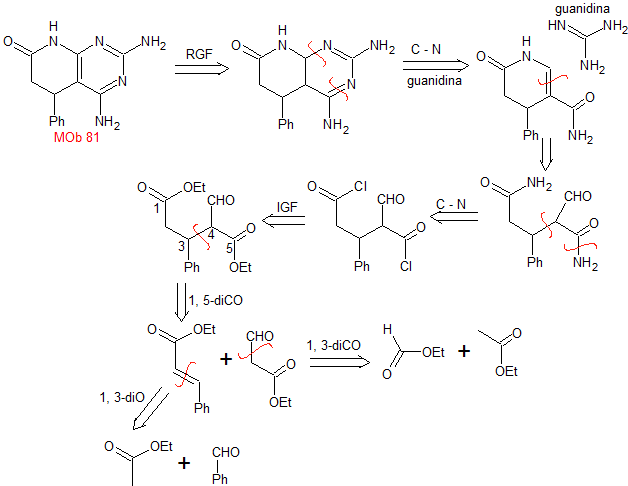
MB 81 . Retrosynthetische Analyse . Zunächst wird im MOb ein RGF durchgeführt, um einen die Guanidingruppe tragenden Precursor zu erzeugen, weshalb gleichzeitig eine CN-Spaltung durchgeführt wird, um die Spaltung durch das gebildete Enamin fortzusetzen. Das 1,5-diCO-Verhältnis ist das beste, um weiterhin Strukturen mit Disauerstoffverhältnissen von 1,3 zu trennen und herzustellen. Dies führt zu einfachen Molekülen als Ausgangsmaterialien.
|
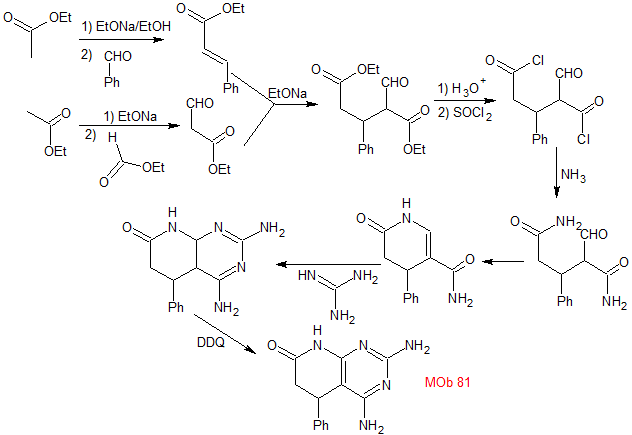
Synthese. Die Claisen- und Claisen-Schmidt-Kondensationen ermöglichen den Erhalt eines Schlüsselintermediats, das sich leicht in einen Diester umwandeln lässt, der sich nach der Hydrolyse mit SOCl2 verbindet, um ein dihalogeniertes Molekül zu bilden, das mit Ammoniak in ein Diamid umgewandelt wird.
Die intramolekulare Reaktion des vorherigen Produkts ergibt das geeignete Substrat, das mit Guanidin reagiert. Das so gebildete Produkt wird dann einem "Aromatisierungsprozess" mit DDQ unterzogen, um es zu bilden
|
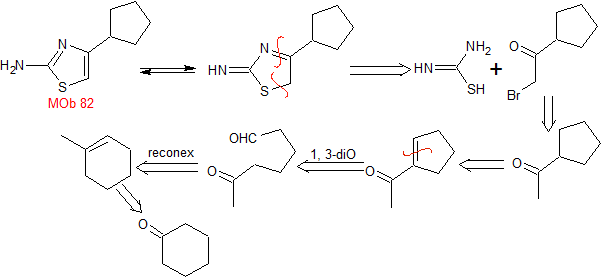
MOb 82. Retrosynthetische Analyse. Ein Tautomer von
|
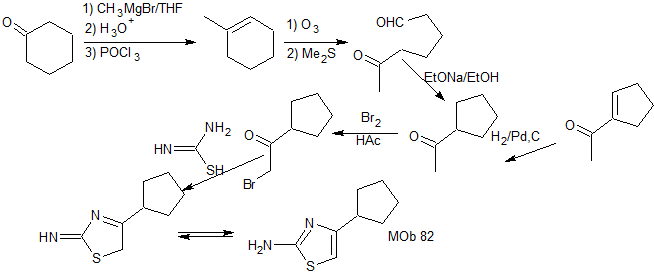
Synthese . Cyclohexanon ist das einfache Ausgangsmaterial, das nach mehreren Reaktionen durch Ozonolyse in einem Dimethylsulfid-Medium geöffnet wird, um eine 1,6-diCO-Verbindung herzustellen, die in einem basischen Medium kondensiert wird, um das angegebene Keton für seine Bromierung und anschließende zu ergeben Reaktion mit Thioharnstoff zu bilden
|
2. Abstand Heteroatome (1, 4)
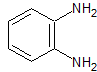
Ethylendiamin |
o- Phenylendiamin |
X = 0, S |
Schlagen Sie für Folgendes ein Synthesedesign vor Moleküle:
MB: 83
| MB: 84
| MB: 85
|
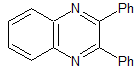
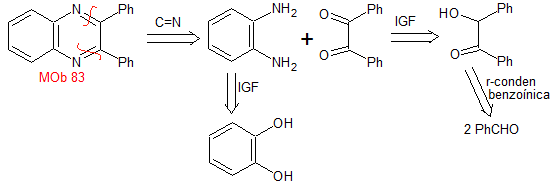
MB 83 . Retrosynthetische Analyse. Die Iminbindungen des MOb werden direkt getrennt, wodurch zwei Strukturen von Vorläufermolekülen entstehen, deren Synthese einfach ist.
|
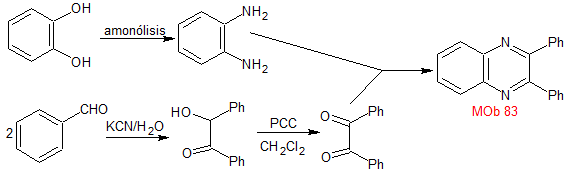
Synthese . Die benzoinische Kondensation von Benzaldehyd ermöglicht es, die notwendige Dicarbonylverbindung zu erreichen, die mit o-Phenylendiamin, hergestellt durch Ammonolyse von Brenzkatechin, zu verbinden ist
|
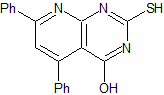
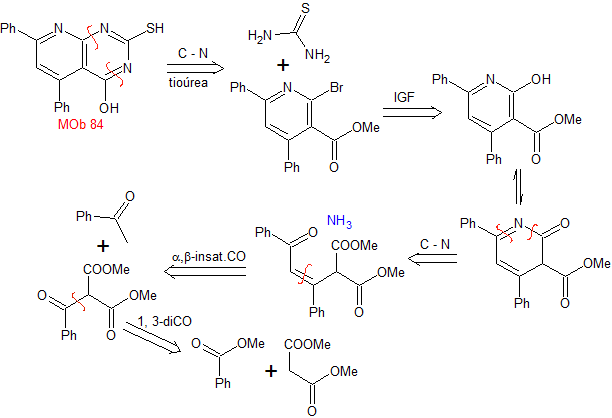
MOb 84 - Retrosynthetische Analyse. Auch im MOb ist die Struktur eines Thioharnstoffs zu erkennen, weshalb dieser durch die CN-Bindungen aufgetrennt ist. Die Funktionalisierung des bromierten synthetischen Äquivalents ermöglicht es uns, zu Strukturen mit dioxygenierten Verhältnissen zu gelangen, die in ihren Trennungen leicht zu handhaben sind.
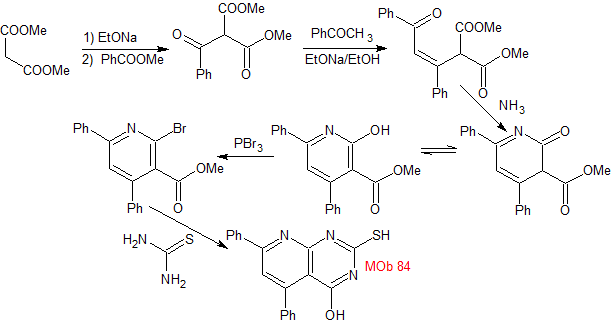
Synthese . Somit stellt sich Dimethylmalonat als einfaches Ausgangsmaterial für die Herstellung von MOb 84 heraus.
|
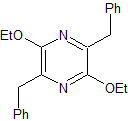
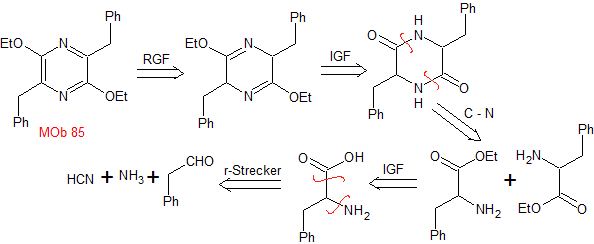
MB 85 . Retrosynthetische Analyse. Das MOb ist ein Pyrazinderivat, es wird funktionalisiert, um einen Vorläufer zu erreichen, der zwei Imingruppen enthält. Die Trennung des Moleküls durch diese Bindungen ermöglicht die Erzeugung eines anderen Vorläufers, der ein Alpha-Aminoester ist, das Molekül, das sich selbst kondensiert.
|
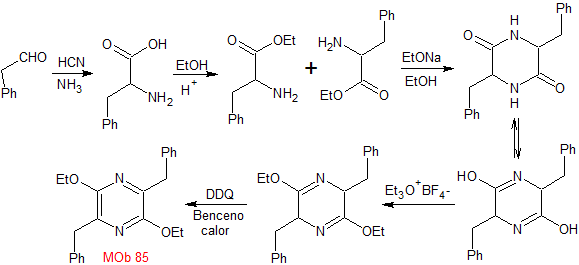
Synthese . Die Strecker-Synthese wird verwendet, um den erforderlichen Aminoester zu bilden, der in einem basischen Medium selbst kondensiert. Das Et 3 ONF 4 ermöglicht das Erreichen der Diiminverbindung, die dann durch das DDQ oxidiert oder aromatisiert wird, um MOb 85 zu bilden.
|