Die organische Synthese, das Herzstück der organischen Chemie , ist im Wesentlichen eine heuristische Aktivität, das heißt, ein Prozess, bei dem die hochvoraussagenden kreativen Aktivitäten des logischen Denkens und der empirischen Verfahren, reich an künstlerischer Ausarbeitung, verschmelzen und den organischen Chemiker zu einem echten Innovator machen.
Wie jede Methode hat auch die „ Disconnection- oder Synthon-Methode “ ihre eigene Struktur, Symbologie und Sprache, die von denjenigen, die bereit sind, dieses synthetische Werkzeug zu verwenden, zunächst assimiliert und verstanden werden müssen.
Das Syntheseverfahren der Unterbrechungen oder Synthons umfasst Zwei Phasen;
![]() Phase der retrosynthetischen Analyse . Es zeigt alle Transformationen, die bei der Vereinfachung der Struktur von durchgeführt werden
Phase der retrosynthetischen Analyse . Es zeigt alle Transformationen, die bei der Vereinfachung der Struktur von durchgeführt werden
![]() Synthesephase . Wo das "Gedachte", basierend auf Kriterien der mechanistischen Rationalität und Reaktivität organischer Verbindungen, in einem Syntheseweg materialisiert, der geschrieben wird, wie er im chemischen Labor erwartet wird. Hier entsteht Erfahrung und manifestiert die „ Kunst des Tuns oder erfinden “ des Chemikers, d.h.
Synthesephase . Wo das "Gedachte", basierend auf Kriterien der mechanistischen Rationalität und Reaktivität organischer Verbindungen, in einem Syntheseweg materialisiert, der geschrieben wird, wie er im chemischen Labor erwartet wird. Hier entsteht Erfahrung und manifestiert die „ Kunst des Tuns oder erfinden “ des Chemikers, d.h.
Der Begriffe, Definitionen oder Syntheseoperationen, die in diesem Verfahren immer wieder verwendet werden, sind die folgenden:
Zielmolekül (MOb) .
Dies ist der Name für jedes Molekül, das aus einfachen und erschwinglichen Materialien synthetisiert oder hergestellt werden soll, das in einem Problem zuvor definiert oder an die Optionen angepasst werden kann, die der Chemiker in seinem Syntheseplan oder Design generiert.
Verwandlung . ( ![]() ).
).
Der spezielle unidirektionale Retrosynthesepfeil ist als symbolische Darstellung des Ausdrucks „ wird hergestellt aus “ zu verstehen und repräsentiert auch eine Art Transformation in der Struktur von
Die genannten Transformationstypen sind eigentlich retrosynthetische Operationen wie: Trennungen, Wiederverbindungen, Umlagerungen, Umwandlung funktioneller Gruppen (IGF), Addition funktioneller Gruppen (AGF), Deletion funktioneller Gruppen (SGF) usw.
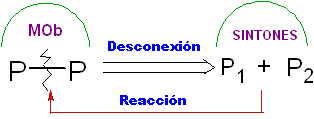
Trennung.
Es handelt sich um eine retrosynthetische Operation, die das imaginäre Aufbrechen der chemischen Bindungen darstellt, die im Zielmolekül, von den Synthonen oder genauer gesagt von ihren synthetischen Äquivalenten (Vorläufermolekülen), gebildet worden wären, postuliert.
Es kann als Umkehrung einer chemischen Reaktion verstanden werden, es wird durch einen Pfeil (sehr verschieden von dem einer chemischen Reaktion oder Gleichgewichtsbedingungen) und eine gekreuzte Wellenlinie über der Bindung dargestellt, die "getrennt" wird.
Es ist sogar möglich, die vorgeschlagene Trennung auf dem Pfeil zu platzieren: CC, CS. CX, CO, CN. usw.. Ausdrücke, die uns mit der Art der Reaktion verbinden, die verwendet wird, bei der Bildung von
In anderen Fällen kann das verwendete Trennungsmodell geschrieben werden, zum Beispiel ist es üblich zu finden: 1, 3-diO, 1,4 –diCO, 1,5-diCO oder α, β -insatCO . Usw.
Daher können in einem dioxygenierten Molekül die folgenden Trennungen erwartet werden:
![]() heterolytische Trennungen,
heterolytische Trennungen,
![]() Homolytische oder radikale Trennungen
Homolytische oder radikale Trennungen
![]() Elektrozyklische Unterbrechungen
Elektrozyklische Unterbrechungen
![]() Verbindungsabbrüche neu ordnen
Verbindungsabbrüche neu ordnen
Es ist die synthetische Operation der Wiederverbindung zweier Punkte
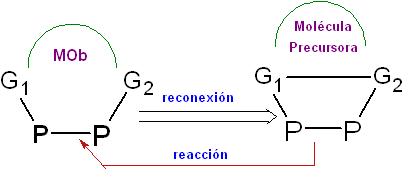
Ein typisches Beispiel für die Wiederverbindung sind die Moleküle, die durch die Öffnung einer chemischen Bindung erhalten wurden, wie es beispielsweise bei der Ozonolyse von Alkenen der Fall ist, die Produkte liefern, die für ihre Synthese mit dem Wiederverbindungsvorgang beginnen müssen.
Neuordnung . Die Transformationsoperation, mit der Sie eine Unterstruktur von verschieben können
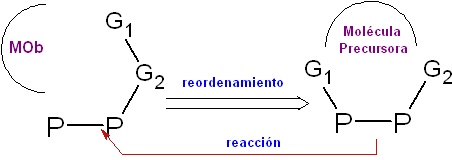
Die Pinakolin-Umlagerung, die Fries-Umlagerung, die Beckmann-Umlagerung, die Curtius-Umlagerung und die Claisen-Umlagerung.
Dies sind einige typische Beispiele für eine Transposition, deren Produkte eine Umordnung ihrer strukturellen Komponenten in der Transformationsoperation erfordern, um ihr Vorläufermolekül zu erreichen.
Retroelektrozyklisch .
Es ist möglich, eine gleichzeitige Trennung durch zwei Verbindungen zu postulieren, von denen angenommen wird, dass sie von a gebildet wurden
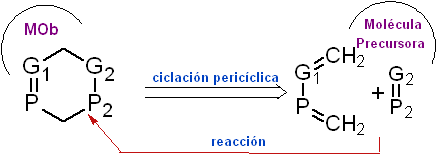
konzertierte pericyclische Reaktion, dies ist sehr häufig, wenn in
Umwandlung funktioneller Gruppen (IGF).
Es ist der Prozess, durch den die Gruppe(n) funktionelle Gruppe(n) des Moleküls, die einer retrosynthetischen Analyse unterzogen werden, in eine andere funktionelle Gruppe umgewandelt werden, die sich in der Struktur des Synthons oder synthetischen Äquivalents (Vorläufermolekül) befindet, die durch eine normale Reaktion von Substitution, Eliminierung, Addition, Umlagerung, Oxidation umgewandelt wird oder Reduktion, wird es in die funktionelle Gruppe des Moleküls umgewandelt, das erhalten werden soll.
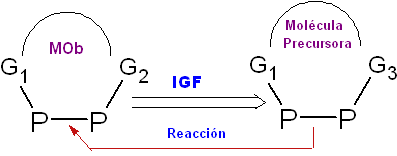
Die Umkehrung eines IGF ist die chemische Reaktion. Es wird durch den Pfeil dargestellt: ![]() mit den Initialen IGF oder anderen, die Retrosyntheseoperationen darstellen, darauf
mit den Initialen IGF oder anderen, die Retrosyntheseoperationen darstellen, darauf
Hinzufügen einer funktionellen Gruppe (AGF ).
Es ist die Hinzufügung einer neuen funktionellen Gruppe in der Struktur des Vorläufermoleküls (synthetisches Äquivalent), die wird
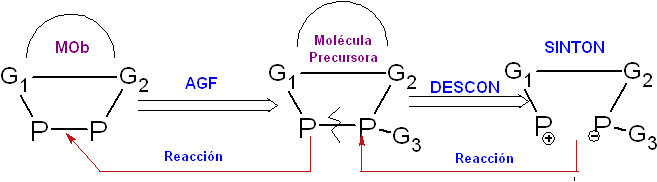
Der Zweck der Einführung dieser neuen funktionellen Gruppe besteht normalerweise darin, den Aufbau des Vorläufermoleküls (Synthon, intermediäres Molekül, synthetisches Äquivalent) leichter durchführbar zu machen Synthesevorgang, der zum Beispiel sein könnte: Eine einfache Trennung, da die hinzugefügte funktionelle Gruppe die aus der Trennung resultierende Synthonstruktur stabilisieren könnte, das Molekül für eine andere chemische Reaktion davon aktivieren oder deaktivieren könnte.
Entzug der funktionellen Gruppe (RGF) oder Unterdrückung der funktionellen Gruppe (SGF)
Diese retrosynthetische Transformationsoperation ermöglicht das Vorläufermolekül, aus dem es hergestellt wird
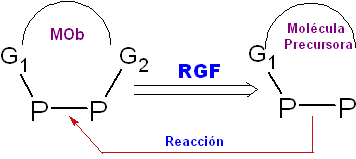
in der Struktur von
Synthon.
Im Allgemeinen ist dies der Name, der der chemischen Spezies gegeben wird, die fast immer aus einer Trennung einer Bindung von resultiert
Synthetisches Äquivalent (Stammmolekül ).
In jedem Fall ist ein Synthon eine chemische Spezies, die nicht direkt in einer chemischen Reaktion verwendet werden kann, manchmal aufgrund ihrer Instabilität und manchmal, weil es sich um eine Spezies handelt, die nicht existiert.Dazu muss zuvor eine durchgeführt werden Abstraktionsprozess über die Struktur Synthon, um seine Existenz durch ein anderes Molekül namens synthetisches Äquivalent zu rechtfertigen. Das letztere, das synthetische Äquivalent oder Vorläufermolekül, ist also ein echtes Molekül, das wie die Synthone wirkt, die durch die bewirkte Trennung erzeugt werden
Tautomerisierung.
Es erlaubt, die Gültigkeit eines Tautomers zu erklären, das im Gleichgewicht mit einem Vorläufermolekül steht und dessen Struktur es erlaubt, einen späteren Synthesevorgang im Synthesedesign zu erklären und zu verstehen.







