 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp. .
Más información en www.foroquimico.com
Si prefieres un curso de química orgánica tanto básica como avanzada te invito a acceder al canal: https://www.youtube.com/channel/UC_RiUaA2326jO9XozAA4q2g , en el que encontrarás más de 750 vídeos de teoría y ejercicios.
TEORÍA DE ALQUENOS
- Detalles
- Germán Fernández
- TEORÍA DE ALQUENOS
- Visto: 88961
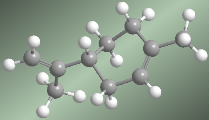 Los alquenos son hidrocarburos que contienen enlaces dobles carbono-carbono. Se emplea frecuentemente la palabra olefina como sinónimo.
Los alquenos son hidrocarburos que contienen enlaces dobles carbono-carbono. Se emplea frecuentemente la palabra olefina como sinónimo.
Los alquenos abundan en la naturaleza. El eteno, es un compuesto que controla el crecimiento de las plantas, la germinación de las semillas y la maduración de los frutos.
- Detalles
- Germán Fernández
- TEORÍA DE ALQUENOS
- Visto: 384753
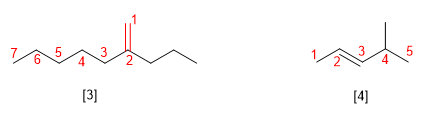
Los alquenos se nombran reemplazando la terminación -ano del correspondiente alcano, por -eno. Los alquenos más simples son el eteno y el propeno, también llamados etileno y propileno a nivel industrial.

- Detalles
- Germán Fernández
- TEORÍA DE ALQUENOS
- Visto: 160791
 Cada anillo o ciclo de una molécula implica la pérdida de dos hidrógenos respecto a un alcano de fórmula CnH2n+2. Se denomina grado de insaturación al número de ciclos y dobles enlaces presentes en una molécula..
Cada anillo o ciclo de una molécula implica la pérdida de dos hidrógenos respecto a un alcano de fórmula CnH2n+2. Se denomina grado de insaturación al número de ciclos y dobles enlaces presentes en una molécula..
- Detalles
- Germán Fernández
- TEORÍA DE ALQUENOS
- Visto: 102133
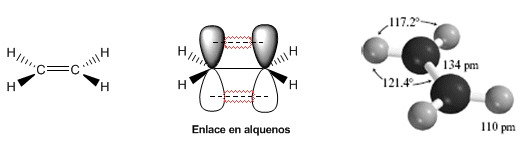
Los siguientes modelos muestran la estructura, distancias y ángulos de enlace del eteno. Cada uno de los carbonos de la molécula tiene hibridación $sp^2$. Su geometría es plana, con ángulos de enlace próximos a los 120º.
- Detalles
- Germán Fernández
- TEORÍA DE ALQUENOS
- Visto: 153074
Los alquenos presentan puntos de fusión y ebullición próximos a los alcanos correspondientes.
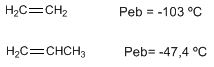
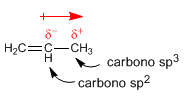
Momento dipolar en alquenos. El carbono $sp^2$ los electrones en el orbital s están más próximos al núcleo y son atraídos fuertemente por éste, de modo que un carbono $sp^2$ tiene tendencia a atraer hacia si electrones, lo que genera momentos dipolares.
- Detalles
- Germán Fernández
- TEORÍA DE ALQUENOS
- Visto: 93432
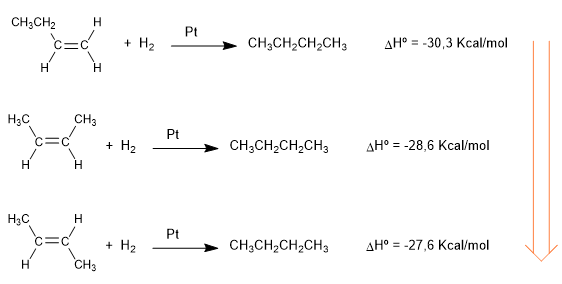
Los calores desprendidos en las siguientes reacciones de hidrogenación, nos dan una idea sobre la diferente estabilidad de los alquenos.
- Detalles
- Germán Fernández
- TEORÍA DE ALQUENOS
- Visto: 84620
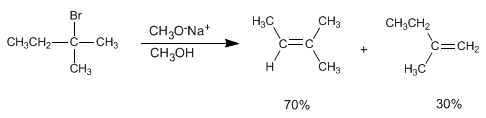
Los alquenos pueden prepararse a partir de haloalcanos y sulfonatos de alquilo mediante eliminación bimolecular (E2). En el siguiente ejemplo el 2-bromo-2-metilbutano reacciona con metóxido de sodio para formar una mezcla de 2-metil-2-buteno y 2-metil-1-buteno.
- Detalles
- Germán Fernández
- TEORÍA DE ALQUENOS
- Visto: 164208
El tratamiento de alcoholes con ácidos minerales a elevadas temperaturas provoca la pérdida e agua, que transcurre a través de mecanismos E1 o E2.
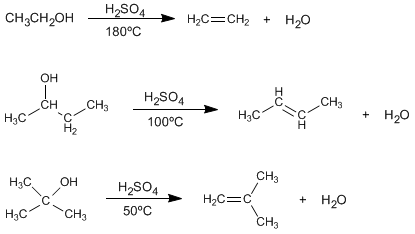
Leer más: Síntesis de Alquenos por Deshidratación de Alcoholes