 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp. .
Más información en www.foroquimico.com
Si prefieres un curso de química orgánica tanto básica como avanzada te invito a acceder al canal: https://www.youtube.com/channel/UC_RiUaA2326jO9XozAA4q2g , en el que encontrarás más de 750 vídeos de teoría y ejercicios.
-
Detalles
-
Germán Fernández
-
TEORÍA DE ESTEREOQUÍMICA
-
Visto: 16201
Vamos a ver como las reacciones químicas pueden introducir quiralidad en las moléculas, obteniéndose productos en forma de mezclas racémicas o bien mezclas de diastereoisómeros.
El butano se halogena en presencia de bromo y luz, en el carbono 2, para formar una mezcla de enantiómeros. El radical formado presenta caras enantiotópicas, que son halogenadas con igual probabilidad, dando lugar a una mezcla racémica (enantiómeros en igual proporción).
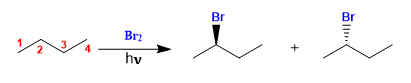
El mecanismo de esta reacción consta de tres etapas: iniciación, propagación y terminación. La propagación es la etapa que determina la estereoquímica del producto final
Halogenación del butano
Etapa 1. Iniciación
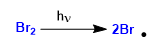
Etapa 2. Propagación
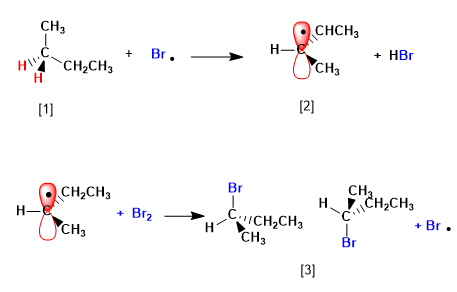
[1 ] H (Hidrógenos enantiotópicos)
[2 ] Radical con caras enantiotópicas
[3 ] Pareja de enantiómeros
El producto se obtiene como mezcla racémica, debido a la formación de un radical plano que es halogenado por las dos caras. Los hidrógenos enantiotópicos son químicamente equivalentes y el bromo los sustrae con la misma velocidad.
El radical generado es plano y los lóbulos son atacados con igual probabilidad por el bromo molecular, lo que produce 2-bromobutano racémico.
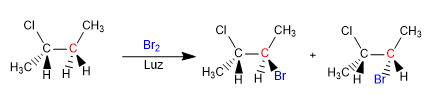
Halogenación del (S)-2-Clorobutano en C3
La reacción de halogenación con bromo del(S)-2-Clorobutano sobre el carbono C3 tiene el siguiente forma:
Las etapas de propagación que determinan la estereoquímica del producto formado son:
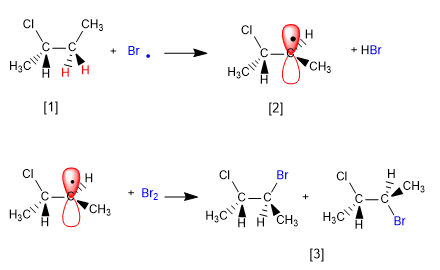
[1 ] H (hidrógenos diastereotópicos)
[2 ] Radical con caras diastereotópicas
[3 ] Mezcla de diastereoisómeros
La halogenación de la posición C3 conduce a diastereoisómeros. Las caras del radical formado no son equivalentes y son atacadas a distinta velocidad por la molécula de bromo. Se denominan caras diastereotópicas y los hidrógenos que sustrae el bromo: hidrógenos diastereotópicos.



 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?