ESPECTROSCOPÍA DE INFRARROJO
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 58176
Los fotones de radiación infrarroja son absorbidos por los enlaces de una molécula pasando a niveles vibracionales superiores.
Cada tipo de enlace absorbe radiación infrarroja a una frecuencia distinta, lo que permite determinar que tipo de grupos funcionales posee la molécula en estudio. Los espectrofotómetros de infrarrojo trabajan en el infrarrojo medio y hacen un barrido desde los 4000 $cm^{-1}$ hasta los 400 $cm^{-1}$
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 41314
Para que una molécula absorba radiación infrarroja deben cumplirse dos condiciones:
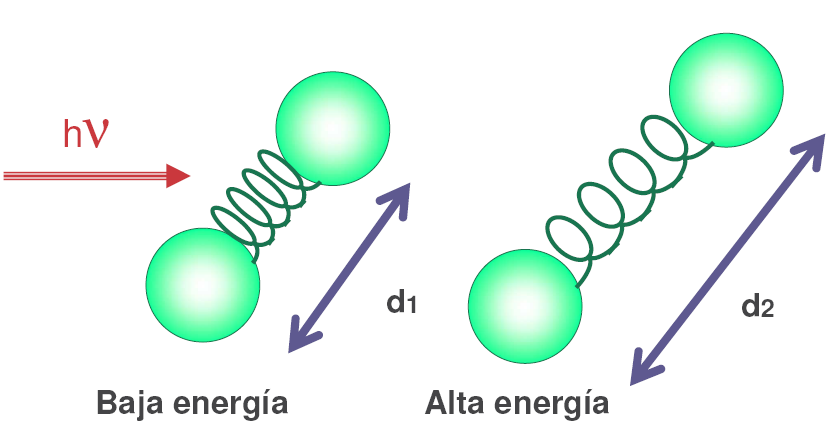
- La frecuencia de la radiación (fotón) debe ser la adecuada para permitir la transición entre estados vibracionales. Dicho de otro modo, la frecuencia de la radiación debe coincidir con la frecuencia natural del movimiento vibracional.
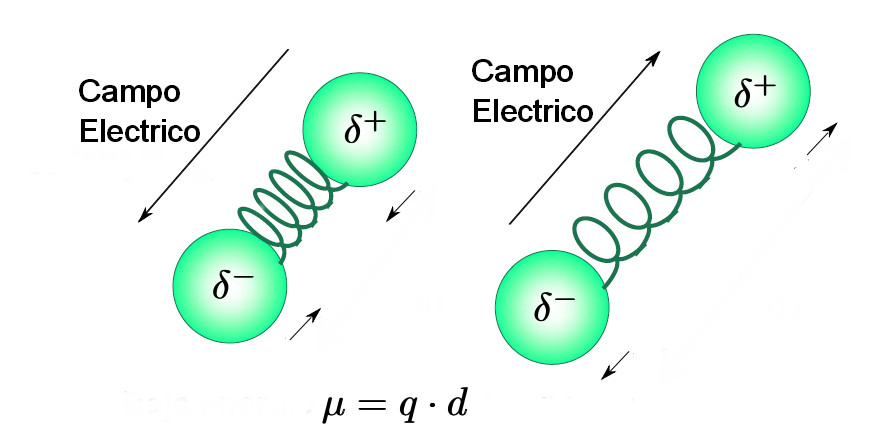
- Una molécula sólo absorbe radiación infrarroja cuando su momento dipolar interacciona con el campo electrico de la onda, variando en fase con este. Como es lógico este acoplamiento sólo es posible si las frecuencias de la radiación y la vibración del enlace coinciden. Por ello, moléculas apolares no absorben en el infrarrojo y moléculas poco polares dan lugar a absorciones muy débiles.
- Regla de selección de la espectroscopía infrarroja: "sólamente aquellos enlaces cuya vibración provoque un cambio en el momento dipolar de la molécula absorben en el infrarrojo".
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 55417
Vibración de tensión (stretching). Los átomos unidos por enlaces simples, dobles o triples se acercan y alejan siguiendo la dirección del enlace, igual que oscilan dos masas unidas por un muelle.
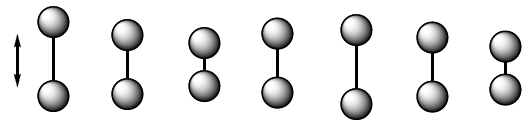 Vibración de Tensión
Vibración de Tensión
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 25173
Las vibraciones moleculares pueden estudiarse con el modelo del oscilador armónico cuántico. La energía viene dada por:
\begin{equation}\label{energia-oscilador} E_v=\left(v+\frac{1}{2}\right)h\nu \end{equation}
Los distintos niveles de energía vienen dados por el número cuántico v, que toma valores 0.1.2.3.4.....
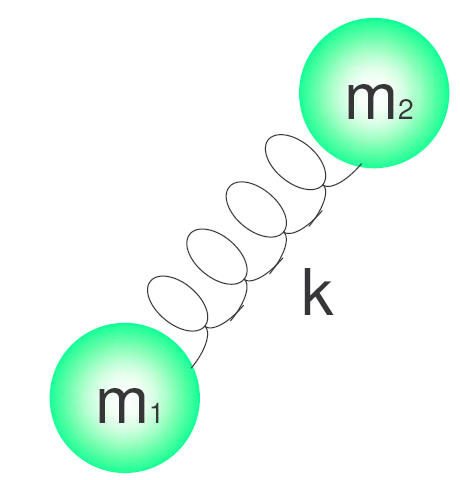
h es la constante de Planck y $\nu$ la frecuencia del oscilador que viene dada por la expresión:\begin{equation} \nu=\frac{1}{2\pi}\sqrt{\frac{k}{\mu}} \end{equation} Donde k es la constante de fuerza del muelle y $\mu$ la masa reducida del sistema. $\mu=\frac{m_1m_2}{m_1+m_2}$.
Dividiendo la frecuencia entre la velocidad de la luz se obtiene número de ondas $\bar{\nu}$ \begin{equation}\label{numero-ondas} \bar{\nu}=\frac{1}{2\pi c}\sqrt{\frac{k}{\mu}} \end{equation} El estudio de la ecuación (\ref{numero-ondas}) nos permitirá predicir a qué número de ondas absorben radiación infrarroja los enlaces de una molécula. Esta ecuación sólo es aplicable a las vibraciones de tensión.
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 21163
- Absorciones fundamentales, son transiciones vibracionales desde el estado fundamental al primer estado excitado. Dan lugar a las bandas de mayor intensidad.
- Sobretonos, son transiciones vibracionales desde el estado fundamental a estados excitados superiores. Las frecuencias de absorción son $2/nu,3\nu...$ siendo $\nu$ la frecuencia de la absorción fundamental.
- Bandas de combinación, resultan del acoplamiento de 2 bandas $\nu_1$ y $\nu_2$ para dar lugar a una nueva banda de frecuencia $\nu_{comb}=\nu_1 + \nu_2$
- Bandas de diferencia, , resultan del acoplamiento de 2 bandas $\nu_1$ y $\nu_2$ para dar lugar a una nueva banda de frecuencia $\nu_{comb}=\nu_1 - \nu_2$
- Resonancia de Fermi, resultan del acoplamiento de una banda de absorción fundamental con un sobretono o una banda de combinación.
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 23194
Como comentamos en el punto anterior la frecuencia de absorción depende de la constante de fuerza y de la masa de los átomos que vibran.
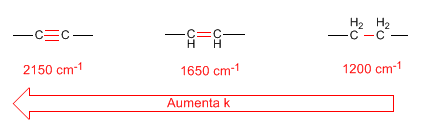
- Constante de fuerza. Los enlaces triples son más fuertes que los dobles y éstos más fuertes que los simples. Por ello, la constante de fuerza de los enlaces triples es mayor que la de los dobles, siendo la constante de fuerza de los enlaces simples la menor.
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 41883
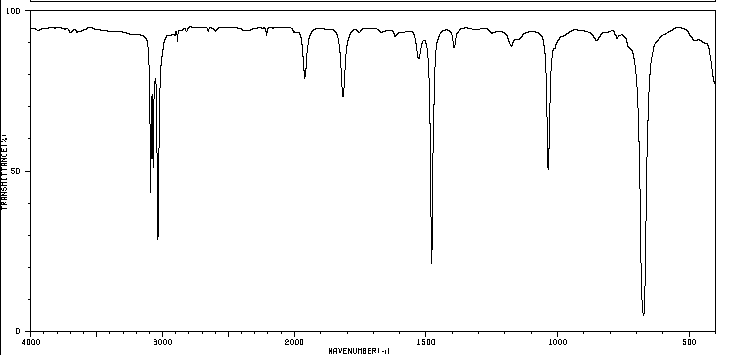
En un espectro de infrarrojos se representa la frecuencia (en número de onda) frente al porcentaje de luz transmitida (transmitancia). El porcentaje de transmitancia se define como el cociente entre la intensidad de la luz transmitida a través de la muestra, $I_M$, y la intensidad de la luz del haz de referencia $I_R$ multiplicado por 100. \begin{equation} \%Transmitancia=\frac{I_M}{I_R}\times 100 \end{equation} El barrido de frecuencia oscila entre 400 y 4000 $cm^{-1}$
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 67837
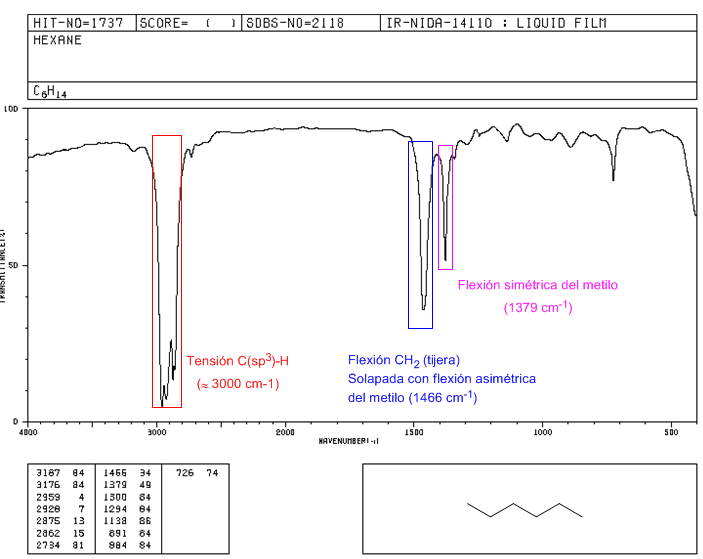
• Tensión C-H: los alcanos presentan vibraciones de tensión C-H ligeramente por debajo de 3000 $cm^{-1}$
• Flexión C-H: los $CH_2$ de la cadena presentan vibraciones de flexión (tijera) a 1465 $cm^{-1}$, mientras que los metilos producen una banda a 1375 $cm^{-1}$ debida a la vibración de flexión simétrica y otra a 1450 $cm^{-1}$ debida a la vibración de flexión asimétrica. Todas las bandas de flexión son de intensidad media.
Obsérvese que la banda de flexión asimétrica del metilo solapa con la de flexión en tijera del $CH_2$.
Espectro IR del Hexano
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 7517
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 49162
Los cicloalcanos tienen un espectro de IR muy similar a los alcanos con banda de tensión C-H ligeramente por debajo de 3000 $cm^{-1}$ y banda de flexión C-H en tijera para los CH2 a 1465 $cm^{-1}$. La principal diferencia con los alcanos es la ausencia de la banda de tensión simétrica del metilo.
Espectro IR del ciclohexano
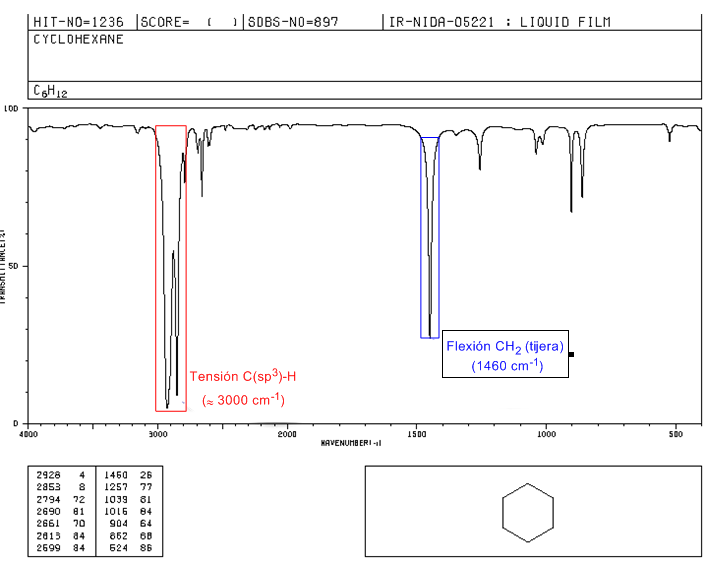
Obsérvese la ausencia de la banda de flexión simétrica del metilo que presentan los alcanos a 1375 $cm^{-1}$.
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 71651
• Tensión C(sp2)-H: 3100 -3000 cm-1
• Tensión C=C: 1600 cm-1
• Flexión fuera del plano (oop) del enlace C=C-H: 1000 - 650 cm-1. Este tipo de banda permite conocer el grado de sustitución del alqueno.
Espectro IR del 1-Penteno
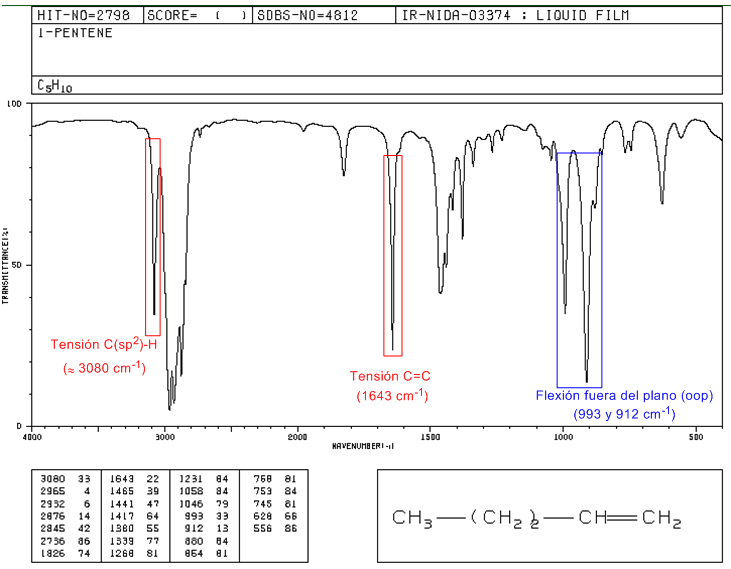
En los alquenos monosustituidos, como el 1-penteno, las flexiones C-H fuera del plano producen dos bandas situadas en 1005-985 y 920-900 $cm^{-1}$.
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 5410
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 48038
♦ Tensión $\equiv C-H$: 3300 $cm^{-1}$
♦ Tensión $-C\equiv C-$: 2150 $cm^{-1}$. Los alquinos simétricos no presentan esta banda, siendo muy débil en los internos. La conjugación baja ligeramente el valor.
Espectro IR del 1-hexino
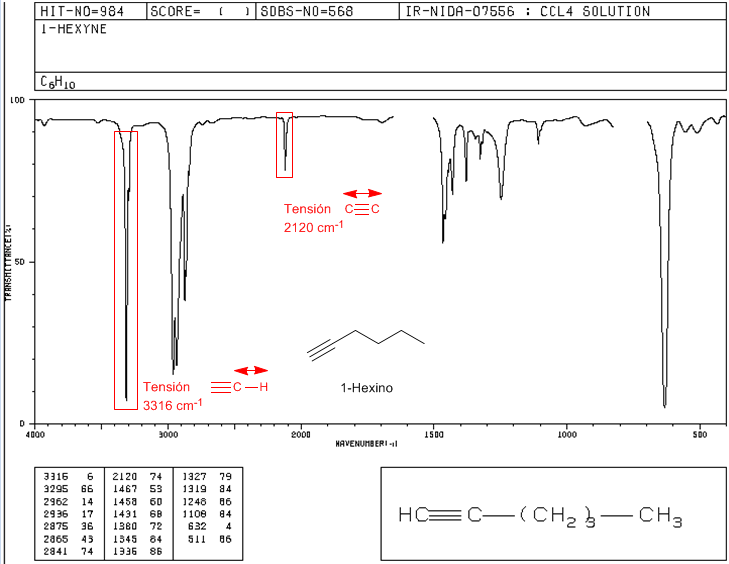
En el espectro, además de las bandas características del alquino, se observan las bandas de tensión C-H de la cadena (por debajo de 3000) y las bandas de flexión en tijera del CH2 (1467) y las de flexión simétrica y asimétrica del metilo.
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 4035
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 101278
♦ Tensión =C-H: 3100 cm-1
♦ Tensión -C=C-: 1600 y 1475 cm-1
♦ Flexión =C-H fuera del plano: 900-690 cm-1
Las vibraciones oop junto con los sobretonos y bandas de combinación que aparecen entre 2000 y 1667 cm-1 permiten conocer el grado de sustitución del benceno.
Espectro IR del tolueno
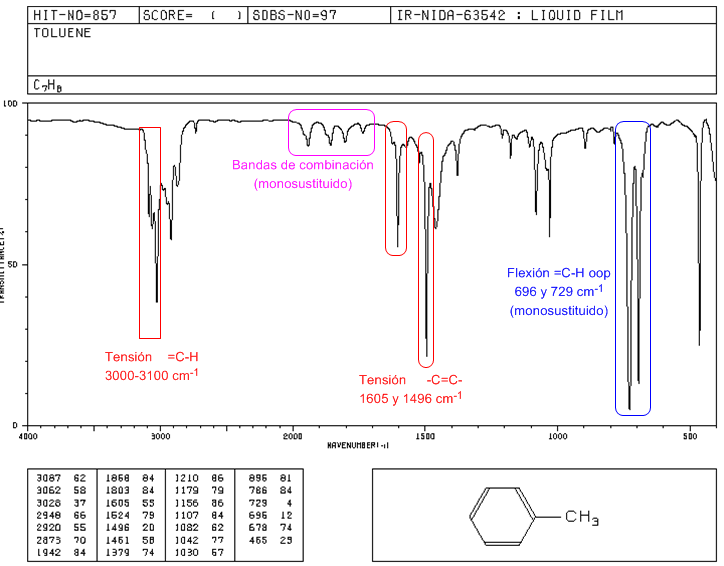
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 6111
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 5012
Pulsa en las diferentes bandas del espectro para excitar el modo vibracional correspondiente en el modelo molecular
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 109192
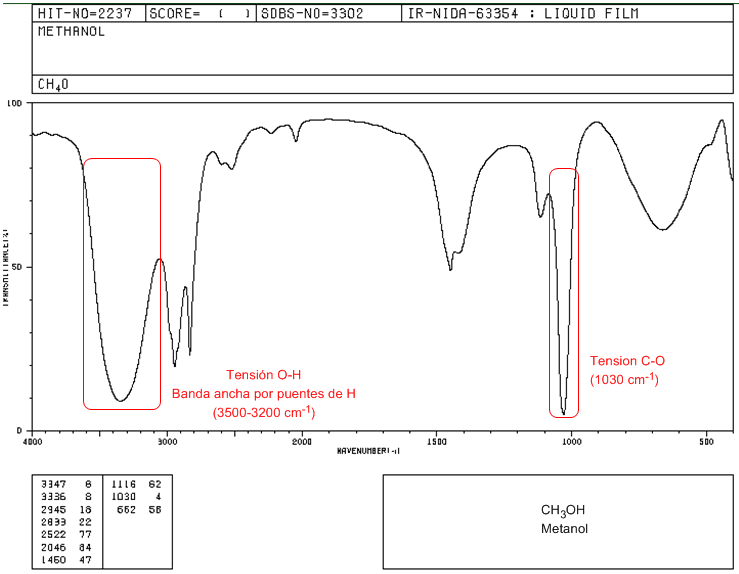
♦ Tensión O-H: Banda ancha desde 3500 a 3200 cm-1. En ausencia de puentes de hidrógeno aparece como un pico agudo a 3650-3600 cm-1.
♦ Tensión C-O: Banda comprendida entre 1250-1000 cm-1. Permite distinguir entre alcoholes primarios (1050 cm-1), secundarios (1100 cm-1), terciarios (1150 cm-1) y fenoles (1220 cm-1).
Espectro IR del metanol
En el espectro del metanol podemos observar la banda de tensión O-H, muy ancha, por formación de puentes de hidrógeno. La banda de tensión C-O sale a número de ondas bajo (1030) por tratarse de un alcohol sin sustituyentes.
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA DE INFRARROJO
- Visto: 64224
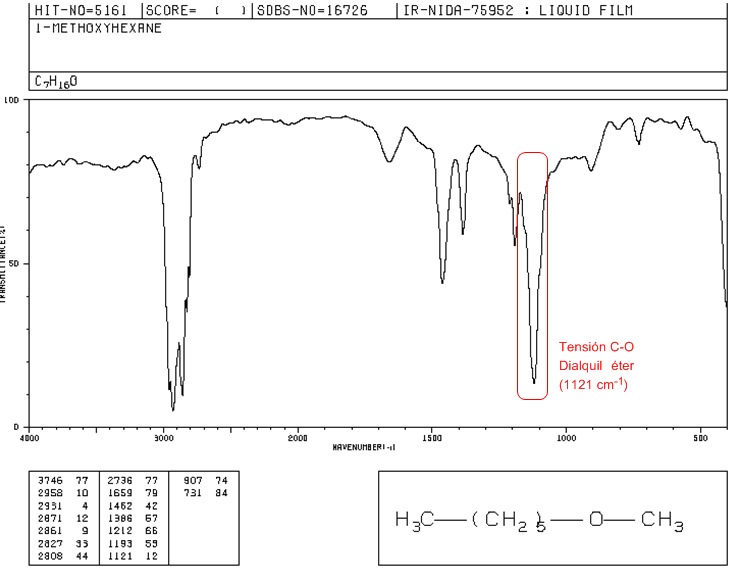
♦ Tensión C-O: 1300-1100 cm-1. Los dialquil éteres (R-O-R) presentan una banda a 1120 cm-1
♦ Los alquil vinil éteres (CH2=CH-O-R) presentan dos bandas a 1220 y 850 cm-1. Esta última muy débil.
♦ Los aril alquil éteres (Ar-O-R) presentan dos bandas a 1250 y 1040 cm-1
Espectro IR del 1-Metoxihexano
El 1-metoxihexano presenta una banda de tensión C-O a 1120 cm-1