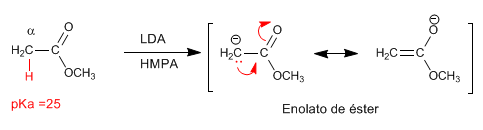
Gli esteri hanno idrogeni acidi con pKa=25 nella loro posizione, che possono essere sottratti usando basi. La base coniugata è un estere enolato, una specie altamente nucleofila che attacca un numero vario di elettrofili.
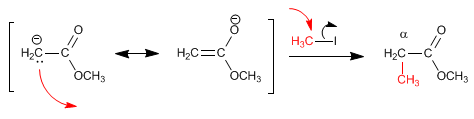
Reazione di enolati di esteri con aloalcani primari
L'estere enolato agisce come un nucleofilo, reagendo con gli aloalcani primari tramite il meccanismo S N 2. Gli aloalcani secondari e terziari danno principalmente eliminazioni, a causa della significativa basicità dell'enolato.
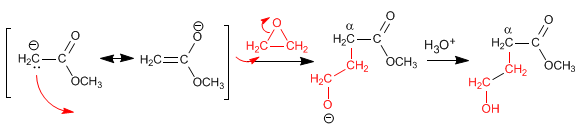
Reazione di enolati di esteri con ossaciclopropano (epossidi)
L'estere enolato attacca e apre l'ossaciclopropano. L'ossaciclopropano contribuisce al carbonio a dell'enolato una catena con due atomi di carbonio, che contiene un -OH sul secondo carbonio.
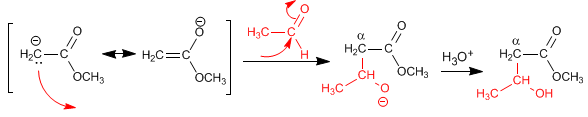
Reazione di enolati di esteri con aldeidi e chetoni
Il prodotto finale in condizioni adeguate può ciclizzare per formare un lattone.