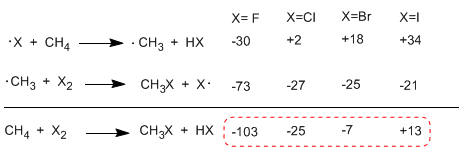Confrontando le entalpie degli stadi di propagazione dei diversi alogeni si osservano differenze importanti nei calori scambiati. Nel caso del fluoro, entrambi gli stadi sono esotermici (anche l'estrazione dell'idrogeno) con un bilancio energetico globale di -103 Kcal/mol. Le energie di attivazione degli stati di transizione in questa reazione sono molto basse, rendendolo l'alogeno più reattivo.
All'altro estremo della reattività c'è lo iodio, la cui reazione è endotermica e non avviene.
Ordine di reattività F2 > Cl2 > Br2 > I2
La tabella seguente mostra il calore scambiato negli stadi di propagazione per l'alogenazione del metano.
La reazione è fortemente esotermica nel caso del fluoro (alogeno più reattivo) mentre nel caso dello iodio è endotermica a 13 Kcal/mol.