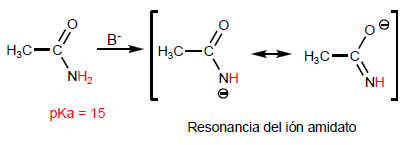
I derivati acidi si comportano come basi attraverso l'ossigeno carbonilico. La basicità di questo ossigeno dipende dalla stabilizzazione della risonanza dell'acido coniugato.
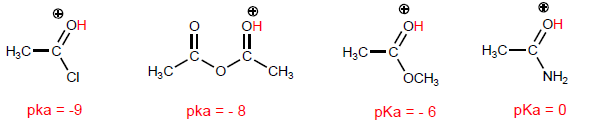
Confrontiamo le strutture che stabilizzano la base sull'alogenuro e sull'ammide.
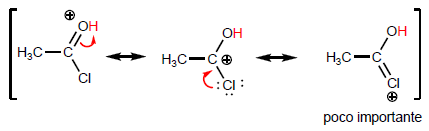
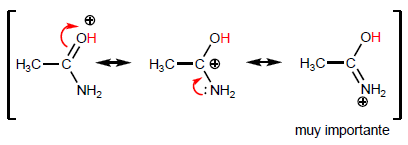
Man mano che l'ultima struttura aumenta di peso, l'acido diventa più stabile (debole) e quindi la base più forte. Le ammidi sono le basi più forti di tutti i derivati degli acidi.
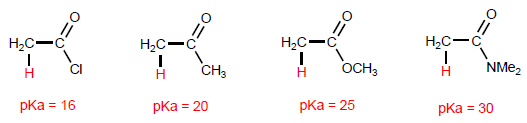
I derivati acidi presentano idrogeni acidi su carbonio.
Gli alogenuri alcanoilici hanno gli idrogeni più acidi nella posizione a , mentre le ammidi hanno il meno acido.
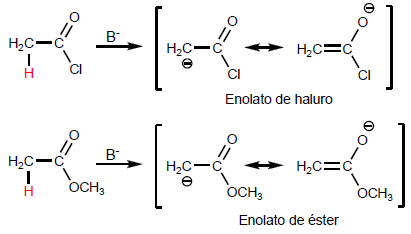
La deprotonazione della posizione produce enolati
Le ammidi hanno idrogeni molto acidi sull'atomo di azoto la cui sottrazione forma ammidati.