¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp. .
Más información en www.foroquimico.com
Si prefieres un curso de química orgánica tanto básica como avanzada te invito a acceder al canal: https://www.youtube.com/channel/UC_RiUaA2326jO9XozAA4q2g , en el que encontrarás más de 750 vídeos de teoría y ejercicios.
- Detalles
- Germán Fernández
- TEORÍA DE ALQUINOS
- Visto: 77051
Los alquinos se pueden preparar mediante doble deshidrohalogenación de dihaloalcanos vecinales o geminales.
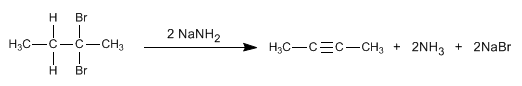
Leer más: Preparación de Alquinos Mediante Doble Eliminación
- Detalles
- Germán Fernández
- TEORÍA DE ALQUINOS
- Visto: 125600
- Detalles
- Germán Fernández
- TEORÍA DE ALQUINOS
- Visto: 84299
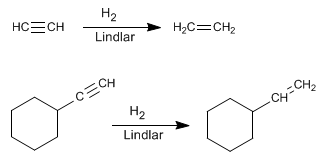
Leer más: Hidrogenación de Alquinos con Catalizador de Lindlar
- Detalles
- Germán Fernández
- TEORÍA DE ALQUINOS
- Visto: 65866
Una alternativa a la hidrogenación con el catalizador de Lindlar es la reducción de alquinos con sodio o litio en amoniaco líquido, la diferencia radica en el alqueno obtenido. Así, la hidrogenación con el catalizador de Lindlar produce alquenos cis, mientras la hidrogenación con sodio en amoniaco líquido genera alquenos trans.
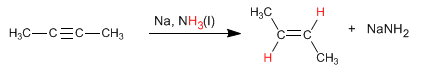
Leer más: Hidrogenación de Alquinos con Sodio en Amoniaco Líquido
- Detalles
- Germán Fernández
- TEORÍA DE ALQUINOS
- Visto: 128282
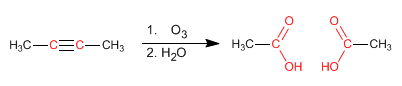
Los alquinos reaccionan con ácido sulfúrico acuoso en presencia de un catalizador de mercurio para formar enoles. El enol isomeriza (tautomeriza) rápidamente en las condiciones de reacción para dar aldehídos o cetonas.
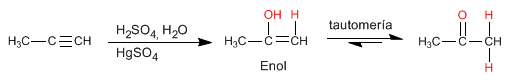
- Detalles
- Germán Fernández
- TEORÍA DE ALQUINOS
- Visto: 69069
La hidroboración es la hidratación antiMarkovnikov de un alquino. Como reactivo se emplea un borano impedido (diciclohexilborano o diisoamilborano) obteniéndose un enol que tautomeriza a aldehído o cetona. Los alquinos terminales dan lugar a aldehídos los internos a cetonas.
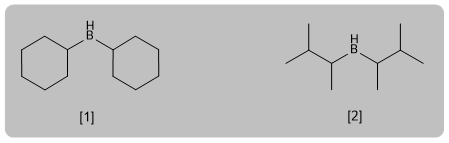
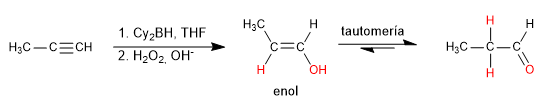
- Detalles
- Germán Fernández
- TEORÍA DE ALQUINOS
- Visto: 99383
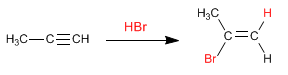
De forma similar a los alquenos, los alquinos adicionan haluros de hidrógeno (HBr, HCl, HI) al triple enlace para formar haluros de alquenilo.
- Detalles
- Germán Fernández
- TEORÍA DE ALQUINOS
- Visto: 132128
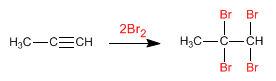
- Detalles
- Germán Fernández
- TEORÍA DE ALQUINOS
- Visto: 89774