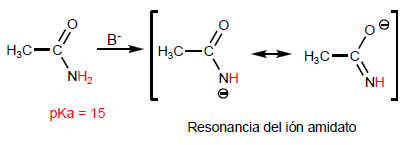
Derivados ácidos se comportam como bases através do oxigênio carbonílico. A basicidade deste oxigênio depende da estabilização da ressonância do ácido conjugado.
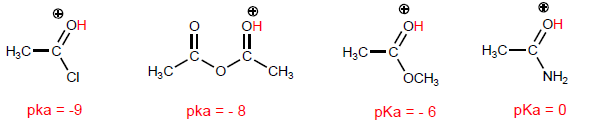
Vamos comparar as estruturas que estabilizam a base no haleto e na amida.
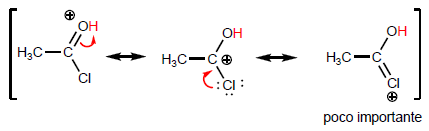
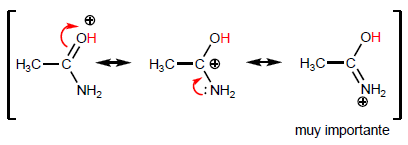
À medida que a última estrutura ganha peso, o ácido se torna mais estável (fraco) e, portanto, a base mais forte. As amidas são as bases mais fortes de todos os derivados de ácidos.
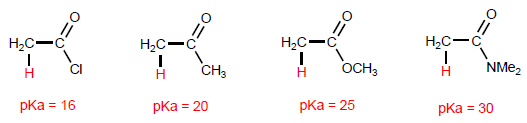
Derivados ácidos apresentam hidrogênios ácidos no carbono.
Os haletos de alcanoíla têm os hidrogênios mais ácidos na posição a , enquanto as amidas têm os menos ácidos.
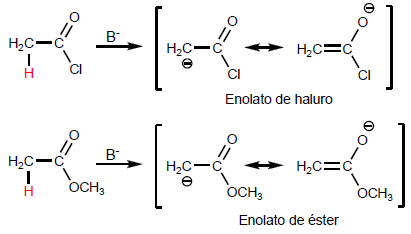
A desprotonação da posição produz enolatos
Amidas têm hidrogênios muito ácidos no átomo de nitrogênio cuja subtração forma amidatos.