¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp. .
Más información en www.foroquimico.com
Si prefieres un curso de química orgánica tanto básica como avanzada te invito a acceder al canal: https://www.youtube.com/channel/UC_RiUaA2326jO9XozAA4q2g , en el que encontrarás más de 750 vídeos de teoría y ejercicios.
HETEROCICLOS - AROMATICIDAD
- Detalles
- Germán Fernández
- HETEROCICLOS - AROMATICIDAD
- Visto: 3081
- Detalles
- Germán Fernández
- HETEROCICLOS - AROMATICIDAD
- Visto: 9998
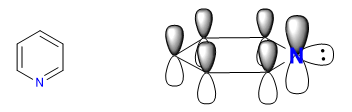
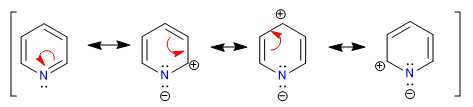
A) Heterociclos de 6 átomos y 6 electrones p.
- Detalles
- Germán Fernández
- HETEROCICLOS - AROMATICIDAD
- Visto: 4491
Existen varios criterios para determinar el grado de aromaticidad de un heterociclo:
A) Longitudes de enlace.
Un heterociclos es tanto más aromático cuanto menor diferencia exista entre las longitudes de los diferentes enlaces que componen el anillo. El benceno tiene igual longitud en todos sus enlaces carbono-carbono lo que lo convierte en el compuesto más aromático. Los heterociclos presentan diferencias en las distancias de enlace, siendo menos aromáticos cuanto mayores sean estas diferencias.
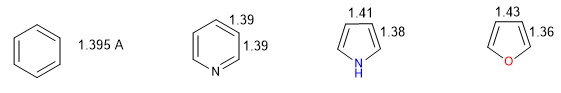
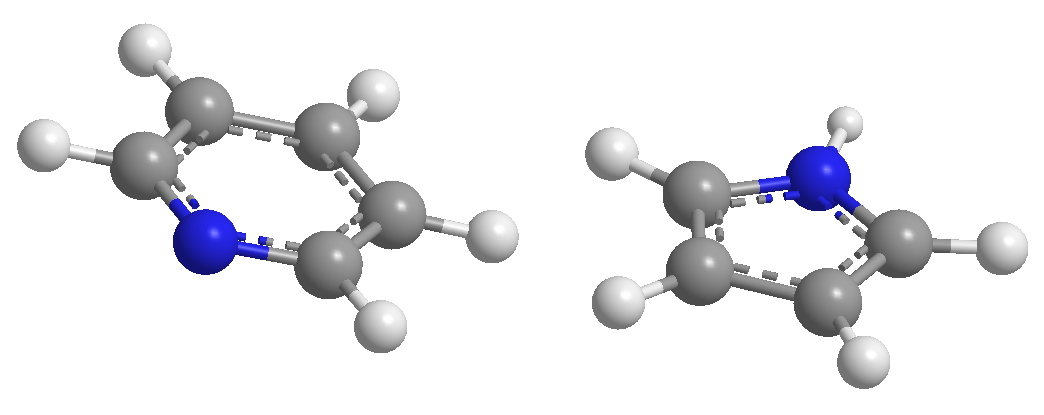
Todos los enlace C-C en el benceno miden 1.395 A, una distancia de enlace intermedia entre el enlace simpre (1.48 A) y el doble (1.34 A). En el furano se aprecia una diferencia notable entre la longitud de los enlaces, indicando una menor aromaticidad que en el pirrol. La piridina por el contrario tiene unas distancias de enlace C-C muy similares entre ellas y parecidas a las del benceno, lo que muestra una mayor aromaticidad que en pirrol o furano.
Leer más: Criterios para determinar la aromaticidad en heterociclos
- Detalles
- Germán Fernández
- HETEROCICLOS - AROMATICIDAD
- Visto: 5724
Los compuestos heteroaromáticos de 6 miembros que poseen grupos -OH o -SH en posiciones 2,4 existen preferentemente en disolución en las formas ceto o tioceto. En disolución, los compuestos con grupos amino en posiciones 2,4 existen preferentemente en la forma amino, más que como tautómero imino.
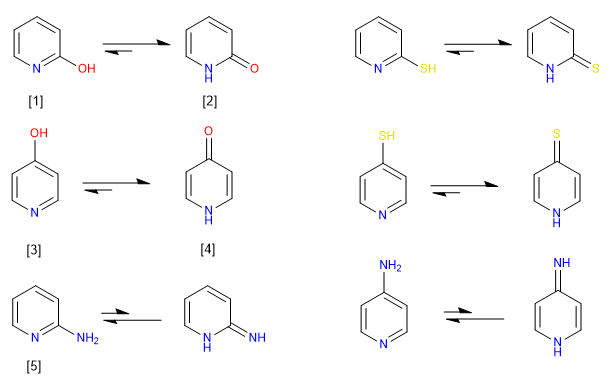
[1 ] 2-Hidroxipiridina
[2 ] 2-Piridona
[3 ] 4-Hidroxipiridina
[4 ] 4-Piridona
[5 ] 2-Aminopiridina
- Detalles
- Germán Fernández
- HETEROCICLOS - AROMATICIDAD
- Visto: 4245
En este apartado vamos a estudiar la influencia de las tensiones anulares en las propiedades de los heterociclos.
A) Tensión angular en heterociclos pequeños (3 y 4 miembros).
Los ángulos de enlace naturales de un carbono sp3 son de 109,5o, sim embargo en ciclos de tres miembros este ángulo disminuye a 60o, lo que produce una enorme tensión. Para aliviar esta tensión los enlaces entre carbonos dejan de ser rectos, doblándose, dando lugar a unos enlaces curvos denominados "enlaces banana". Los ángulos que forman estos enlaces son de 104o, una discrepancia más tolerable.
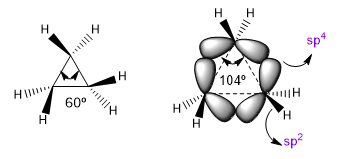
| Hibridación | Angulo de enlace |
| sp sp2 sp3 sp4 |
180º 120º 109.5º 104º |
- Detalles
- Germán Fernández
- HETEROCICLOS - AROMATICIDAD
- Visto: 5176
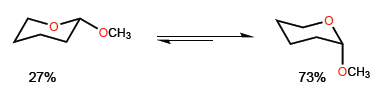
Se llama efecto anomérico al fenómeno por el que se estabiliza la conformación axial de un heterociclo sutituido en posición 2. Por ejemplo, el 2-metoxioxano presenta una proporción 27:73 a favor de la conformación con el metoxido en posición axial.