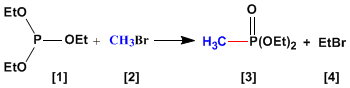¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp. .
Más información en www.foroquimico.com
Si prefieres un curso de química orgánica tanto básica como avanzada te invito a acceder al canal: https://www.youtube.com/channel/UC_RiUaA2326jO9XozAA4q2g , en el que encontrarás más de 750 vídeos de teoría y ejercicios.
REACCIONES EN QUÍMICA ORGÁNICA
- Detalles
- Germán Fernández
- REACCIONES EN QUÍMICA ORGÁNICA
- Visto: 12921
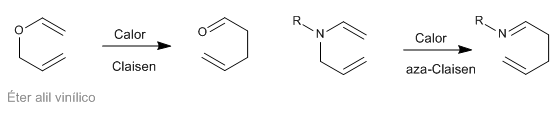
Los reagrupamientos sigmatrópicos [3,3] de las N-alilenaminas son conocidos como reagrupamiento aza-Claisen. Esta reacción es análoga a la transposición de Claisen de los éteres alíl vinílicos.
- Detalles
- Germán Fernández
- REACCIONES EN QUÍMICA ORGÁNICA
- Visto: 10962
Reacción análoga al reagrupamiento de Wittig, en el que éteres alfa metalados reagrupan a alcóxidos, generando alcoholes secundarios o terciarios después de hidrólisis. En el caso de la aza-[2,3]-Wittig se trata de aminas terciarias alílicas alfa metaladas que producen aminas secundarias después de hidrólisis.

- Detalles
- Germán Fernández
- REACCIONES EN QUÍMICA ORGÁNICA
- Visto: 18445
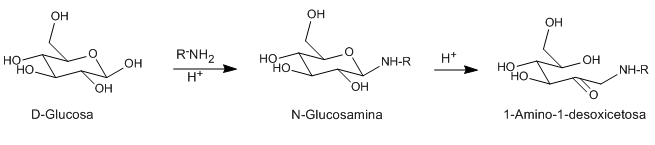
Los ácidos y las bases catalizan la isomerización de los N-glicosidos (glicosaminas) de aldosas a 1-aminodesoxicetosas. Este reagrupamiento se puede catalizar con un variado número de ácidos de Lewis (CuCl2, MgCl2, AlCl3, SnCl4). La amina utilizada como reactivo puede ser primaria o secundaria, alifática o aromática.
- Detalles
- Germán Fernández
- REACCIONES EN QUÍMICA ORGÁNICA
- Visto: 17909
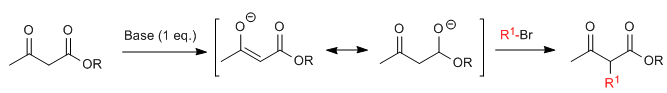
La síntesis acetilacética permite preparar cetonas mediante la C-alquilación del acetilacetato de etilo (3-oxobutanoato de etilo. El acetoacetato de etilo puede ser desprotonado en las posiciones C2 o C4 dependiendo del tipo y cantidades de base utilizados. Los hidrógenos de la posición C2 presentan una acidez importante (pKa=11) debido a estabilización de la base conjugada sobre los dos carbonilos vecinos. En presencia de un equivalente de base (alcóxidos, LDA, NaHMDS, etc.) se forma un enolato de cetoéster capaz de atacar a numerosos electrófilos carbonados.
- Detalles
- Germán Fernández
- REACCIONES EN QUÍMICA ORGÁNICA
- Visto: 20592
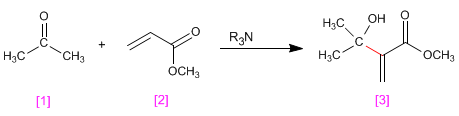
Los aldehídos y cetonas [1 ] reaccionan con compuestos a,b-insaturados [2 ] en presencia de aminas terciarias que actúan como catalizadores, para formar productos a-hidroxialquilados [3 ].
- Detalles
- Germán Fernández
- REACCIONES EN QUÍMICA ORGÁNICA
- Visto: 20237
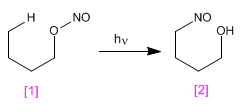
La reacción de Barton produce 4-nitrosoalcoholes [2 ] a partir de nitritos [1 ] por irradiación con luz ultravioleta.
- Detalles
- Germán Fernández
- REACCIONES EN QUÍMICA ORGÁNICA
- Visto: 29016
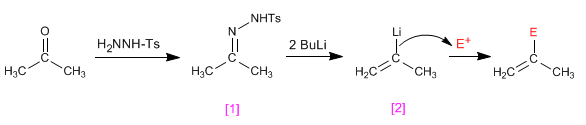
Las tosilhidrazonas de aldehidos o cetonas [1 ] reaccionan con dos equivalentes de organolíco generando un intermedio aniónico [2 ] capaz de sufrir procesos de alquilación.
- Detalles
- Germán Fernández
- REACCIONES EN QUÍMICA ORGÁNICA
- Visto: 21590
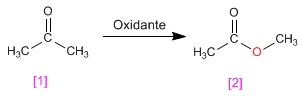
La oxidación de Baeyer Villiger permite transformar cetonas en ésteres.
- Detalles
- Germán Fernández
- REACCIONES EN QUÍMICA ORGÁNICA
- Visto: 24722
La condensación de claisen supone la reacción de ésteres [1 ] en medio básico formando 3-cetoésteres [2 ]
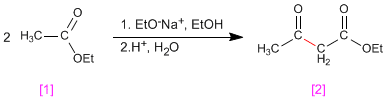
- Detalles
- Germán Fernández
- REACCIONES EN QUÍMICA ORGÁNICA
- Visto: 33384
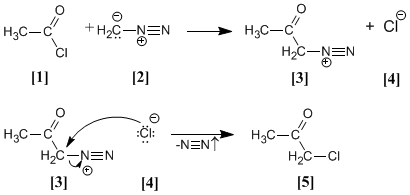
Cloruro de acetilo [1 ] se trata con diazometano [2 ] rindiendo la sal de diazonio [3 ]. El cloruro [4 ] producido reacciona con la sal de diazonio para dar la α-clorocetona [5 ].
- Detalles
- Germán Fernández
- REACCIONES EN QUÍMICA ORGÁNICA
- Visto: 21655
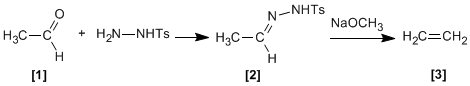
Tosilhidrazonas [2 ] de aldehídos o cetonas alifáticos [1 ] reaccionan con bases fuertes para dar alquenos [3 ].
- Detalles
- Germán Fernández
- REACCIONES EN QUÍMICA ORGÁNICA
- Visto: 41716
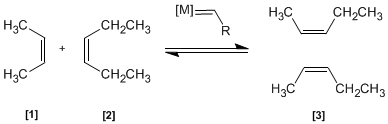
En esta reacción dos alquenos [1 ] y [2 ] son tratados con un metal de transición que actúa como catalizador, dando una mezcla de alquenos [3 ] (incluyendo isómeros Z/E). Este productos se obtiene por intercambio de grupos alquilideno.
- Detalles
- Germán Fernández
- REACCIONES EN QUÍMICA ORGÁNICA
- Visto: 34054
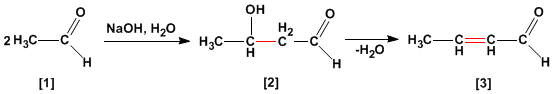
La condensación aldólica es una reacción de aldehídos o cetonas [1 ] que forma 3-hidroxicarbonilos (aldoles) [2 ]. El 3-hidroxialdehído [2 ] bajo condiciones de deshidratación por calentamiento rinde un aldehído alfa,beta-insaturado [3 ].
- Detalles
- Germán Fernández
- REACCIONES EN QUÍMICA ORGÁNICA
- Visto: 29863
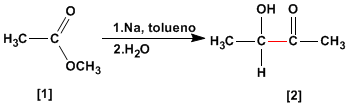
La condensación aciloínica transforma esteres [1 ] en alfa-hidroxicetonas [2 ]. Esta reacción se realiza con sodio metal en disolvente inerte.
- Detalles
- Germán Fernández
- REACCIONES EN QUÍMICA ORGÁNICA
- Visto: 27286
La reacción de Abuzov se emplea en la síntesis de fosfonatos [3 ] a partir de fosfitos [1 ]. Los fosfonatos obtenidos en la síntesis de Abuzov se emplean como materiales de partida en la síntesis de Horner-Wittig.