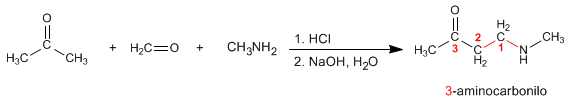¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp. .
Más información en www.foroquimico.com
Si prefieres un curso de química orgánica tanto básica como avanzada te invito a acceder al canal: https://www.youtube.com/channel/UC_RiUaA2326jO9XozAA4q2g , en el que encontrarás más de 750 vídeos de teoría y ejercicios.
TEORÍA DE AMINAS
- Detalles
- Germán Fernández
- TEORÍA DE AMINAS
- Visto: 80760
La aminación reductora consiste en formar una imina, a partir de aldehídos o cetonas y aminas, que se reduce en una etapa posterior a amina. Esta reducción puede realizarse con $H_2$ catalizado por Niquel o bien con $NaBH_3CN$.
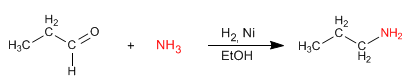
- Detalles
- Germán Fernández
- TEORÍA DE AMINAS
- Visto: 44604
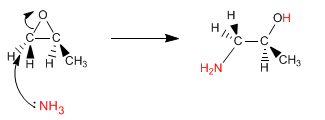
Los epóxidos (oxaciclopropanos) abren por ataque de nucleófilos, debido a la importante tensión del anillo. Si el nucleófilo empleado es amoniaco se obtiene un $\beta$-aminoalcohol. También puede obtenerse este tipo de producto abriendo el epóxido con azida de sodio, y reduciendo la azida en una segunda etapa.
- Detalles
- Germán Fernández
- TEORÍA DE AMINAS
- Visto: 97358
La eliminación de Hofmann permite convertir aminas en alquenos. Es una reacción regioselectiva que sigue la regla de Hofmann, formando el alqueno menos sustituido mayoritariamente.
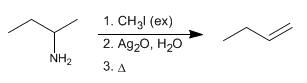
- Detalles
- Germán Fernández
- TEORÍA DE AMINAS
- Visto: 56480
La eliminación de Cope permite obtener alquenos a partir de aminas terciarias. La reacción consiste en oxidar la amina terciaria, formando un N-óxido de amina, que por calentamiento elimina de forma intramolecular, originando el alqueno.
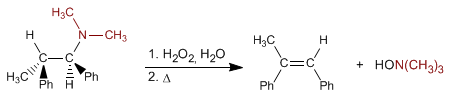
- Detalles
- Germán Fernández
- TEORÍA DE AMINAS
- Visto: 65480
Mannich prepara 3-aminocarbonilos a partir de aminas primarias o secundarias, metanal y un carbonilo enolizable. Veamos un ejemplo: