-
ferorpinel
-
 Autor del tema Autor del tema
-
Fuera de línea
-
Navegador Iniciado
-

-
Mensajes: 4
-
Gracias recibidas: 0
-
-
|
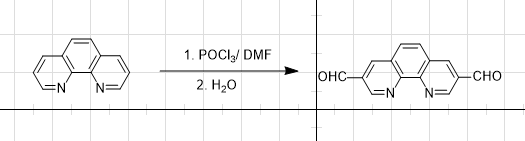
Hola, quisiera un poco de ayuda en la síntesis de un aldehído derivado de la fenantrolina (adjunto imagen) por medio de la reacción de Vilsmeier-Haack, mi duda es si es posible añadir el grupo aldehídico en la posición meta respecto al nitrógeno (ambos lados, esta es la posición que me interesa) o si es el nitrógeno el que ataca al electrófilo de Vilsmeier, y de ser posible, que condiciones podrían emplearse.
Gracias de antemano.
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
-
Germán Fernández
-

-
Fuera de línea
-
Administrador
-

-
Mensajes: 2822
-
Gracias recibidas: 752
-
-
|
Hola, el electrófilo de Vilsmeier es débil y requiere de anillos muy ricos en densidad electrónica (pi excedentes) para reaccionar, como son pirrol, tiofeno o furano.
Incluso con el benceno reacciona mal, con la excepción de bencenos fuertemente activados.
Para poner un grupo formilo en una piridina yo haría una bromación (la piridina orienta a su posición 3) seguida de una litiación, con posterior adición de dimetilformamida.
La posición en la que entra el electrófilo viene dada por la estabilidad del intermedio, que se determina por deslocalización de la carga positiva. En el caso de la piridina conviene evitar las estructuras que dejan la carga sobre el nitrógeno, muy inestables. Gran trabajo el que has hecho en ese sentido, Begoña.
Saludos a ambos.
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
Tiempo de carga de la página: 0.192 segundos