1. Éteres a partir de alcoholes primarios
Los éteres simétricos pueden prepararse por condensación de alcoholes. La reacción se realiza bajo calefacción (140ºC) y con catálisis ácida. Así, dos moléculas de etanol condensan para formar dietil éter.
El mecanismo de la reacción transcurre en las siguientes etapas:
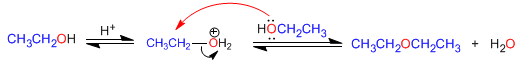
2. Uno de los alcoholes es secundario o terciario
En este caso la reacción transcurre en condiciones más suaves, a través de mecanismos SN1.
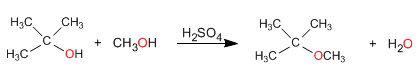
El mecanismo transcurre con formación de un carbocatión terciario de gran estabilidad
Etapa 1. Protonación del alcohol terciario
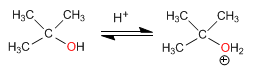
Etapa 2. Formación del carbocatión por pérdida de agua
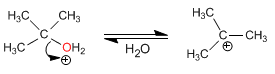
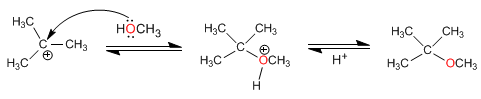
Etapa 3. Ataque nucleófilo del metanol
 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?