El número máximo de estereoisómeros que presenta una molécula puede calcularse con la fórmula (2n), donde n representa el número de carbonos asimétricos. Así una molécula con 2 centros quirales presenta 4 estereoisómeros.
Ejemplo 1. Dibujar los posibles estereoisómeros del 2-Bromo-3-clorobutano.
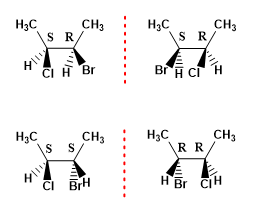
El 2-Bromo-3-clorobutano presenta 4 estereoisómeros al tener dos centros quirales. Estos cuatro estereoisómeros se clasifican en dos parejas de enantiómeros.
Ejemplo 2. Dibujar los estereoisómeros del 1,2-Dimetilciclohexano.
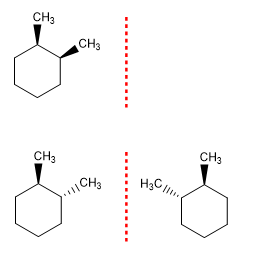
El 1,2-Dimetilciclohexano tiene dos centros quirales. Por tanto, el número máximo de estereoisómeros es: 2n = 4. La simetría de la molécula puede hacer que algunos estereoisómeros no existan. Así, el cis-1,2-dimetilciclohexano carece de enantiómero al ser una forma meso y el número de estereoisómeros es 3.
 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?