 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp. .
Más información en www.foroquimico.com
Si prefieres un curso de química orgánica tanto básica como avanzada te invito a acceder al canal: https://www.youtube.com/channel/UC_RiUaA2326jO9XozAA4q2g , en el que encontrarás más de 750 vídeos de teoría y ejercicios.
AZUFRE, FÓSFORO Y SILICIO
- Detalles
- Germán Fernández
- AZUFRE, FÓSFORO Y SILICIO
- Visto: 20006
Los tioles se caracterizan por contener el grupo funcional -SH. Se nombran terminando el nombre de la cadena principal en -tiol, de forma análoga a los alcoholes cuya terminación es -ol
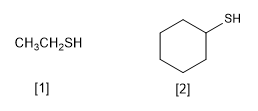
[1 ] Etanotiol
[2 ] Ciclohexanotiol
Los tioles presentan una mayor acidez que los alcoholes debido al mayor tamaño del azufre en comparación con el oxígeno. Los valores de pKa se sitúan en torno a 10 - 11, frente a los alcoholes que tienen valores compendidos entre 16-18.
- Detalles
- Germán Fernández
- AZUFRE, FÓSFORO Y SILICIO
- Visto: 13253
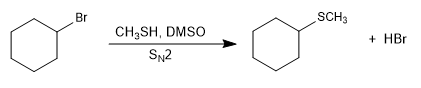
Son compuestos similares a los éteres en los que se reemplaza el oxígeno por azufre (R-S-R). También se denominan sulfuros.
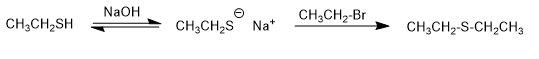
- Detalles
- Germán Fernández
- AZUFRE, FÓSFORO Y SILICIO
- Visto: 7124
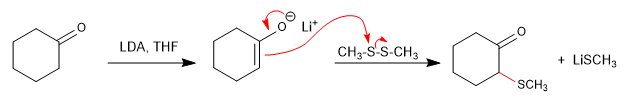
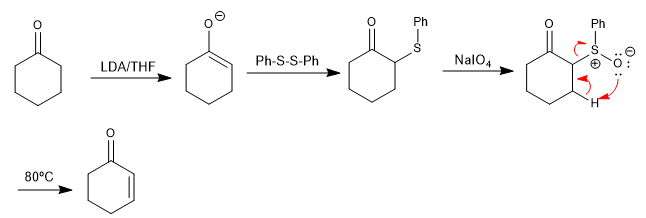
Los sulfóxidos sufren reacciones de eliminación, bajo ligera calefacción, para formar alquenos. El sulfóxido se puede preparar fácilmente por oxidación de un tioéter, el cual es fácil de formar en la posición alfa de un carbonilo a partir de un disulfuro. Este procedimiento permite la preparación a carbonilos $\alpha,\beta$-insaturados.
- Detalles
- Germán Fernández
- AZUFRE, FÓSFORO Y SILICIO
- Visto: 8867
Los iluros de azufre se preparan a partir de tioéteres por alquilación, seguido de desprotonación.
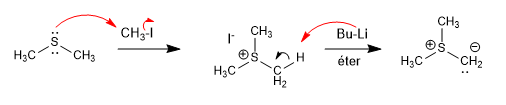
[1 ] Iluro de azufre
- Detalles
- Germán Fernández
- AZUFRE, FÓSFORO Y SILICIO
- Visto: 11195
La reacción de carbonilos con tioles forma tioacetales que pueden utilizarse como grupos protectores o para reducir el carbonilo a alcano.
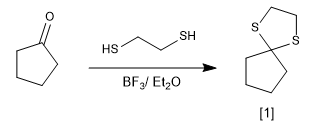
[1 ] Tioacetal
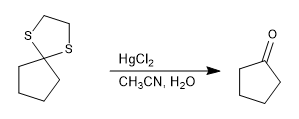
El tioacetal es estable en medios ácidos pero puede hidrolizarse con sales de mercurio (II).
- Detalles
- Germán Fernández
- AZUFRE, FÓSFORO Y SILICIO
- Visto: 10758
Los 1,3-ditianos permiten cambiar la polaridad del carbono carbonilo de los aldehídos por sustracción del hidrógeno ácido, obteniéndose un organolítico capaz de atacar a gran variedad de electrófilos.
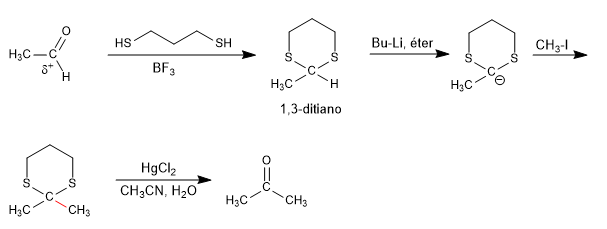
El carbonilo inicial, con polaridad positiva en el carbono, cambia en la reacción umpolung a carboanión. Los azufres del 1,3-ditiano son vitales en la estabilización de la carga negativa no siendo viable la reacción con el equivalente oxigenado.
- Detalles
- Germán Fernández
- AZUFRE, FÓSFORO Y SILICIO
- Visto: 10786
Las fosfinas se obtienen por reacción de tricloruro de fósforo con reactivos organometálicos. Así, el tricloruro de fósforo reaccióna con el bromuro de fenilmagnesio para formar trifenilfosfina.
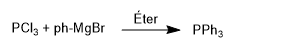
Esta reacción se controla bien y permite introducir sólo dos grupos.