El enlace carbono - hidrógeno de alquinos terminales está polarizado y muestra una ligera tendencia a ionizarse.
El Hidrógeno del propino es débilmente ácido, con un pKa = 25. Utilizando bases fuertes (NaH, LDA, NH2-) se puede desprotonar, obteniéndose su base conjugada -propinil sodio- una especie muy básica y nucleófila.
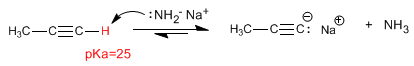
El propinil sodio generado en la reacción anterior puede actuar como nucleófilo atacando a haloalcanos primarios mediante mecanismo SN2.
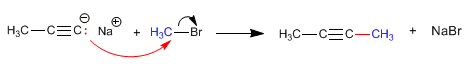
Las bases derivadas de alcoholes y agua son demasiado débiles para desprotonar los alquinos, estando los equilibrios ácido-base muy desplazados a la izquierda.
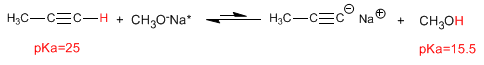
Un equilibrio ácido-base se desplaza hacia el ácido conjugado de mayor valor de pKa.
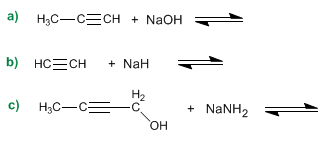
Ejemplo: completar los siguientes equilbrios ácido-base
 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?