 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp. .
Más información en www.foroquimico.com
Si prefieres un curso de química orgánica tanto básica como avanzada te invito a acceder al canal: https://www.youtube.com/channel/UC_RiUaA2326jO9XozAA4q2g , en el que encontrarás más de 750 vídeos de teoría y ejercicios.
-
Detalles
-
Germán Fernández
-
PROBLEMAS DE ALQUENOS
-
Visto: 19742
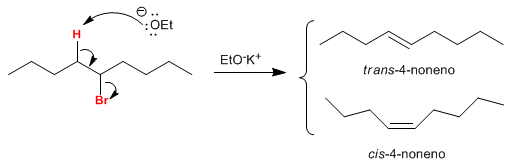
En la reacción de eliminación del 5-bromononano con etóxido de potasio en etanol dibuje las proyecciones de Newmann que muestren la conformación que conduce al cis-4-noneno y al trans-4-noneno, respectivamente. Indique el hidrógeno que se pierde en cada caso y sugerir un mecanismo que explique la estereoselectividad observada.
Solución
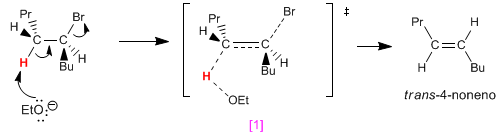
En el carbono b del haloalcano hay dos hidrógenos que al colocarse anti con respecto al grupo saliente, generan los dos isómeros. El isómero trans se obtienen en mayor cantidad, por ser de menor energía el estado de transición de la reacción que lo forma.
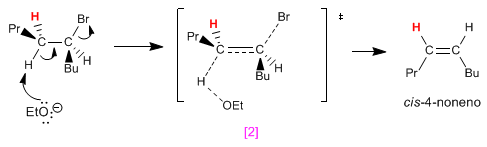
Rotando el carbono de la izquierda 120º, colocamos el hidrógeno negro anti con respecto al bromo. La eliminación de este hidrógeno forma el alqueno cis.
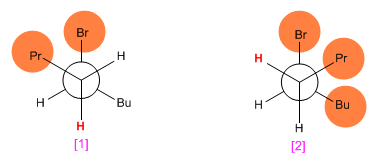
Haciendo proyecciones de Newmann de ambas conformaciones, se observa que la [1 ] tiene menos repulsiones (propilo y butilo a lados opuestos) que el [2 ]. Esto hace que el isómero trans se obtenga en más cantidad que el cis (la reacción que forma el producto trans es más rápida por tener menor energía de activación).
 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?