La síntesis acetilacética permite preparar cetonas mediante la C-alquilación del acetilacetato de etilo (3-oxobutanoato de etilo. El acetoacetato de etilo puede ser desprotonado en las posiciones C2 o C4 dependiendo del tipo y cantidades de base utilizados. Los hidrógenos de la posición C2 presentan una acidez importante (pKa=11) debido a estabilización de la base conjugada sobre los dos carbonilos vecinos. En presencia de un equivalente de base (alcóxidos, LDA, NaHMDS, etc.) se forma un enolato de cetoéster capaz de atacar a numerosos electrófilos carbonados.
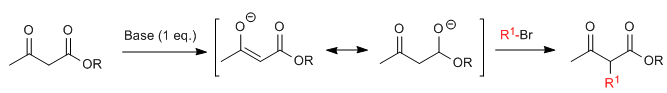
Donde R1 es un grupo alquilo primario o secundario, alilo o bencilo.
El sustrato monoalquilado es susceptible de una segunda alquilación por adición de un segundo equivalente de base seguido del electrófilo.
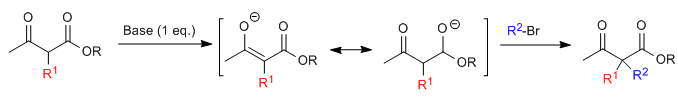
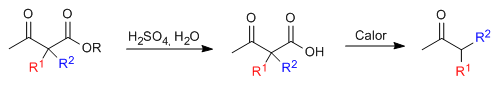
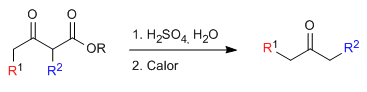
El cetoéster monoalquilado o dialquilado es sometido a continuación a una etapa de hidrólisis ácida que lo transforma en un cetoácido sensible a la descarboxilación por calefacción.
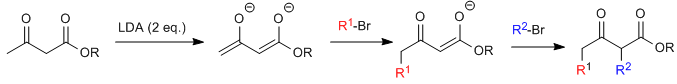
 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?






