DESCONEXIÓN DE COMPUESTOS 1,4-DIOXIGENADOS
Otro grupo de compuestos de mucha importancia en la síntesis química, lo constituyen las moléculas dioxigenadas que se hallan en una relación de distancia 1,4. Estos compuestos cuando se someten a un análisis de desconexión retrosintético, generan sintones, en donde uno de ellos, el electrófilo o nucleófilo, puede ser considerado “anómalo” o “ilógico”, en razón a que la carga asignada a uno de los átomos no puede explicarse en términos de la electronegatividad intrínseca o inducida del mismo.
1. Compuestos 1,4-dioxigenados (1,4-diO)
En este tipo de compuestos, la desconexión conduce también a un sintón lógico y a otro sintón ilógico (no natural), que puede ser un nucleófilo o un electrófilo, cuyo equivalente sintético, tiene que ser todavía reelaborado adecuadamente, para poder ser utilizado en la reacción química.
1. 1. Compuestos 1,4-dicarbonílicos
1.1.1. Compuestos 1,4- dicetónicos
Las alternativas de desconexión de este tipo de compuestos o moléculas a ser sintetizadas (MOb), pueden conducir a las siguientes opciones:
a. Un sintón aniónico lógico y un sintón catiónico ilógico
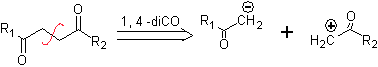
El equivalente sintético del anión es el ión enolato o el mismo enol del compuesto carbonílico. En cambio el equivalente sintético para el carbocatión es el alfa halocarbonilo. (Umpoloung)
b. Un sintón catiónico lógico y un sintón aniónico ilógico
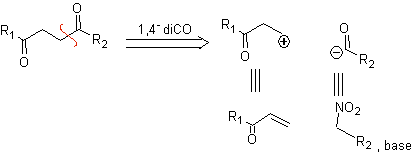
El equivalente sintético del sintón catiónico lógico es el compuesto carbonílico α, β– insaturado. Un equivalente sintético adecuado para el sintón aniónico puede ser un anión de nitroalcano. El grupo –NO2 en los alcanos puede transformarse en C=O, por medio de la reacción de Nef, o por la variantes de la reacción de McMurry, donde por acción de TiCl3, el nitroalcano es transformado en una imina, que luego es hidrolizada en medio ácido al compuesto carbonílico respectivo..
1.1.2. Compuestos 1,4-cetoésteres
Los γ- cetoésteres, los 1,4-diésteres y los 1,4- diácidos se pueden desconectar a un sintón catiónico natural, cuyo equivalente sintético es un compuesto carbonílico α, β insaturado, y al sintón aniónico no natural (“ilógico”) (-) COOR, cuyo equivalente sintético es el ión cianuro.
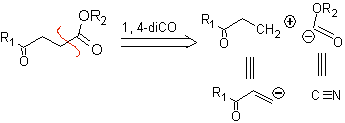
Ejemplos: Proponer un diseño de síntesis, a partir de materiales simples y asequibles, para cada una de las siguientes moléculas:
|
MOb 35
|
|
MOb 36
|
|
|
|
|
|
MOb 37
|
|
MOb 38
|
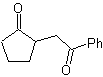
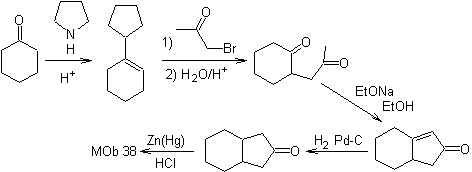
MOb 35 (a). Análisis retrosintético. La molécula puede desconectarse según el modelo 1,4-diCO. La ciclopentanona precursora generada, deberá de activarse previamente para que su Cα, sea más nucleófilo, y ser luego utilizado en la reacción con la α.bromoacetona.
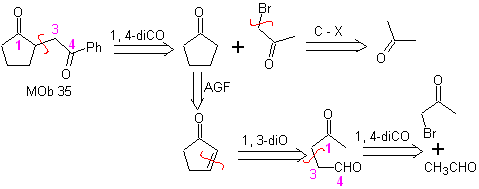 Síntesis. Se controla y garantiza la nucleofilicidad de la ciclopentanona, utilizando LDA, para llegar a
Síntesis. Se controla y garantiza la nucleofilicidad de la ciclopentanona, utilizando LDA, para llegar a
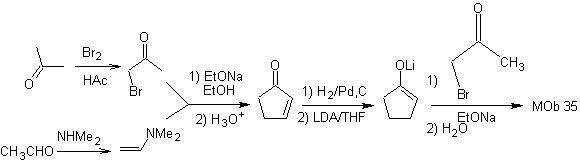
MOb 35 (b). Análisis retrosintético. El modelo 1,4-diCO que presenta
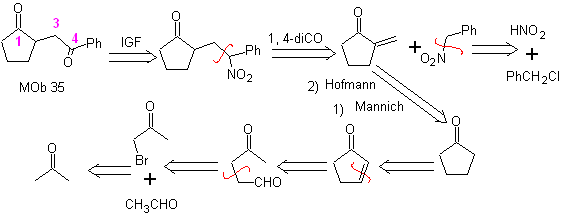
Síntesis. Asimismo, la última etapa, para llegar a
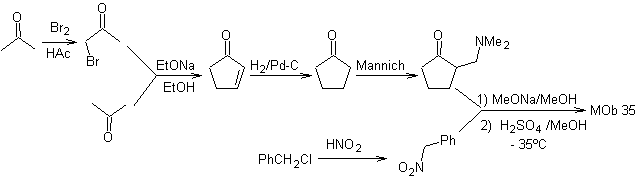
El uso de nitroalcanos o nitroarenos secundarios, genera como producto cetonas, por la reacción de Nef, razón por la cual esta metodología solo es aplicable a compuestos 1,4-cetoésteres, 1,4-cetocetonas y 1,4-cetoaldehidos.
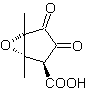
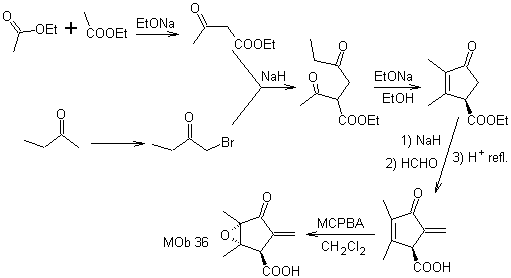
MOb 36. Análisis retrosintético. En primera instancia, el grupo carboxílico de
Se debe comprender que el doble enlace del anillo es más reactivo a la epoxidación, que el otro enlace doble. La desconexión α,β-insat CO posterior, permite formar una estructura más fácil de desconectar por los modelos dioxigenados generados en las moléculas intermedias.
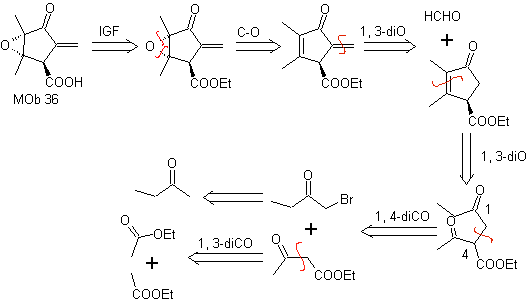
Síntesis. El único cuidado que se debe tener en esta síntesis e la epoxidación del doble enlace anular, más reactivo que el doble enlace vinílico, luego las reacciones para llegar a la síntesis de
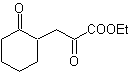
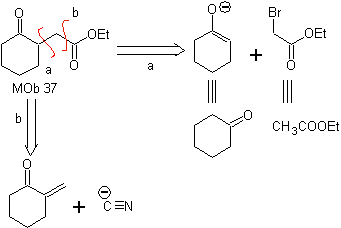
MOb 37. Análisis retrosintético: La desconexión de
Síntesis: Se sigue la desconexión (a). La hidrólisis al final debe ser controlada, para no afectar al grupo éster de MOb 37
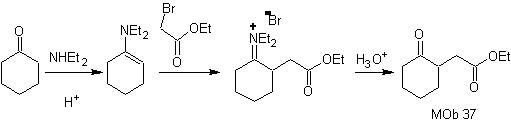
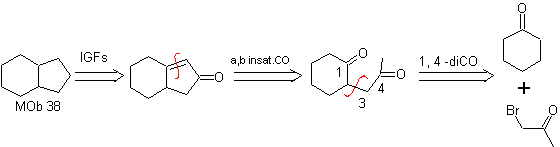
Síntesis. Se recurre nuevamente a la enamina de la ciclohexanona, para desplazar el halógeno de la cetona. El compuesto 1,4- diCO formado, se cicla en medio básico.
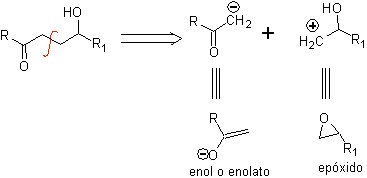
2.1.2. Compuestos g-hidroxicarbonílicos
Un compuesto γ-hidroxicarbonílico corresponde al modelo 1,4-diO, razón por la cual, la desconexión del mismo, proporciona un sintón aniónico lógico y un sintón catiónico ilógico, cuyo equivalente sintético puede ser un epóxido.
|
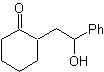
Como podría sintetizarse la siguiente molécula? |
MOb 39
|
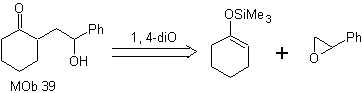
MOb 39. Análisis retrosintético. La desconexión del modelo γ-hidroxi- carbonílico, MOb 39, origina la ciclohexanona como molécula precursora y un epóxido aromático. Se tiene que buscar el enol o enolato de la cetona, que active su Cα, para aperturar el epóxido por el lado menos impedido.
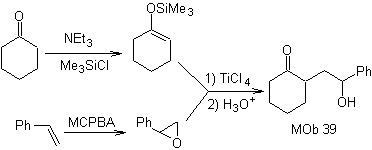
Síntesis. El sililenol éter, es un potente nucleófilo, capaz de atacar a un epóxido por el lado menos protegido, en medio ácido y catalizado por sal de Ti (IV).
 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?