¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp. .
Más información en www.foroquimico.com
Si prefieres un curso de química orgánica tanto básica como avanzada te invito a acceder al canal: https://www.youtube.com/channel/UC_RiUaA2326jO9XozAA4q2g , en el que encontrarás más de 750 vídeos de teoría y ejercicios.
|
Bienvenido,
Invitado
|
|
TEMA:
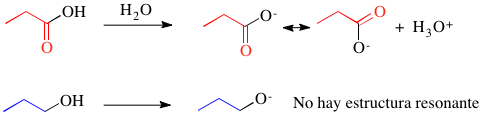
Acidez comparativa de un acido carbox y un alcohol 13 años 4 meses antes #6153
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación. |
Re: Acidez comparativa de un acido carbox y un alcohol 13 años 4 meses antes #6156
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación. |
Re: Acidez comparativa de un acido carbox y un alcohol 13 años 4 meses antes #6158
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación. |
Re: Acidez comparativa de un acido carbox y un alcohol 13 años 4 meses antes #6159
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación. |
Re: Acidez comparativa de un acido carbox y un alcohol 13 años 4 meses antes #6167
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación. |
Re: Acidez comparativa de un acido carbox y un alcohol 13 años 4 meses antes #6171
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación. |
|