A) Heterociclos com 6 átomos e 6 elétrons p .
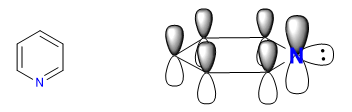
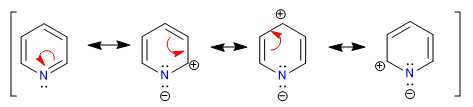
O nitrogênio mais eletronegativo atrai a nuvem de elétrons em sua direção, deixando para trás os carbonos deficientes em elétrons. Portanto, este sistema é considerado pi deficiente em relação ao benzeno. Na imagem a seguir represento as densidades médias de carga que cada carbono suporta, em um benzeno todos os carbonos suportariam uma densidade de 1.
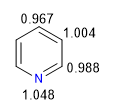
A eletronegatividade do nitrogênio causa a retenção da nuvem eletrônica sobre ele, diminuindo a aromaticidade do sistema, bem como sua capacidade de atacar eletrófilos. No entanto, reações que prosseguem com ataque nucleófilo ao anel são favorecidas.
Oito tipos de compostos aza derivados do benzeno são conhecidos:
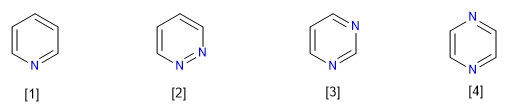
[1] Piridina
[2] Piridazina
[3] Pirimidina
[4] Pirazina
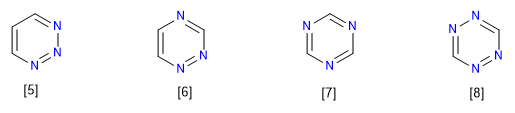
[5] 1,2,3-Triazina
[6] 1,2,4-Triazina
[7] 1,3,5-triazina
[8] 1,2,3,5-Tetrazina
Outros heterociclos pertencentes a esta família com um heteroátomo diferente do nitrogênio são:
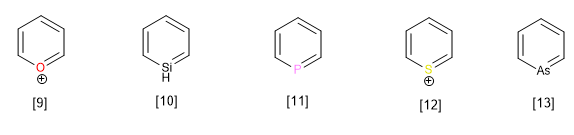
[9] Cátion pirílio
[10] Silabenzeno
[11] Fosfabenzeno
[12] Cátion Tiopirílio
[13] Arsabenzeno
B) Heterociclos de 5 átomos e 6 elétrons pi.
São compostos com excesso eletrônico ou p -excedente. Os carbonos têm uma densidade de carga mais alta que o benzeno, o que os torna muito reativos em relação aos eletrófilos, mas diminui drasticamente sua reatividade em relação aos nucleófilos. Um membro típico desta família é o pirrole.
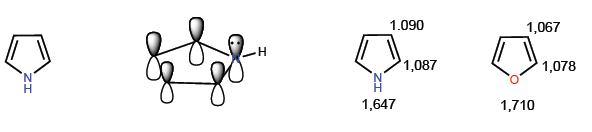
Os membros mais representativos desta família de heterociclos são:
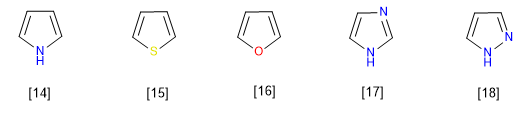
[14] Pirrole
[15] Tiofeno
[16] Furano
[17] Imidazol
[18] Pirazol
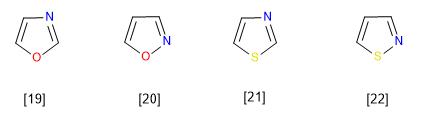
[19] Oxazol
[20] Isoxazol
[21] Tiazole
[22] Isotiazol
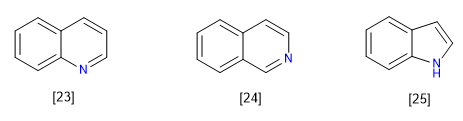
C) Sistemas condensados ou fundidos