Ciclación intramolecular (Williamson intramolecular): Alcoholes halogenados en posición 2 ciclan en medios básicos formando oxiranos.
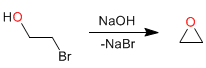
Mecanismo:
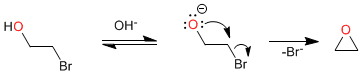
La primera etapa del mecanismo consiste en un equilibrio ácido - base que despotona el alcohol, generando un buen nucleófilo (alcóxido) que cicla en la segunda etapa mediante una SN2 intramolecular.
Epoxidación de alquenos: Los perácidos (MCPBA) reaccionan con alquenos formando oxiranos (epóxidos).

Mecanismo:
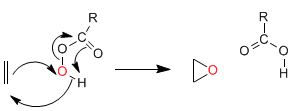
Epoxidación asimétrica de Sharples: Los alcoholes alílicos reaccionan de forma enantioselectiva con tetraisopropóxido de titanio, tert-butilhidroperóxido y (+) ó (-) tartrato de dietilo, para dar oxiranos.
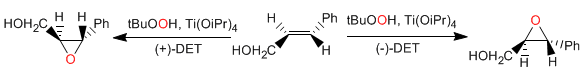
Síntesis de Darzens: La reacción parte de ésteres halogenados en posición alfa, que forman enolatos en medio básico. La reacción del enolato de éster con aldehídos o cetonas, seguida de una SN2 intramolecular, produce oxiranos.
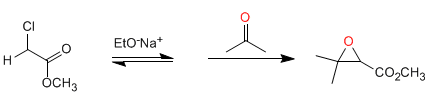
Mecanismo:
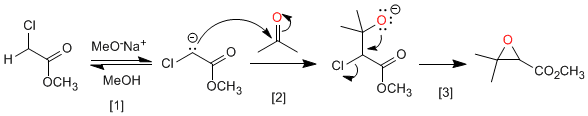
[1 ] Desprotonación de éster.
[2 ] Ataque nucleófilo del enolato de éster al carbonilo.
[3 ] Sustitución nucleófila intramolecular que genera el oxirano.
Síntesis de Corey (Iluros de azufre): Los iluros de azufre reaccionan con aldehídos o cetonas formando oxiranos.
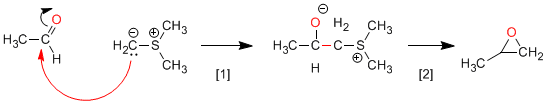
[1 ] Ataque nucleófilo del iluro al carbonilo.
[2 ] Etapa de ciclación aprovechando la capacidad del azufe como grupo saliente.
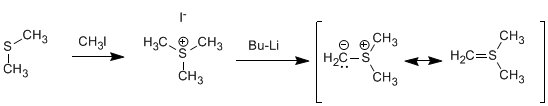
El iluro de azufre se prepara por metilación del sulfuro de dimetilo seguido de tratamiento con base fuerte
 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?