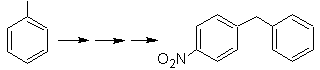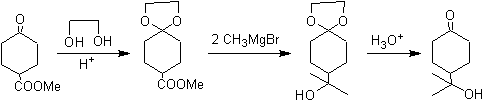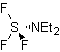SÍNTESIS ORGÁNICA
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 39126
La síntesis orgánica, corazón de la química orgánica, es una actividad esencialmente heurística, es decir, es un proceso donde se fusionan las actividades creadoras del pensamiento lógico altamente predictivas y los procedimientos empíricos, ricos en elaboración artística, que hacen del químico orgánico un verdadero innovador.
Como todo método, el “método de las desconexiones o del sintón”, tiene su estructura, simbología y lenguaje propios, que inicialmente deben de ser asimilados y comprendidos, por quiénes se disponen a utilizar esta herramienta sintética.
El método de síntesis de las desconexiones o del sintón, comprende dos fases;
![]() Fase de análisis retrosintético. En él, se muestra todas las transformaciones que se realizarán en el proceso de simplificar la estructura de
Fase de análisis retrosintético. En él, se muestra todas las transformaciones que se realizarán en el proceso de simplificar la estructura de
![]() Fase de síntesis. En donde lo “pensado”, en base a criterios de racionalidad mecanística y de reactividad de los compuestos orgánicos, se concreta en una ruta de síntesis, que será escrita, tal cual se espera ocurra en el laboratorio químico. Es donde aflora la experiencia y manifiesta el “arte de hacer o inventar” del químico, es decir
Fase de síntesis. En donde lo “pensado”, en base a criterios de racionalidad mecanística y de reactividad de los compuestos orgánicos, se concreta en una ruta de síntesis, que será escrita, tal cual se espera ocurra en el laboratorio químico. Es donde aflora la experiencia y manifiesta el “arte de hacer o inventar” del químico, es decir
Los términos, definiciones u operaciones de síntesis, recurrentemente utilizados en este método, son los siguientes:
Molécula Objetivo (MOb).
Se denomina así, a toda molécula que se desea sintetizar o preparar a partir de materiales simples y asequibles, que en un problema, pueden estar previamente definidos o estar ajustados a las opciones que el químico genere en su plan o diseño de síntesis.
Transformación. (![]() ).
).
La flecha unidireccional especial de retrosíntesis, debe entenderse como una representación simbólica de la expresión “se prepara a partir de” y también representa algún tipo de transformación en la estructura de
Los tipos de transformación al que se hace referencia, en realidad son operaciones retrosintéticas como las: Desconexiones, Reconexiones, Reordenamientos, Interconversión de Grupos Funcionales (IGF), Adición de Grupos Funcionales (AGF), Supresión de Grupos Funcionales (SGF), etc.
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 21959
Otras estrategias de síntesis
que utilizan sintones “ilógicos”
1.
Adición de triple enlace
La estrategia de "adicionar" un triple enlace, entre
dos funciones oxigenadas en posición 1,4, permite trabajar posteriormente con una desconexión
basada en la química de los acetiluros. Con el fín de ejemplificar esta estrategia, veamos la e laboración de un plan de
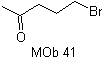
síntesis para
MOb.
40. Análisis
retrosintético. Una primera IGF en
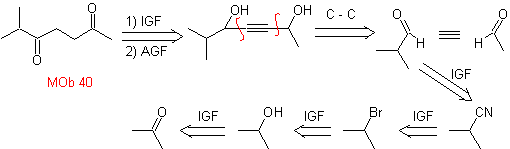
Síntesis. El diacetiluro o
acetiluro por etapas, se combina con moléculas de aldehídos diferentes, se hidrogenan la
molécula intermedia formada y seguidamente se oxida los alcoholes de la misma
al compuesto dicetónico Mob 40.
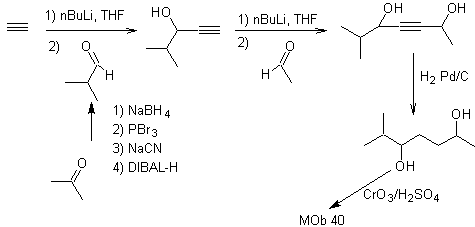
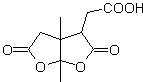
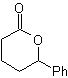
Las γ-lactonas, pueden también prepararse de manera análoga,
como se muestra a continuación:

2.
Adición del grupo COOR como grupo
activante
La adición del grupo COOR, además de activar el sintón
aniónico, facilita la desconexión de una molécula 1,4 diX.
|
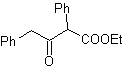
Sintetizar |
|
MOb 41. Análisis retrosintético.
Leer más: Otras estrategias de síntesis que utilizan sintones "ilógicos·
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 29209
DESCONEXIONES DE COMPUESTOS 1,3-DIOXIGENADOS
Los compuestos orgánicos oxigenados,
son los más abundantes en la naturaleza y en particular los dioxigenados, razón
por la cual, muchos investigadores químicos, han modelizado la desconexión
retrosintética de estas moléculas, aspecto que se estudiará en los siguientes
párrafos.
Para empezar, los modelos de
desconexión de moléculas dioxigenadas, se han dividido en dos grandes grupos,
atendiendo a la naturaleza de los síntones que se generan con la aplicación de
una operación sintética básica
denominada “DESCONEXIÓN” a la
molécula a ser sintetizada y que generalmente se la denomina como molécula objetivo (MOb).
Estos grandes grupos son:
![]() Modelos de desconexión “lógicos”,
y
Modelos de desconexión “lógicos”,
y
![]() Modelos de desconexión “anómalos
“ o “ilógicos”
Modelos de desconexión “anómalos
“ o “ilógicos”
Los modelos de desconexión
denominados “lógicos”, son aquellos que por la aplicación de una “desconexión”
de uno o varios enlaces químicos en
Los compuestos que pueden
clasificarse como 1,3-dioxigenados y 1,5-dioxigenados, cuando son sometidos a
una retrosíntesis, generalmente forman sintones considerados “lógico”. En
cambio, las moléculas orgánicas con relación 1,2-dioxigenadas, 1.4-dioxigenadas
y 1,6-dioxigenadas, generan sintones
considerados “ilógicos”
Modelo de desconexión
1,3-dioxigenado
![]() Compuestos β-dicarbonílicos
Compuestos β-dicarbonílicos
Los compuestos 1,3-dicarbonílicos
se obtienen con buenos rendimientos a través de reacciones de condensación del
tipo Claisen, que implican la reacción entre ésteres y compuestos con
hidrógenos activos, tales como: ésteres, cetonas, aldehídos, nitrilos,
nitroderivados y algunos hidrocarburos en presencia de reactivos alcalinos.
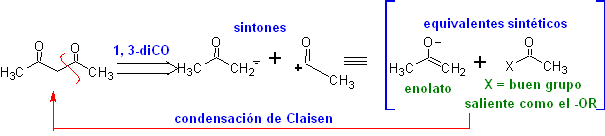
Las β-dicetonas y los β-cetoaldehidos se obtienen por la
condensación de Claisen cruzada, utilizando una cetona y un éster adecuados. En
la condensación de Claisen cruzada de cetonas y ésteres se obtienen buenos
rendimientos debido a que las cetonas son notablemente más ácidas que los
ésteres, por lo tanto, en el medio básico la cetona se desprotona en mayor
grado que el éster
Ejemplos: Proponer un diseño de síntesis a
partir de materiales simples, para las siguientes moléculas:
|
MOb 16
|
|
MOb 17
|
|
MOb 18
|
Solución:
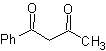
MOb 16. Aparentemente las dos alternativas
de desconexión (a) y (b), mostradas en
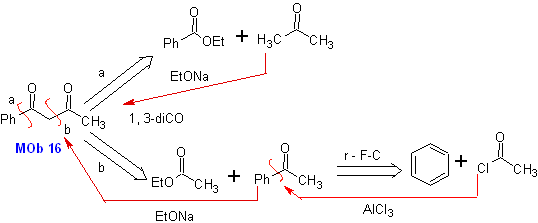
Sin embargo, la alternativa (b), resulta ser la más adecuada,
en razón a que, en el medio básico de la reacción, el carbanión formado PhCOCH2-
estaría mejor estabilizado, por efectos de resonancia e inductivos.
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 56763
SÍNTESIS DE COMPUESTOS AROMÁTICOS I
(Método del Árbol de Síntesis)
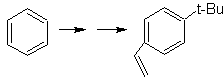
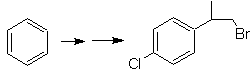
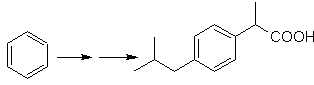
Proponer un plan de síntesis, a
partir del tolueno o xileno como materiales de partida, para las siguientes
moléculas:
|
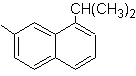
(MOb 12)
1-isopropil-7-metilnaftaleno |
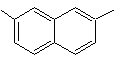
(MOb 13)
2,7-dimetilnaftaleno |
|
|
|
|
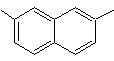
(MOb 14)
1-isopropil-6-metilnaftalen
|
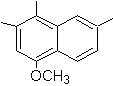
(MOb 15)
4-metox-1,2,7-trimetilnaftaleno |
Solución:
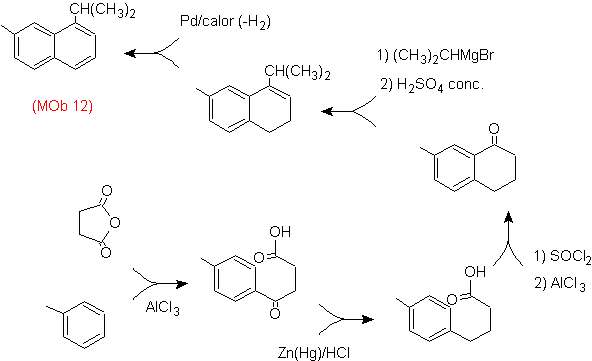
(MOb 12).
En la estrategia que se asume, se
toma en cuenta que la última etapa puede responder a un proceso de
“aromatizacion”, por lo cual se propone que la molécula precursora presenta un
anillo no aromático, con un doble enlace
sobre el carbono que contiene el doble enlace y el grupo alquilico.
Esta
estructura se puede conseguir por la acción del un Grignard sobre un carbonilo
y la posterior deshidratación del alcohol formado. La cetona se forma por la
acilación sobre el compuesto bencénico adecuado con el anhídrido succínico y
sus posteriores cierres intramoleculares de acilación de Friedel -Crafts.
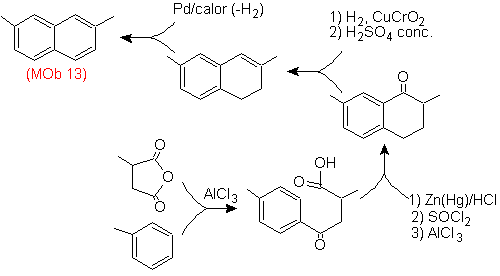
Solución (MOb
13).
Nuevamente la molécula precursora
tiene que se “aromatizada”, la estrategia mas adecuada de entre otras se basa en la combinación de acilación con
anhídrido succínico sustituido y la reducción de Clemmensen.
El
carbonilo final se reduce a alcohol que será deshidratado luego con hidrogeno
molecular y un catalizador denominado cromilo de cobre.
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 27346
Los compuestos 1,5-dioxigenados generalmente son resultado de
reacciones de adición conjugada de nucleófilos provenientes de compuestos
carbonílicos, con Hα acídicos (enoles,
enolatos, enaminas, etc.), al igual que nitrilos y nitratos, sobre sustratos
alfa beta insaturado respecto a grupos carbonílicos y similares, conocida como
reacción de Michael, siendo opciones complementarias, la reacción de Nef y la
reacción de anelación (anillación) de Robinson.
Modelo de desconexión 1, 5 dioxigenado
(1,5-diO)
El modelo de desconexión 1,5-diO, puede ser aplicado, luego
de la funcionalización necesaria, a compuestos como: 1,5-dihidroxilos,
1,5-hidroxialdehidos, 1,5-hidroxicetonas, 1,5-hidroxiésteres,
1,5-cetoaldehidos, 1,5-dicetonas, 1,5-cetoésteres, 1,5-dialdehidos, etc.
Las posibilidades se incrementan, si además se toma en cuenta
a los nitroderivados y nitrilos, que pueden formar en medio básico, carbaniones
muy reactivos capaces de adicionarse a compuestos a,b-insaturado carbonílicos,
para obtener productos del tipo 1,5-diO.
El análisis fundamental de la desconexión
de los compuestos 1,5-diO es el siguiente:
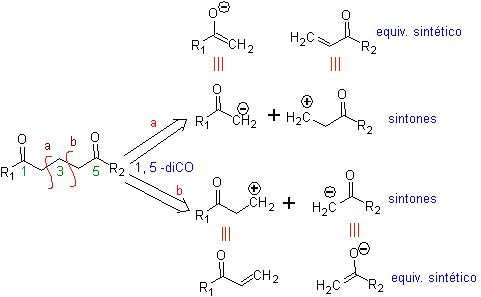
La elección de la desconexión (a) o (b), en torno al C3,
dependerá de la naturaleza de los grupos R1 y R2, que puedan conferir una mayor
o menor estabilidad al sintón o equivalente sintético necesarios para la
formación de
Proponer un diseño de síntesis para las MOb 29, 30 y
|
MOb 29
|
|
MOb 30
|
|
MOb 31
|
Solucion:
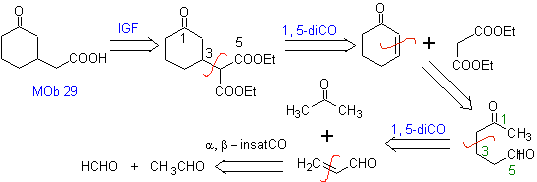
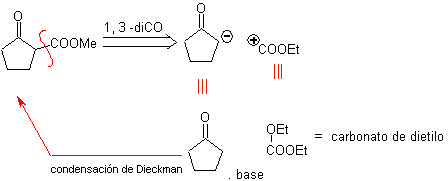
MOb 29. Análisis retrosintético:
El carbanión necesario para adicionarse al compuesto a,b-
insaturado CO puede obtenerse a partir
del malonato de dietilo en medio básico. Que posteriormente obligará a una
descarboxilación, para llegar a
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 31216
SINTESIS DE COMPUESTOS AROMÁTICOS
II
(Método del Árbol de
Síntesis)
Si bien uno de los primeros
problemas a resolver en la síntesis de los compuestos aromáticos multi-
sustituidos, es el control de los efectos orientadores y la formación de
isómeros no deseados, es también importante estudiar la reactividad de los
arenos, en tanto que en algún sentido la presencia de grupos alifáticos en el
compuesto aromático, muchas veces, presentan características y reactividades,
propias del tipo de compuesto orgánico al que pertenecen y las particulares
que resultan de la interacción mutua de los grupos alifáticos y aromáticos.
En ese propósito, se basa,
la síntesis de las moléculas Nº 20 al
27, esta vez a partir de materiales
especificados, por lo que la interrogante, se presenta del siguiente modo: ¿Cuáles
son las reacciones que justifican las
siguientes transformaciones?:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
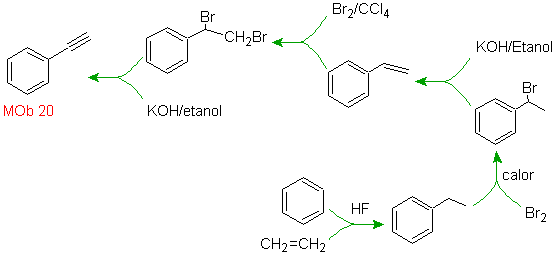
Solución MOb
20.
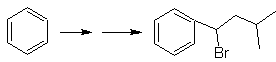
Sabemos que no existe la
posibilidad de que el ión acetiluro actúe directamente sobre el benceno, por
consiguiente el triple enlace se obtiene
a partir de un grupo alquílico
vec-dibromado, que se obtiene por bromación del estireno, obtenido
previamente por una deshidrobromacion de
un haluro de bencilo formado por una bromación por el mecanismo de radicales
libres sobre el etilbenceno
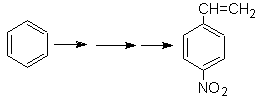
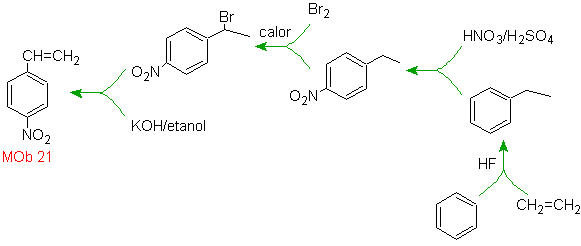
Solución MOb
21.
El para nitroestireno, no es
posible obtener por nitración directa del estireno, debido a que el grupo
etenilo unido al anillo es inestable en las condiciones de la nitración.
En tal virtud la molécula
precursora tendrá un grupo que sea fácil de deshidrobromar. Este precursor se
obtiene por Bromación de radicales del grupo etilo ligado al anillo bencénico,
que previamente fue nitrado mayoritariamente en la posición para.
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 68228
En el diseño de síntesis de una molécula con varios grupos funcionales, es muy común que un reactivo que produce una transformación sobre un grupo funcional, afecte también a otro grupo presente en otra parte de la molécula. En los casos en que no se puede lograr una quimioselectividad adecuada sobre el grupo funcional que tiene que transformarse, el grupo que debe permanecer inalterado se protege convirtiéndolo temporalmente en una funcionalidad inerte a las condiciones de la reacción.
La operación de protección, requiere del siguiente procedimiento:
· Proteger el grupo o los grupos funcionales más reactivos selectivamente y en condiciones suaves.
· Efectuar la reacción sobre el grupo funcional requerido sin afectar el grupo protegido
· Desproteger el grupo funcional, sometido a protección
La acción de protección debe satisfacer los siguientes requisitos básicos:
· La reacción debe tener buen rendimiento y ser quimioselectiva
· El nuevo grupo funcional debe ser estable en las condiciones de la reacción del grupo que reaccionará
· La funcionalidad introducida no debe agregar centros quirales a la molécula que puedan generar diasterómeros
· El grupo funcional original debe poder regenerarse con buen rendimiento y sin afectar al resto de la molécula
El uso de protectores debe reducirse al mínimo indispensable y su elección debe ser tal que no se requiera reemplazarlos a lo largo de la síntesis ya que los pasos de introducción y remoción (desprotección) suman costo y trabajo a la síntesis y disminuyen el rendimiento. Ejemplo.
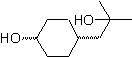
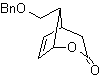
Se ha protegido el grupo cetónico de la molécula transformándolo en un cetal cíclico, con un etanodiol en medio ligeramente ácido, posteriormente se ha hecho reaccionar esta molécula con dos moles del bromuro de fenil magnesio, que actúa sobre el grupo éster, para transformarlo en un alcohol terciario, con dos sustituyentes metilo aportados por el Grignard. Finalmente se hidroliza el cetal cíclico para regenerar la cetona.
No existe en la práctica un grupo protector perfecto para cada funcionalidad, en cambio se puede afirmar de que existe una gran batería de protectores posibles, cada uno de los cuales cumple las condiciones anteriores en determinadas circunstancias. Una lista breve, de protección de los grupos más comunes, se recoge en los siguientes apartados:
Leer más: Protección de Grupos Funcionales en Síntesis Orgánica
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 34053
SÍNTESIS
DE ALCOHOLES
(Método del
Árbol de Síntesis)
Proponer un plan de síntesis, para
las moléculas objetivo señaladas a partir de moléculas simples que se indican
(MOb 30 -41). Para ello, utilice los reactivos y condiciones de reacción que
crea necesarios:
Solución
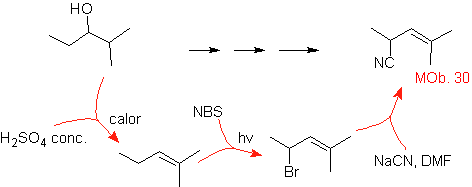
MOb 30.
Estrategia:
Se observa que la molécula de partida ha sido deshidratada y en la posición
alílica inicialmente no sustituida, se ha desplazado un hidrógeno por el grupo
ciano o nitrilo. Esta última reacción puede ocurrir sólo si la molécula
precursora es un haluro alílico, razón por la cual se propone a la misma como
precursora de
El Br se introduce en la posición
deseada con el NBS y el alqueno es producto de la deshidratación de la molécula
de partida.
Solución
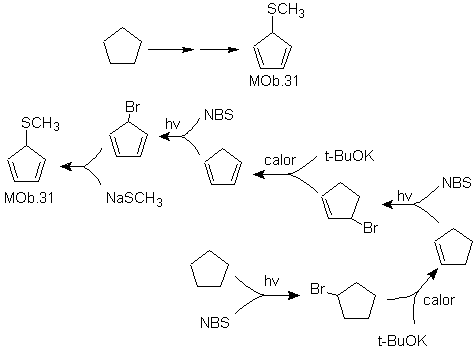
MOb 31.
Estrategia:
Se trata de un tío éter, la molécula precursora necesaria será un haluro del
1,3-ciclopentadieno.
Este haluro se prepara por la acción del NBS, sobre
el cicloalqueno dienico, el cual a su vez es preparado por la deshidrobromación
de la molécula precursora, al que se llega por la acción del NBS sobre el
cicloalqueno formado previamente por
deshidrohalogenación de la molécula de partida bromada por radicales
Solución
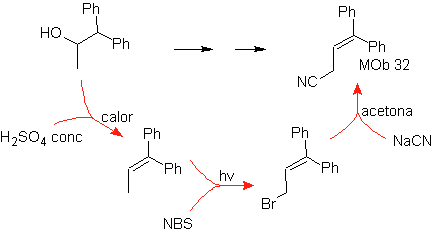
MOb 32.
Estrategia:
Es similar a la utilizada en la obtención de
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 30507
El control en síntesis orgánica, es una de las labores más importantes, para conseguir la transformación requerida o planificada y/o de evitar la formación de aquellos subproductos que perjudican sustancialmente el desarrollo óptimo de la síntesis orgánica encarada. Asimismo desde una perspectiva más general, el control también puede comprender o abarcar a los aspectos de simetría y selectividad.
Entonces, por control se deberá entender a una serie de operaciones sintéticas, que permiten al químico, formar el esqueleto carbonado con la funcionalidad pretendida o de “colocar” un grupo o átomo en el lugar o posición requeridos.
Consiguientemente, estas operaciones podrán ser de una variada gama de rutinas con una intencionalidad reflexionada por el químico y que demandan de éste, ciertas habilidades cognitivas y destrezas similares a las artísticas, para la construcción (síntesis) de las moléculas orgánicas.
En tal virtud, en las reacciones de condensación, como en otras, las operaciones de control, pueden estar comprendidas, en alguna de las siguientes categorías.
![]() Reacciones competitivas (autocondensación y/o condensación cruzada)
Reacciones competitivas (autocondensación y/o condensación cruzada)
![]() Activación – desactivación
Activación – desactivación
![]() Selectividad y especificidad
Selectividad y especificidad
![]() Protección- desprotección
Protección- desprotección
En las reacciones de condensación de compuestos carbonílicos, es fundamental establecer anticipadamente el orden de los eventos para minimizar o en su caso suprimir las posibilidades de autocondensación y la ocurrencia de condensaciones cruzadas, que lamentablemente son una evidente amenaza en estas reacciones..
Autocondensación
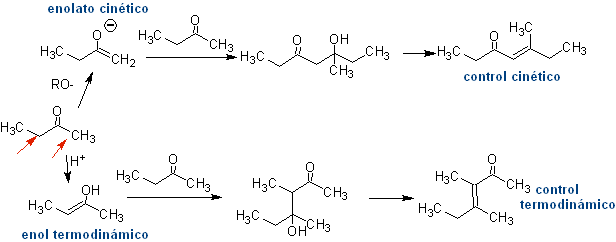
Todo compuesto carbonílico que posee uno o más hidrógenos alfa, en los carbonos adyacentes al grupo carbonilo, corren el riesgo de sufrir una reacción de autocondensación si no se procede con el rigor correspondiente.
Así por ejemplo, si a una 2-butanona, se agrega una base no hidroxilada como el EtONa, se formará un enolato que podría eventualmente combinarse con otra molécula de la misma cetona. De igual modo, si se agrega H+, puede también ocurrir un autocondensación, como puede verse en el siguiente esquema: Esto puede minimizarse agregando con la misma velocidad, desde alimentadores separados, la base o ácido al compuesto que proporcionará el enol o enolato y el compuesto carbonílico que será atacado en el carbono carbonílico. Un balón de tres cuellos y agitación magnética puede servir.
Leer más: Control en las condensaciones de compuestos carbonílicos
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 26618
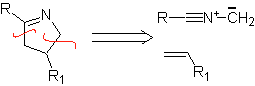
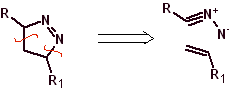
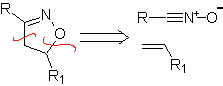
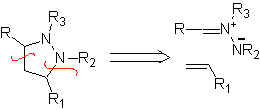
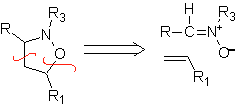
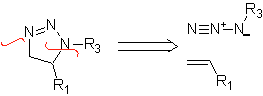
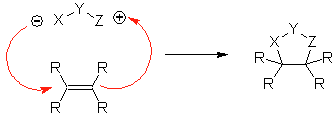
Estas reacciones normalmente forman anillos heterocíclicos de cinco eslabones, para lo cual es necesario la reacción entre un compueston1,3 dipolar y un alqueno. La reacción es una cicloadición [3-2]. Los compuestos 1,3-dipolares que más uso han tenido para formar heterociclos pentagonales son:
 |
 |
 |
 |
 |
 |
| MOb: 86
|
. |
MOb: 87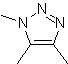 |
.. |
MOb: 88 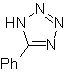 |
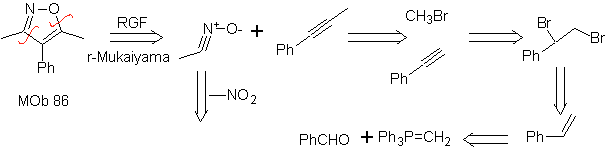
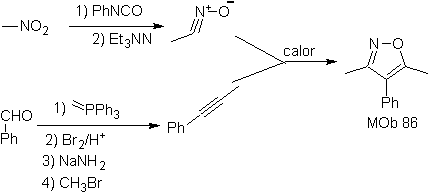
Leer más: Síntesis de heterociclos por ciclación intermolecular
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 27695
Desconexión de compuestos 1,2-dioxigenados
1.- Compuestos a-hidroxicarbonílicos
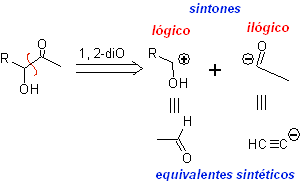
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 27378
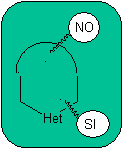
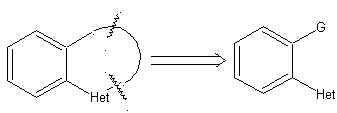
SÍNTESIS DE HETEROCICLOS POR CICLACIÓN INTRAMOLECULAR
La construcción de sistemas heterocíclicos también utiliza estas mismas
reacciones, con la particularidad de que en el sistema heterocíclico debe estar
presente o contener al menos un átomo diferente al carbono. Los más comunes son
el nitrógeno, oxigeno, azufre y fósforo.
El sistema cíclico de la molécula que se desea sintetizar, puede
provenir de la modificación de un sistema cíclico presente en alguno de los
reactivos implicados en la síntesis o ser el resultado de la ciclación de
antecedentes no cíclicos y que ha sido construido en el desarrollo de la
síntesis por ciclación intramolecular o por métodos basados en ciclaciones
intermoleculares (cicloadiciones).
1. Ciclación intramolecular
Las reglas generales de desconexión de heterociclos provenientes de una
ciclación intramolecular, fueron adecuadamente sistematizadas por J. I. Borrell[1],
las mismas que se asumen en la presente sección (Het = N, O, S)
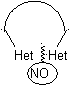
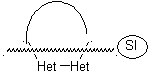
1.
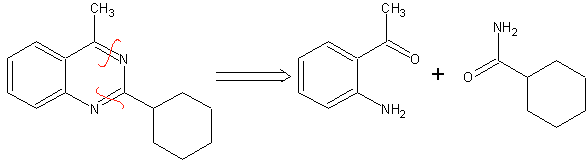
En la síntesis de un compuesto monociclico, el cierre del
anillo supone generalmente la formación de un enlace carbono- heteroátomo.
|
Modelo:
|
|
|
Ejemplo: |
|
|
|
|
|
|
Ejemplo:
|
|
|
Modelo:
|
|
|
Ejemplo:
|
|
[1] BORRELL J.I. “Introducción
al Análisis Retrosintético”. Cap. 8.Laboratori de Sintesi. Grup
d’Enginyería Molecular (GEM). Institut Químic de Sarriá, Universitat Ramon
Llull. España. (Diapositivas de apoyo para Clases)
Leer más: Síntesis de heterociclos por ciclación intramolecular
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 28721
DESCONEXIÓN DE COMPUESTOS 1,4-DIOXIGENADOS
Otro grupo de compuestos de mucha importancia en la síntesis química, lo constituyen las moléculas dioxigenadas que se hallan en una relación de distancia 1,4. Estos compuestos cuando se someten a un análisis de desconexión retrosintético, generan sintones, en donde uno de ellos, el electrófilo o nucleófilo, puede ser considerado “anómalo” o “ilógico”, en razón a que la carga asignada a uno de los átomos no puede explicarse en términos de la electronegatividad intrínseca o inducida del mismo.
1. Compuestos 1,4-dioxigenados (1,4-diO)
En este tipo de compuestos, la desconexión conduce también a un sintón lógico y a otro sintón ilógico (no natural), que puede ser un nucleófilo o un electrófilo, cuyo equivalente sintético, tiene que ser todavía reelaborado adecuadamente, para poder ser utilizado en la reacción química.
1. 1. Compuestos 1,4-dicarbonílicos
1.1.1. Compuestos 1,4- dicetónicos
Las alternativas de desconexión de este tipo de compuestos o moléculas a ser sintetizadas (MOb), pueden conducir a las siguientes opciones:
a. Un sintón aniónico lógico y un sintón catiónico ilógico
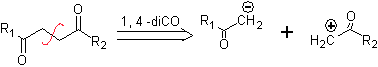
El equivalente sintético del anión es el ión enolato o el mismo enol del compuesto carbonílico. En cambio el equivalente sintético para el carbocatión es el alfa halocarbonilo. (Umpoloung)
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 23324
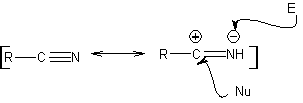
MOb: 75 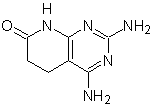 |
MOb: 76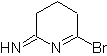 |
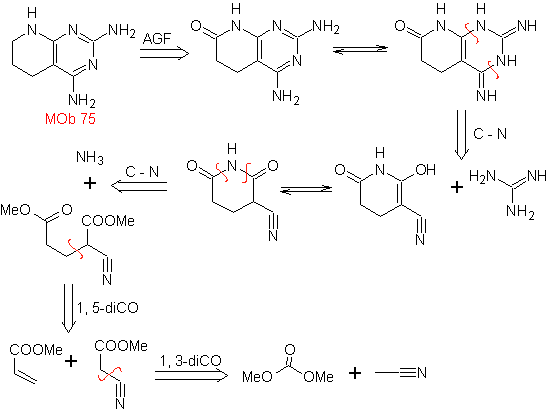
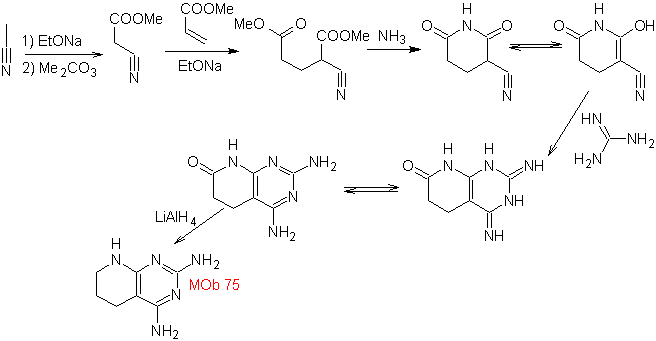
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 22935
DESCONEXIÓN DE COMPUESTOS 1,6-DIOXIGENADOS
Los compuestos 1,6 difuncionalizados, preferentemente utilizan la estrategia de la reconexión para su respectiva síntesis; esta estrategia, puede muy bien combinarse con la reacción de Diels-Alder, que en general forma como producto, aductos olefínicos de seis eslabones o la reducción de Birch de anillos bencénicos, que igualmente genera productos olefínicos de seis eslabones
1. Compuestos 1,6 dioxigenados
La reacción que genera compuestos dicarbonílicos, de diferente combinación posible: dicetonas, cetoácidos, cetoaldehidos, diácidos, etc y a diferentes distancia la una de la otra, sin duda, es la reacción de ozonólisis de compuestos olefínicos.
Dependiendo de la estructura del sustrato y las condiciones de la reacción sobre el ozónido intermedio formado, se conseguirán una diversidad enorme de compuestos como resultado de la ruptura del doble enlace olefínico. De ellos, son de especial interés aquellos que se hallan en una relación 1, 6 – dioxigenada, como puede colegirse de la siguiente operación sintética de “reconexión”:
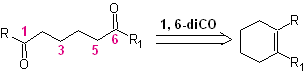
La mejor manera de comprender el funcionamiento de esta “operación sintética de reconexión”, se lo conseguirá a través de la solución de la síntesis de las siguientes moléculas orgánicas:
|
MOb 50
|
|
MOb 51
|
|
MOb 52
|
|
|
|
|
|
|
|
MOb 53
|
|
MOb 54
|
|
MOb 55
|
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 28620
Síntesis de heterociclos con varios heteroátomos
Los compuestos heterocíclicos como ya se tiene dicho
poseen una amplia gama de aplicaciones: predominan entre los compuestos usados
como farmacéuticos, agroquímicos y de uso veterinario; se utilizan como aditivos
abrillantadores, antioxidantes, inhibidores de la corrosión, como colorantes y
pigmentos; y en muchas aplicaciones más.
Por lo tanto es razonable, que actualmente gran parte
de las investigaciones en química traten de la síntesis y propiedades de los
compuestos heterocíclicos. A ese fin se orienta este artículo que pretende
proporcionar a los estudiantes de química herramientas básicas de la
retrosíntesis.
El proceso de desconexión para moléculas con varios
heteroátomos, puede realizarse para cada enlace carbono-heteroátomos, de
acuerdo a los modelos anteriormente estudiados o simultáneamente, para lo cual
se utilizan reactivos poliheteroatómicos asequibles.
1. Heteroátomos a distancia (1, 2)
Los reactivos más representativos y usuales son, las hidrazinas
e hidrazinas sustituidas, así como la hidroxilaminas.
|
Hidracina |
Hidroxilamina |
Proponer un diseño de síntesis, a partir de materiales simples, para las
siguientes moléculas:
|
|
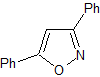
MOb 77
pirazoles |
|
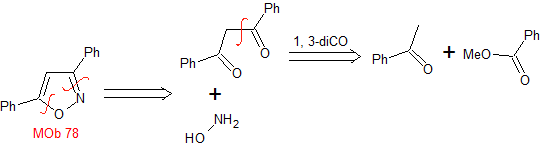
MOb 78
isoxazoles |
|
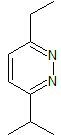
MOb 79
piridacinas |
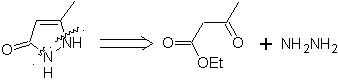
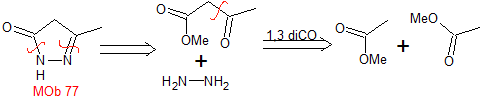
MOb 77. Análisis retrosintético. La MOb es un
derivado del pirazol y se desconecta directamente por los enlaces C-N, para
generar precursores simples como la hidracina y un compuesto 1,3-diCO.
|
|
|
Síntesis. El acetato de metilo, es un buen precursor para
formar el compuesto 1,3-diCO, el cual se combina con la hidrazina para
generar la MOb 77. |
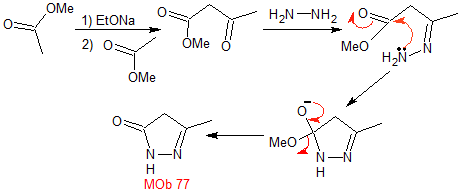
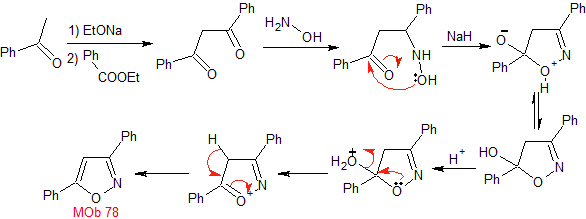
MOb 78- Análisis retrosintético.
|
|
Síntesis. La bezofenona y
el benzoato de etilo permiten formar el 1,3-diCO requerido, para reaccionar en
medio ligeramente ácido con la hidroxilamina y luego de agregar el NaH, se da
la ciclación, que requiere de mayor ácido para
deshidratar y producir finalmente
|
|
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 26610
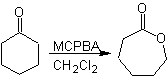
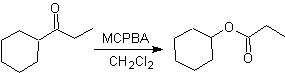
Oxidación de Baeyer–Villiger
Otra reacción que puede asociarse a la estrategia de la retrosíntesis, es la oxidación de cetonas por
peroxiácidos, mas conocida como reacción de Baeyer-Villiger. En cetonas
cíclicas, la oxidación con perácidos, genera lactonas. Los grupos unidos a las
cetonas asimétricas, poseen una aptitud migratoria, que permite, en términos
literales, “ insertar un átomo de oxigeno” entre el grupo carbonilo y el grupo
migrante, produciéndose así, un éster o una lactona.
Se debe tomar en cuenta, que las enonas (cetonas α, β
insaturadas) no son buenos sustratos para la oxidación de Baeyer-Villiger, en
razón a que el alqueno es mucho mas reactivo que la cetona. Sin embargo hay estructuras especiales donde el alqueno
puede ser protegido por un sustituyente cercano por el efecto estérico y
orientarse de este modo el ataque del peracido hacia el grupo carbonilo.
|
|
… |
|
Recuérdese que la aptitud migratoria de los diferentes
grupos, en la reacción de Baeyer-Villiger, es como sigue:
H > Ph
> alquilo 3º > cicloalquilo
> alquilo 2º > alquilo 1º > Me
Proponer un plan de síntesis para las siguientes moléculas:
|
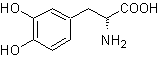
MOb 56
L-Dopa |
. |
MOb 57
|
. |
MOb 58
|
|
|
|
|
|
|
|
MOb 59
|
|
MOb 60
|
|
MOb 61
|
MOb 56. Análisis retrosintético.
El alfa aminoácido, de
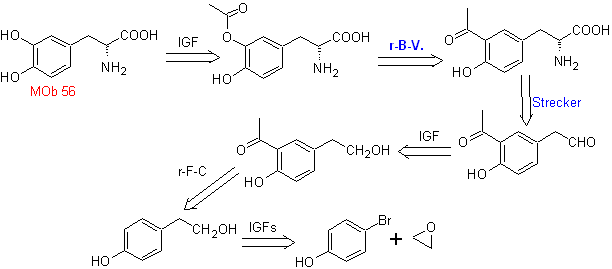
Síntesis.
Para la formación del Grignard
requerido, se protege el OH orto del benceno. La síntesis de Strecker, permite
formar el alfa aminoácido, que es oxidado de acuerdo a Baeyer-Villiger con un
perácido y el producto se somete a una hidrólisis ácida del grupo éster, lo que
conduce a la formación de
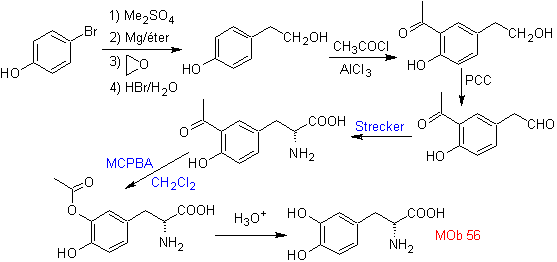
Leer más: La oxidación de Baeyer-Villiger como estrategia en la Retrosíntesis
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 25997
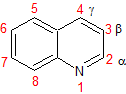
Síntesis de Quinoleínas
(Método de las
desconexiones)
|
|
Las quinoleínas
compuestos formados por núcleos derivados del benceno y piridina se
encuentran en numerosos alcaloides, en cierto tipo de colorantes y en un
considerable número de fármacos, por lo que son de gran interés comercial en
los laboratorios industriales. |
Aquí se mencionarán sólo aquellos métodos de
síntesis, que producen rendimientos aceptables en sus reacciones:
1.
Síntesis de
COMBES
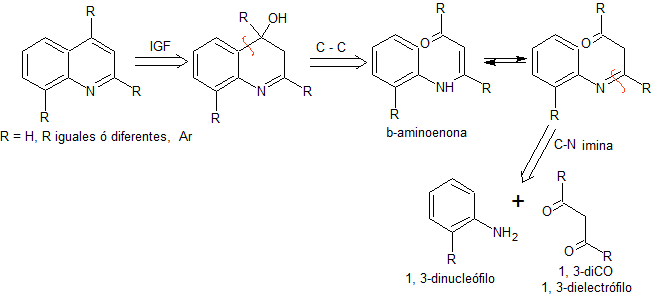
En este método, inicialmente se realiza la condensación
de un compuesto 1,3-diCO con una anilina o su derivado, para formar una
β-aminoenona, que posteriormente se cicla en medio ácido concentrado al
correspondiente derivado quinolénico. En
términos retrosintéticos, la síntesis de COMBES, se expresaría del siguiente
modo:
|
|
|
Proponer un plan de síntesis para
|
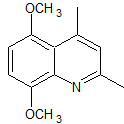
MOb 95:
|
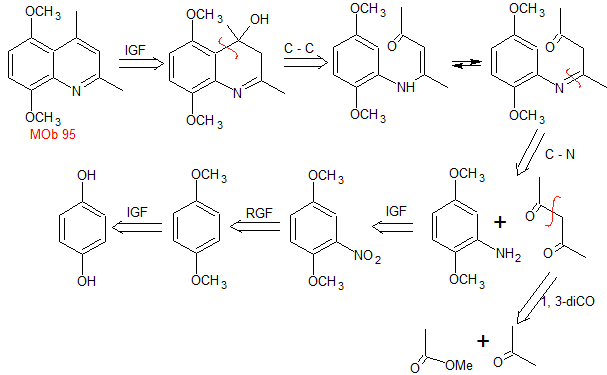
MOb. 95. Análisis retrosintético: Inicialmente se
funcionaliza la MOb, para proceder a desconectarlo, según Combes y generar de
este modo equivalentes sintéticos que conduzcan a moléculas precursoras
1,3-dinucleófilo y 1,3-dielectrófilo.
|
|
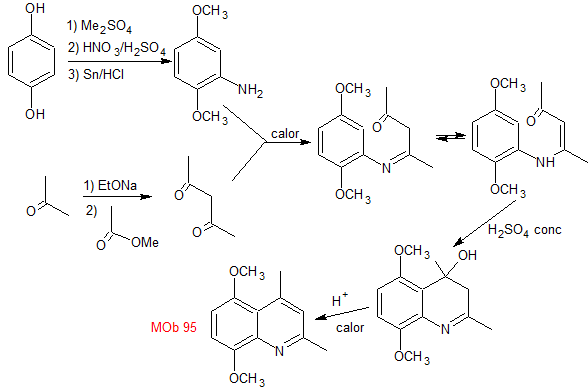
Síntesis: La hidroquinona
permite formar la 2,5-dimetoxianilina como 1.3 dinucleófilo. La condensación de la acetona y acetato de metilo, conducen a la
2,4-pentanodiona, que funciona muy bien como un 1,3-dielectrófilo. Combinadas
ambas moléculas precursoras, utilizando ácido sulfúrico concentrado para
promover la ciclación y por un calentamiento posterior se llega a formar
|
|
|
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 31277
La transposición de
Beckmann como estrategia en
La transposición de oximas en medio acido, denominada
transposición de Beckman, produce una amida o lactama si la cetona de partida
es lineal o cíclica respectivamente.
Para mejorar el rendimiento de este tipo de reacciones se han
estudiado varios catalizadores y medios ácidos. Así por ejemplo, nuevos medios
ácidos utilizados como catalizadores, con el propósito indicado, lo
constituyen, el TCT/DMF, DAST/CH2CL2 , CF3SO3H,
PCl5, HgCl2/MeCN y
el ZnO.
|
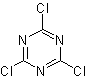
TCT:
Triclorotriazina |
…… |
DAST:
Trifluoruro de
dietilaminosulfuro |
La aptitud migratoria de los grupos es la misma que en la
reacción de Baeyer – Villiger. Proponer un diseño de síntesis para cada una de
las siguientes moléculas:
|
|
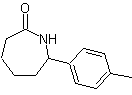
MOb 62
|
|
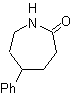
MOb 63
|
|
MOb 64
|
MOb 62. Análisis
retrosintético.
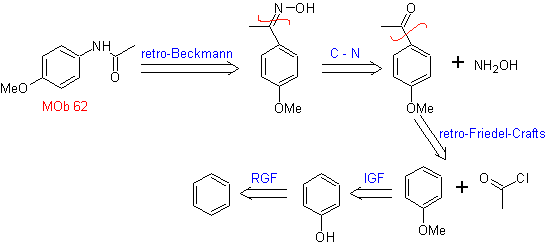
Síntesis. La reacción de la cetona aromática intermedia con NH2OH y su posterior tratamiento con una solución acuosa de ácido sulfúrico y ZnO, permite formar la amida aromática MOb 62.
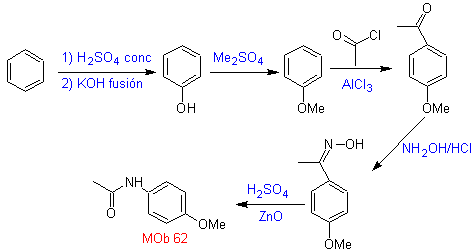
Leer más: La transposición de Beckmann como estrategia en la Retrosíntesis
- Detalles
- Wilbertrivera
- SÍNTESIS ORGÁNICA
- Visto: 21640
Síntesis
de Isoquinoleinas
(Por
el método de las desconexiones)
|
|
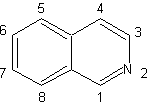
Las
isoquinoleinas difieren estructuralmente de las quinoleinas en la
posición del nitrógeno, ya que esta
última, no se encuentra fusionada, por lo que presenta una “reactividad
alifática”.
No se encuentra libre en la
naturaleza, pero el ciclo de la isoquinoleina se encuentra en algunos
alcaloides, en forma aromática o reducida, por ejemplo, la papaverina. |
Los métodos sintéticos más conocidos para la preparación de isoquinoleinas
se inician con 2-feniletilaminas y comprenden una ciclación por intermedio de
un carbono adicional proporcionado por el grupo carbonilo de otro compuesto.
Los principales métodos sintéticos son: La síntesis de Pomeranz-Fritsch, la
síntesis de Bischler-Napieralski, síntesis de Pictet-Gams y la síntesis de
Pictet-Spengler.
1. Síntesis
de POMERANZ-FRITSCH.
Este método de
síntesis de la isoquinoleina, se produce en dos etapas:
a.
En primer lugar, se condensa el benzaldehído
(1,3-electrófilo-nucleófilo) con el dietilacetal del aminoacetaldehido
(1,3-nucleófilo-electrófilo) para formar una aldimina estable.
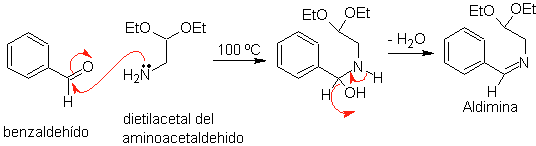
b.
Seguidamente, la aldimina cicla en un medio ácido fuerte,
a una imina, con eliminación simultánea de etanol, para producir una
isoquinoleina.
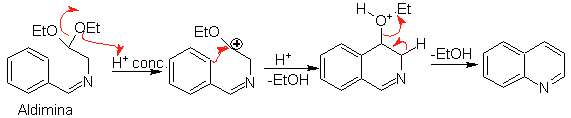
Esta segunda etapa, al ser una sustitución electrofílica, está sujeta al
efecto que tienen en dicha reacción los sustituyentes aceptores o donadores de
electrones sobre el anillo bencénico. Sin embargo, debido a la hidrólisis de la
imina formada, en el medio ácido fuerte utilizado en la reacción, reduce el
rendimiento del proceso.
Este método, permite acceder a isoquinoleinas sustituidas en el C-1, para
lo cual se han probado cetonas aromáticas, con rendimientos muy bajos. No
obstante, se ha tenido mayor éxito al utilizar la variante de las bencilaminas
adecuadamente sustituidas como 1,4-dinucleófilos y el dietilacetal del glioxal
como 1,2-dielectrólfilos
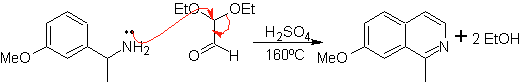
Algo que debe quedar en claro, es que el método de Pomeranz-Fritsch y su
variante, anteriormente analizada, no permiten preparar isoquinoleinas
sustituidas en el C-3 y el C-4 del heteroátomo. El análisis retrosintético de
este método, muestra los posibles intermediarios implicados en la reacción y
los materiales probables de partida.
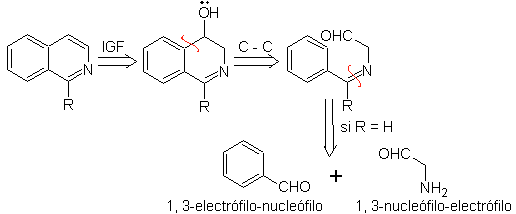
|
Proponer un
diseño de síntesis, para cada una de las siguientes isoquinoleinas:
|
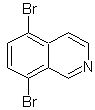
MOb
107
|
|
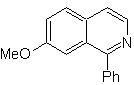
MOb 108
|