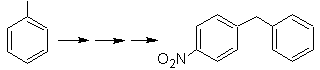SINTESIS DE COMPUESTOS AROMÁTICOS
II
(Método del Árbol de
Síntesis)
Si bien uno de los primeros
problemas a resolver en la síntesis de los compuestos aromáticos multi-
sustituidos, es el control de los efectos orientadores y la formación de
isómeros no deseados, es también importante estudiar la reactividad de los
arenos, en tanto que en algún sentido la presencia de grupos alifáticos en el
compuesto aromático, muchas veces, presentan características y reactividades,
propias del tipo de compuesto orgánico al que pertenecen y las particulares
que resultan de la interacción mutua de los grupos alifáticos y aromáticos.
En ese propósito, se basa,
la síntesis de las moléculas Nº 20 al
27, esta vez a partir de materiales
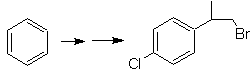
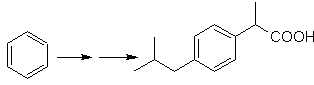
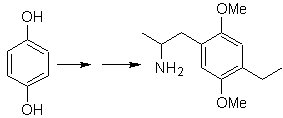
especificados, por lo que la interrogante, se presenta del siguiente modo: ¿Cuáles
son las reacciones que justifican las
siguientes transformaciones?:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
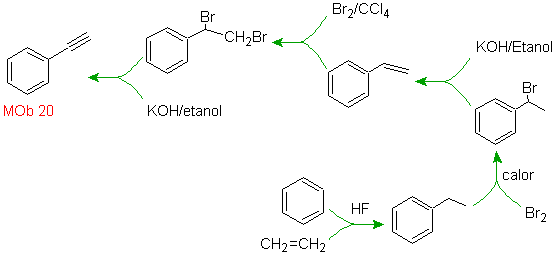
Solución MOb
20.
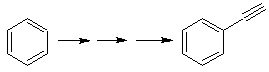
Sabemos que no existe la
posibilidad de que el ión acetiluro actúe directamente sobre el benceno, por
consiguiente el triple enlace se obtiene
a partir de un grupo alquílico
vec-dibromado, que se obtiene por bromación del estireno, obtenido
previamente por una deshidrobromacion de
un haluro de bencilo formado por una bromación por el mecanismo de radicales
libres sobre el etilbenceno
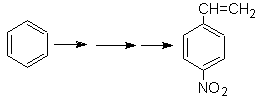
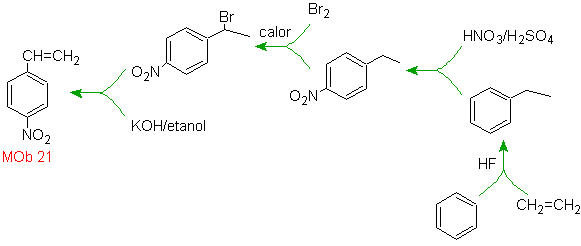
Solución MOb
21.
El para nitroestireno, no es
posible obtener por nitración directa del estireno, debido a que el grupo
etenilo unido al anillo es inestable en las condiciones de la nitración.
En tal virtud la molécula
precursora tendrá un grupo que sea fácil de deshidrobromar. Este precursor se
obtiene por Bromación de radicales del grupo etilo ligado al anillo bencénico,
que previamente fue nitrado mayoritariamente en la posición para.
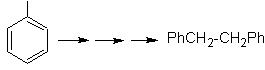
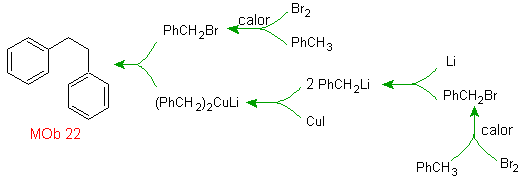
Solución MOb 22.
La simetría de la molécula
permite pensar en una estrategia que tome en cuenta la reacción de Corey-House.
También es una buena ruta si se utiliza el
PhCH2CH2Cl, sobre el benceno o se toma en cuenta una acilación con
PhCH2COCl y posterior reducción del grupo carbonilo por la reducción de
Clemmensen.
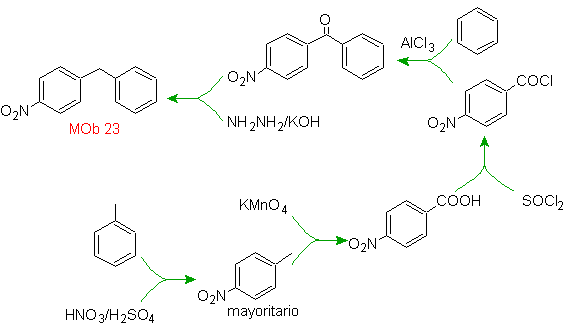
Solución MOb 23.
La molécula precursora puede ser
una cetona, cuyo grupo carbonilo es reducido a metileno por el reductor de
Wolf-Kischner. De este modo se evita la presencia del Zn en medio ‘acido que
afectaría al grupo nitro. Otra molécula precursora puede ser, el haluro
siguiente: O2N-PhCH2Cl que actúe sobre una molécula de
benceno.
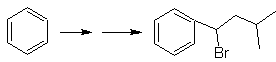
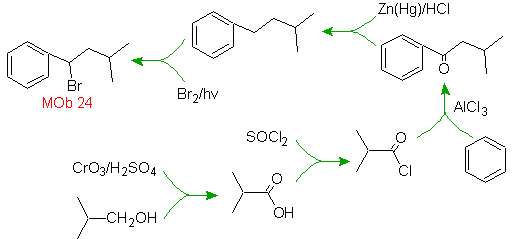
Solución MOb 24.
La posición del bromo en la
molécula precursora, es la típica posición alílica, la que se obtiene por bromación
de radicales del esqueleto carbonado correspondiente.
El grupo alquilico, sobre el anillo
bencénico no se puede obtener del haluro
correspondiente, por que se presentaría transposición. Entonces se recurre a la
acilación y posterior reducción del grupo carbonilo, con amalgama de cinc en
medio acido (reducción de Clemmensen
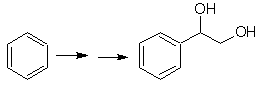
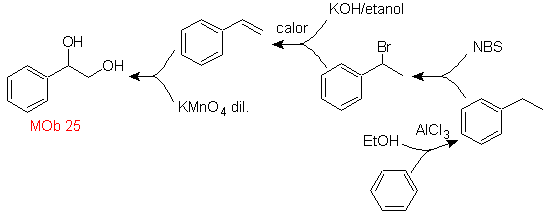
Solución MOb 25.
El diol de esta molécula puede obtener por un
hidroxilación selectiva del estireno, como
molécula precursora. El estireno se forma a partir de la deshidrobromacion,
como en anteriores casos.
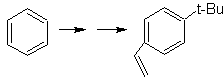
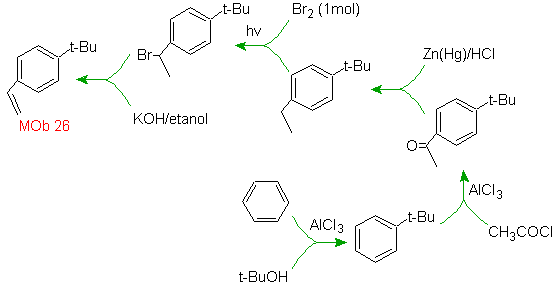
Solución MOb 26.
La molécula precursora, señala que una posible ruta
toma en cuenta la formación del grupo etenilo a partir de un halogenuro y se
aprovecha el grupo voluminoso del t-Butil, para introducir en la posición para,
el grupo acilo portador del grupo etilo.
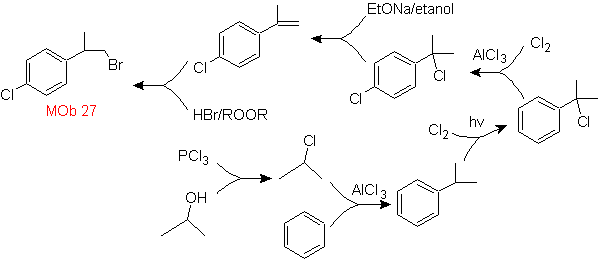
Solución MOb 27.
La estrategia pasa
por definir la inclusión del bromuro en una molécula precursora que no permita
la formación de ningún isómero. El alqueno menos sustituido es el que
obligatoriamente se forma por una deshidrohalogenacion, de un grupo formado por
Halogenación de radicales.
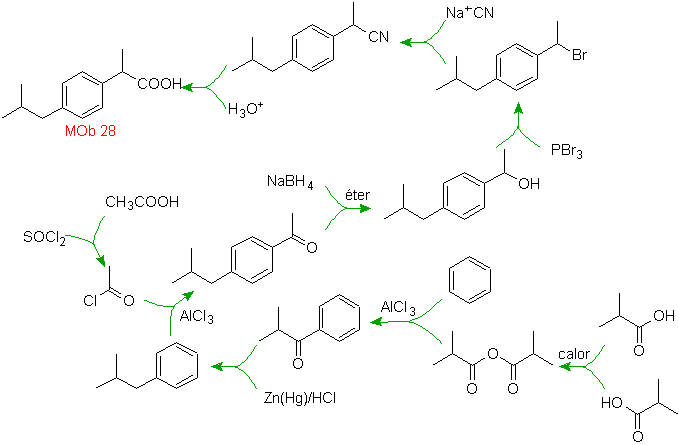
Solución MOb
28.
La ubicación
del grupo carboxílico, permite proponer la formación del mismo a partir de la
hidrólisis del grupo –CN, este último se introduce en las moléculas alifáticas
generalmente por sustitución de un haluro, que a su vez proviene de un alcohol.
Formado por reducción de un carbonilo cetónico.
Los
posteriores pasos están vinculados a acilación de Friedel-Crafts, combinado con
la reducción del C=O por el método de Clemmensen.
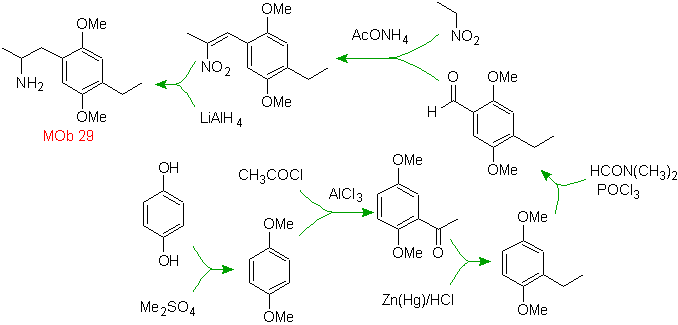
Solución MOb
29.
La presencia
del grupo amino en el resto alquílico del areno, nos hace pensar en el grupo
nitro como precursor de la misma y por la distancia del anillo bencénico, se
pude proponer que el mismo se forma a partir del nitro - alfa-beta insaturado,
resultado de la condensación del tipo aldólico en medio básico con un grupo
–CHO unido al anillo bencénico. Este grupo formilo se introduce en el
anillo por con una formamida
disustituida y oxicloruro de fósforo, conocida como reacción de
Vilsmeier-Haack. Método que sólo puede aplicarse a sustratos aromáticos activados.
Para introducir el grupo etilo por Acilación de Friedel – Crafts, es necesario
previamente transformar en éter metílico los grupos –OH del material de
partida.