Hola badman,
la sintesís exhibida en el archivo "020413.pdf", hacés reaccionar un compuesto organometálico con otro que tiene un grupo alcohol además del grupo halógeno, recordá que los organometálicos que reaccionan con compuestos que tienen fuentes de protones se descomponen, por lo que el rendimiento no será óptimo. En ese caso deberías proteger ese alcohol oxidándolo a cetona, hacer una hidrólisis ácida con etilenglicol, ahí agregas el etillitio, desproteges el acetónido para obtener la cetona. Una vez hecho eso, reducís la cetona a alcohol, y el resto sigue la misma metodología que aplicaste.
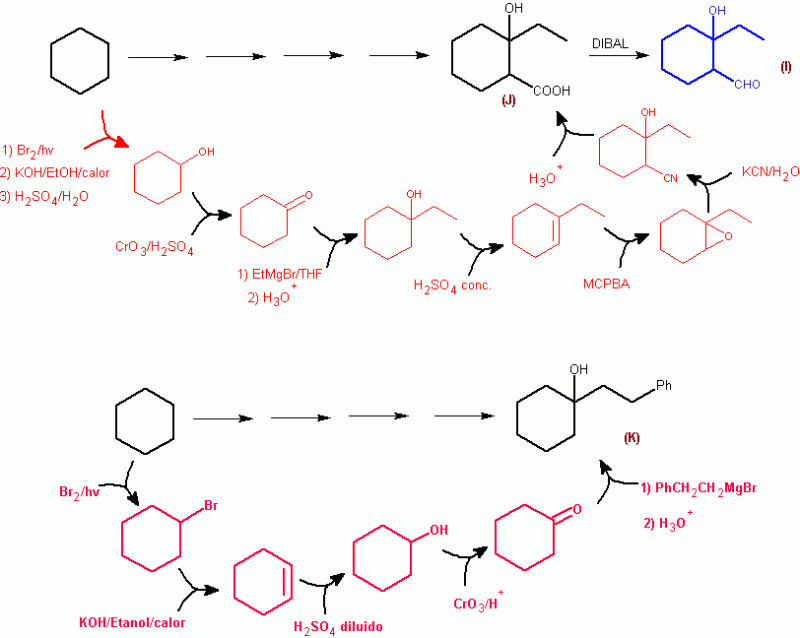
En la síntesis (G), no está mal, una vez que llegaste a la bromohidrina y oxidaste el alcohol a cetona, sólo bastaría con agregar exceso de reactivo de Grignard. (En una E2 no es necesario usar terbutóxido de potasio, se usa especialmente para obtener una alta proporción de alquenos pocos sustituídos, y si hacés una SN2 con KOH el solvente conveniente sería éter o THF,, si el solvente fuese agua la reacción de sustitución será muy lenta)
Otro detalle, el hidruro de diisobutilaluminio (HDIBAL) se usa frecuentemente en ésteres y nitrilos, pero dudo mucho que se use con ácidos carboxílicos (no lo intentaría). Así que en el compuesto con nitrilo y alcohol, primero se usaría el HDIBAL y luego se utiliza el ácido diluído.