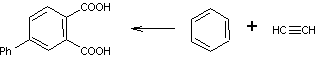Alaynia:
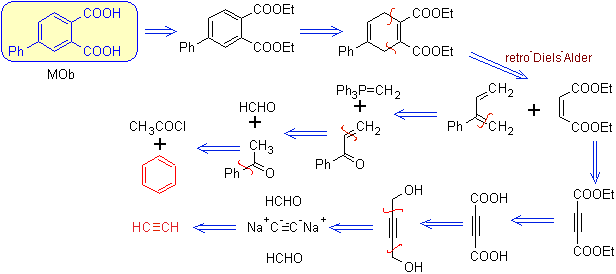
Vuelvo a pasarte un esquema nuevo de retrosíntesis y síntesis, para que tus dudas puedan ser despejadas y te adjunto la reacción de Diels-Alder, cuyos productos se denominan
aductos y tienen una estructura particular por la cual en las retrosínteis hay que buscar el aducto adecuado.
Me explico, la formación del anillo bencénico se la efectúa con mucha facilidad por reacciones de deshidrogenación preferentemente a partir de un cicloalqueno con uno o dos insaturaciones (dobles enlaces). Estas reacciones se han dado en llamar (incorrectamente) reacciones de aromatizacción.
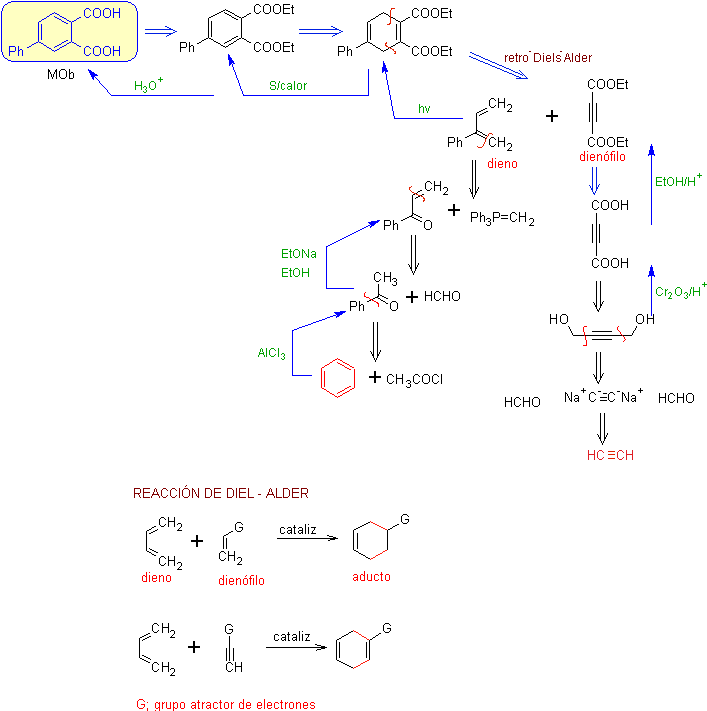
La estructura del cicloalqueno formado en la reacción de Diel - Alder(casi siempre de 6 eslabones), tiene que estar vinculado con las características del aducto.
Por lo menos un doble enlace tiene que aparecer en la posición frontal al enlace (simple o doble) que forman los carbonos que alojan a los grupos atractores de electrones que en este caso son lo ésteres (los grupos carboxílicos no son fácilmente manejables por su acidéz, por lo cual se los tiene como ésteres).
Entonces la \"operación sintética de desaromatización\" no corresponde a una reacción química, sino a una intencionalidad para ubicar el o los dobles enlaces en el ciclohexeno, en las posiciones más adecuadas para una desconexión retro-Diels - Alder. La inversa es una reacción verdadera de \"aromatización\"
Finalmente, al hacer este nuevo esque me percaté de un error en la r-Diel- Alder anterior que ojalá pudieras encontrarlo.
Un saludo:
Wilbert