-
Wilbertrivera
-
 Autor del tema Autor del tema
-
Fuera de línea
-
Moderador
-

-
Mensajes: 1641
-
Gracias recibidas: 384
-
-
|
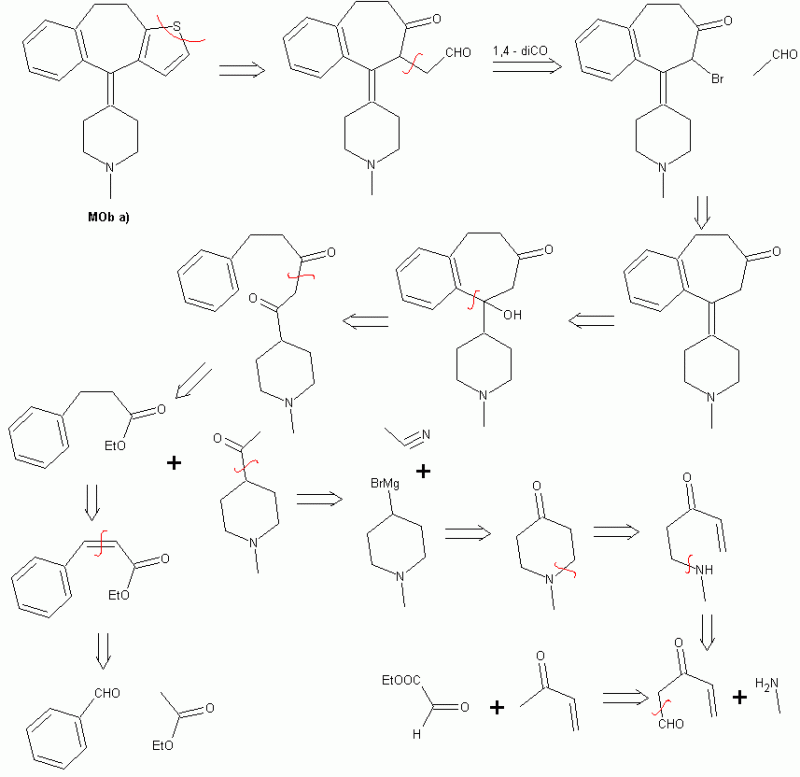
Hola badman.
En el diseño de síntesis que propones para la MOb A, es necesario hacer un pequeño ajuste, es decir el fenol debe ser previamente transformado en un fenóxido, para hacer que éste reaccione con uno de los cloruros de acilo, para formar un éster y luego por acilación intramolecular de Friedel-Crafts, donde se utilizará el ácido de Lewis, formar la lactona.
Había pensado en otra ruta que la subo, para que la analicen:
Saludos. 
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
-
Wilbertrivera
-
 Autor del tema Autor del tema
-
Fuera de línea
-
Moderador
-

-
Mensajes: 1641
-
Gracias recibidas: 384
-
-
|
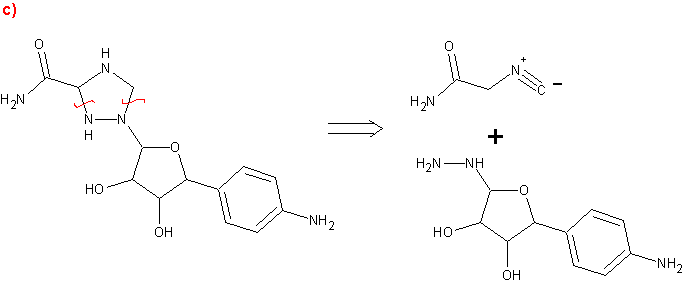
Hola.
La propuesta de badman para la MOb C, presenta un inconveniente en la acilación final, pues esa reacción no garantiza la ubicación requerida del grupo acilo.
Les subo una propuesta, que requiere ser culminada...
SAludos. 
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
-
Wilbertrivera
-
 Autor del tema Autor del tema
-
Fuera de línea
-
Moderador
-

-
Mensajes: 1641
-
Gracias recibidas: 384
-
-
|
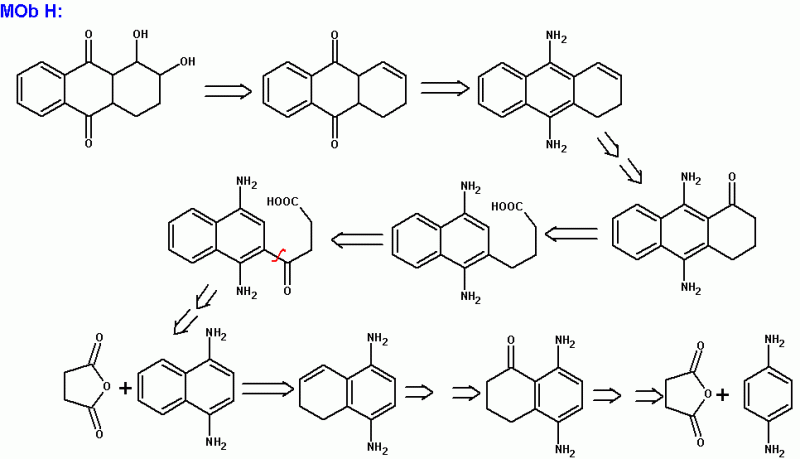
Hola Badman..
La aplicación del MCPBA al sustrato para formar el epóxido, tamb ién afectará a la naftoquinona y se formará una lactona, por lo que hay un serio error en tu propuesta.
Qué les parece la estrategia que les propongo...
Saludos
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
-
Wilbertrivera
-
 Autor del tema Autor del tema
-
Fuera de línea
-
Moderador
-

-
Mensajes: 1641
-
Gracias recibidas: 384
-
-
|
Hola Franz..
La idea en en general está muy bién, sin embargo debes recordar que la cetona es mucho más reactiva que el éster y por lo tanto será la primera en reaccionar con el NH 3 para formar una imina. Luego el reductor LiAlH 4, que reduce los C=O de amidas a metileno, también reducirá el C=O de la cetona a alcohol, entonces, debes de proteger el C=O de la cetona y en el último paso de la síntesis desprotegerla.
Saludos 
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
-
ccv
-

-
Fuera de línea
-
Sancionado
-

-
Mensajes: 349
-
Gracias recibidas: 192
-
-
|
Hola Wilbert, con respecto a la Mob A, no me cuadra la reacción entre metil-vinil-cetona y p-cloro bezaldehído, según yo sobra un carbono y no da la molécula q deseas; yo hubiera usado acetilacetato de etilo y etoxidode sodio para atacar el benzaldehído.
Con respecto a la Mob H,la reacción entre 4-amino anilina y anhídrido succínico tendría problemas, ya que la anilina actuaría como nucleófilo antes de sufrir una acilación aromática, sobre todo sabiendo q hay 2 grupos amino libres presentes.
saludos 
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
Tiempo de carga de la página: 0.214 segundos