-
Alaynia
-
 Autor del tema Autor del tema
-
Fuera de línea
-
Navegador Experto
-
-
Mensajes: 122
-
Gracias recibidas: 0
-
-
|
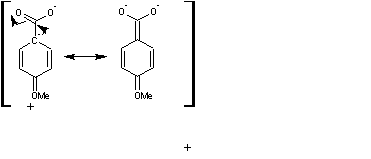
Hola Germán! Gracias por tus explicaciones, pues si que entiendo que el hecho de qué el carbono que sustenta el àcido tenga una carga negativa desestabiliza la molécula.
Lo que sucede (que no acabo de entender aún, perdona) es que he dibujado otra estructura resonante en la molécula de para, que no sé si sería viable. Por eso, como me salen más ECR (se me deslocaliza más) que en meta llego a la conclusión (errónea) que en para es más ácido que en meta. No sé si me explico.
Un saludo!!
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
-
Germán Fernández
-

-
Fuera de línea
-
Administrador
-

-
Mensajes: 2822
-
Gracias recibidas: 751
-
-
|
Perdona Alaynia olvidé esa estructura, que es muy importante. En primer lugar, recordar que una base fuerte (inestable) está asociada a un ácido débil. Cuando el metóxido está en para lleva la carga negativa al carboxilato desestabilizándolo. Es cierto que tienes más estructuras, pero esa última que dibujaste no da estabilidad a la base, todo lo contrario, la desestabiliza al llevar una segunda carga negativa al grupo carboxílico.
En conclusión, la base conjugada del ácido p-metoxibenzoico es más inestable (fuerte) que la del ácido m-metoxibenzoico.
Saludos
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
-
Alaynia
-
 Autor del tema Autor del tema
-
Fuera de línea
-
Navegador Experto
-
-
Mensajes: 122
-
Gracias recibidas: 0
-
-
|
Buenas Germán!!
En primer lugar gracias por tu explicación. Al final creo que ya lo entendí. Como hay separación de cargas desestabiliza más la molécula haciéndola más inestable independientemente del número de ECR.
Muchísimas gracias!!!
|
|
Por favor, Identificarse o Crear cuenta para unirse a la conversación.
|
Tiempo de carga de la página: 0.190 segundos