¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp. .
Más información en www.foroquimico.com
Si prefieres un curso de química orgánica tanto básica como avanzada te invito a acceder al canal: https://www.youtube.com/channel/UC_RiUaA2326jO9XozAA4q2g , en el que encontrarás más de 750 vídeos de teoría y ejercicios.
REACCIONES EN QUÍMICA ORGÁNICA
REACCIONES EN QUÍMICA ORGÁNICA
Las reacciones orgánicas permiten la transformación de unas sustancias en otras y su conocimiento es vital en la síntesis de compuestos orgánicos. En esta sección se recopilan las reacciones orgánicas más importantes, ordenadas alfabéticamente.
- Detalles
- Germán Fernández
- Visto: 8042
Es la reacción entre un haluro insaturado de arilo o vinilo y un alqueno deficiente en electrones, como el acrilonitrilo o el acrilato de metilo. Emplea Paladio(0) como catalizador en presencia de una base que lo regenera.
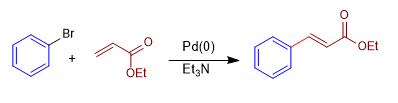
Mecanismo:
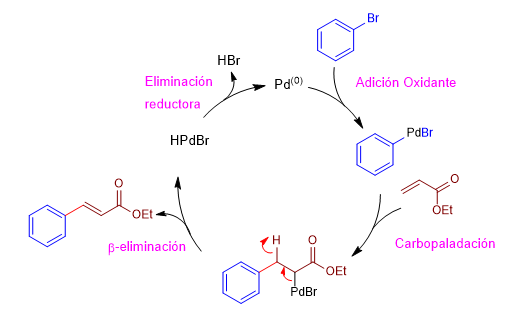
La reacción de Heck transcurre a través de un ciclo catalítico que consta de las siguientes etapas:
Etapa 1. Adición oxidante, es la etapa en la que el paladio se inserta en el enlace carbono-bromo.
Etapa 2. Carbopaladación, ataque del organometálico de paladio al carbono beta del éster a,b-insaturado.
Etapa 3. b-eliminación, formación de un doble enlace por cesión del par del enlace carbono-paladio con perdida de hidruro.
Etapa 4. Eliminación reductora, la presencia de un medio básico permite regenerar el paladio(0).
- Detalles
- Germán Fernández
- Visto: 3965
Se llama aza-Wittig a la reacción entre un aza-iluro y un carbonilo. Los aza-iluros se preparan por reacción entre azidas y trifenilfosfina.
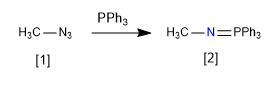
[1] Azida
[2] Aza-iluro
- Detalles
- Germán Fernández
- Visto: 19605
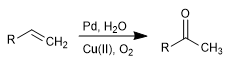
La oxidación de Wacker permite transformar alquenos en las correspondientes cetonas por tratamiento con Pd en presencia de sales de cobre. El cobre tiene la capacidad de oxidar el paladio(0) a paladio(II), siendo este último el ajente catalítico de la reacción.
- Detalles
- Germán Fernández
- Visto: 18050
- Detalles
- Germán Fernández
- Visto: 20562
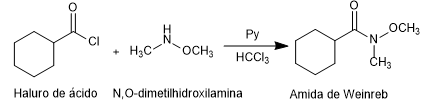
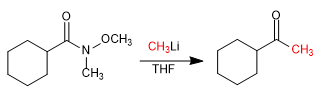
- Detalles
- Germán Fernández
- Visto: 11251
En 1902, Wolff observó que al tratar diazoacetofenona ($\alpha$-diazocetona) con Ag2O/H2O se producía un reagrupamiento que generaba el ácido fenilacético.
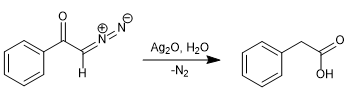
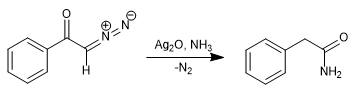
Al reemplazar el agua por amoniaco se obtiene la fenilacetamida.
- Detalles
- Germán Fernández
- Visto: 24659
- Detalles
- Germán Fernández
- Visto: 37001
En 1855, Wurtz trató haluros de alquilo con sodio metal obteniendo el correspondiente alcano simétrico. El acoplamiento de dos carbonos sp3 pertenecientes a haluros de alquilo o arilo por tratamiento con sodio metal se conoce como síntesis de Wurtz. Por otro lado, el acoplamiento de un haluro de alquilo con un haluro de arilo se denomina reacción de Wurtz-Fittig.
- Detalles
- Germán Fernández
- Visto: 14915
- Detalles
- Germán Fernández
- Visto: 10962
La fragmentación de Wharton es una reacción concertada en la que un grupo saliente se sitúa en posición 4 con respecto a un grupo donor de electrones. La cesión de los pares libres del grupo donor produce la fragmentación del enlace vecino y la pérdida del grupo saliente con formación de dobles enlaces. Veamos un ejemplo:
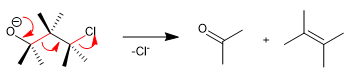
- Detalles
- Germán Fernández
- Visto: 10384
La síntesis de Wharton permite transformar $\alpha,\beta$-epoxicetonas en alcoholes alílicos por tratamiento con hidrazina en medio ácido acético o hidrato de hidrazina seguido de base fuerte. La $\alpha,\beta$-epoxicetona se obtiene a partir de la cetona $\alpha,\beta$-insaturada por oxidación con agua oxigenada en medio básico.
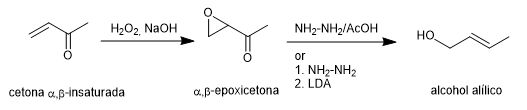
Leer más: Wharton síntesis de olefinas (Transposición de Wharton)
- Detalles
- Germán Fernández
- Visto: 18735
La reacción de Chugaev permite la formación de olefinas a partir de xantantos.
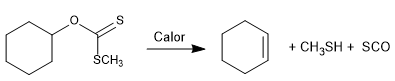
- Detalles
- Germán Fernández
- Visto: 37780
Los aldehídos, sin hidrógenos alfa, dan la reacción de Cannizzaro por tratamiento con una base fuerte (NaOH)
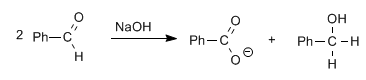
En esta reacción una molécula es reducida a alcohol, mientras que la otra es oxidada a ácido carboxílico.
- Detalles
- Germán Fernández
- Visto: 15949
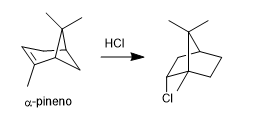
La reacción de Blanc permite la clorometilación de compuestos aromáticos.
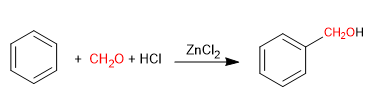
Utiliza como reactivos metanal con cloruro de hidrógeno gaseoso en presencia de un ácido de Lewis. El resultado es la introducción de un grupo hidroximetil en el anillo aromático (benceno) cuyo hidroxilo se reemplaza por cloro en presencia del cloruro de hidrógeno.
- Detalles
- Germán Fernández
- Visto: 23510
La reacción de Beckmann produce el reagrupamiento de una oxima en amida. Esta reacción se realiza en un medio ácido.
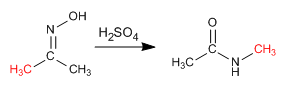
- Detalles
- Germán Fernández
- Visto: 19504
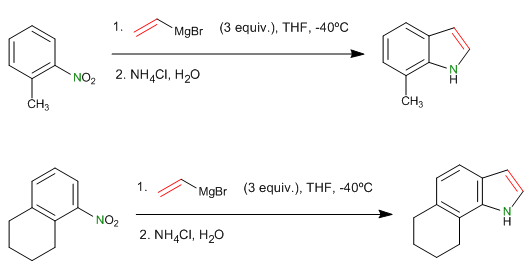
- Detalles
- Germán Fernández
- Visto: 12839
La reacción de Barbier permite obtener reactivos organometálicos inestables en el medio de reacción. Inicialmente se llevó a cabo con Magnesio metal, generando in situ magnesianos. Posteriormente se extendió a otros metales: Sn, Zn.., pudiendo trabajar en medios acuosos, sin precisar la protección de grupos ácidos (hidroxilos)
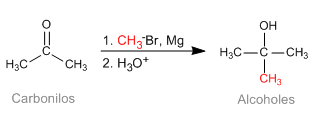
- Detalles
- Germán Fernández
- Visto: 14499
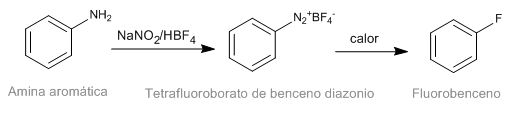
La reacción de Schiemann consiste en la descomposición térmica de tetrafluoroboratos de diazonio aromáticos para rendir el correspondiente derivado fluorado. Aunque las sales de diazonio son intestables los tetrafluoroboratos de diazonio presentan una importante estabilidad y pueden ser preparados con buen rendimiento. El tetrafluoroborato de diazonio se prepara a partir de aminas aromáticas mediante la reacción de diazotación.
- Detalles
- Germán Fernández
- Visto: 11688
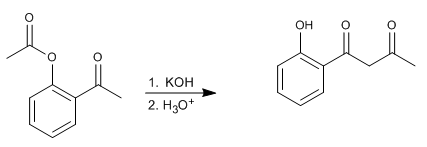
El reagrupamiento de Baker-Venkataraman transforma orto-aciloxicetonas aromáticas en beta-dicetonas por tratamiento básico (catálisis). Las beta-dicetonas poseen un gran interés en la síntesis de cromonas, flavonas y cumarinas. Las bases más utilizadas en la reacción son: KOH, tert-butóxido de potasio, sodio en tolueno, hidruro de potasio.
- Detalles
- Germán Fernández
- Visto: 13338
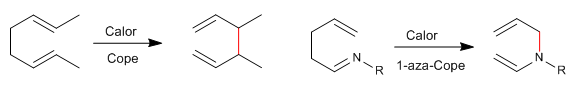
Los 1,5-dienos isomerizan mediante reagrupamientos sigmatrópicos-[3,3] al ser calentados. Reacción conocida como transposición de Cope. El reagrupamiento de 1,5-dienos N-sustituidos recibe el nombre de transposición de aza-Cope. Dependiendo de la posición ocupada por el nitrógeno tenemos: 1-aza-, 2-aza-, 3-aza-Cope. El reagrupamiento 3-aza-Cope coincide con el aza-Claisen.