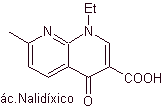
Síntesis de Antibióticos Fluoroquinolonas
Las Quinolonas pertenecen a un grupo de agentes antibacterianos
sintéticos. El agente más antiguo de esta familia, el ácido nalidíxico,
utilizada a principios de los años 60, presenta un buen espectro contra las
enterobacterias (espectro antibacteriano limitado) pero su farmacocinética no
es muy favorable para el uso rutinario en la clínica por su baja
biodisponibilidad en tejidos y su vida media corta.
Por esta razón fue necesario sintetizar nuevos antibacterianos de esta
familia para mejorar el espectro de actividad, el perfil farmacocinético,
disminuir los efectos adversos y la aparición de resistencia bacteriana. Este
nuevo grupo son las llamadas fluoroquinolonas, generadas durante la década de
los 80.
|
|
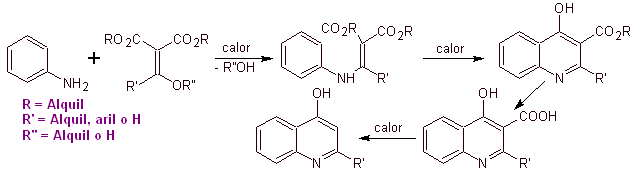
Muchos investigadores
coinciden en que la reacción de
Gould-Jacobs[1],
es la base principal de la síntesis de las primeras quinolonas de uso
farmacológico, ocurrida en la década de los años sesenta, esta reacción,
presenta la siguiente secuencia:
En los años
siguientes, se han introducido en el anillo básico de las benzoquinolonas, el
flúor en la posición 6 y diversos grupos de heterociclos en la posición 7, para
dar lugar a las fluoroquinolonas de mayor espectro antibacteriano.
Partes importantes de
las metodologías utilizadas en estas síntesis han sido recopiladas por Leyva S
y Leyva E[2] en un
trabajo muy bueno desde la perspectiva bioquímica.
El método de las
desconexiones aplicado al reporte de las síntesis que se estudian y las
reacciones de las primeras etapas de las síntesis son de entera responsabilidad
del autor de esta monografía[3].
i) Síntesis reportada por Koga H. et al.[4]
Análisis
retrosintético:
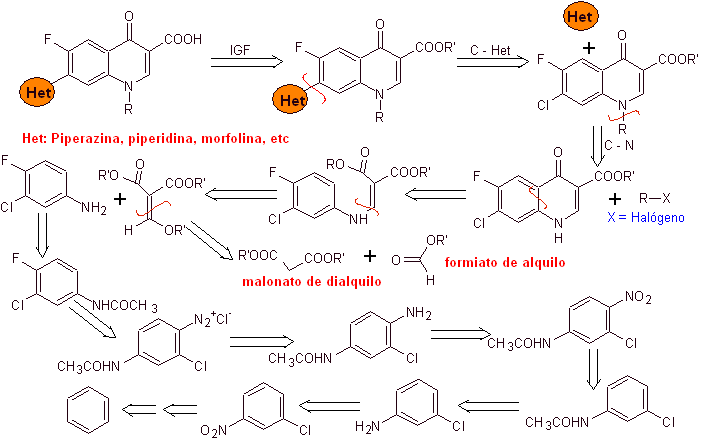
Síntesis:
Se parte del
benceno para formar la 3-cloro-4-fluoroanilina, que reacciona con el EMME de
dietilo para producir el acrilato correspondiente, que por calentamiento, forma
un compuesto cíclico. Este compuesto a su vez se hace reaccionar con un agente
alquilante y posteriormente se introduce el compuesto heterocíclico
nitrogenado, para finalmente hidrolizar y obtener la molécula objetivo.
[1] GOULD,
R.; JACOBS, W.A. J. Am. Chem. Soc. 1939,
61, 2890-2895
[2] LEYVA S. &
LEYVA E. Boletín de
[3] RIVERA W. Síntesis de Fármacos. Bolivia
[4] KOGA, h; et al. J. Med. Chem. 1980, 23, 1358-1363
Análisis
retrosintético:
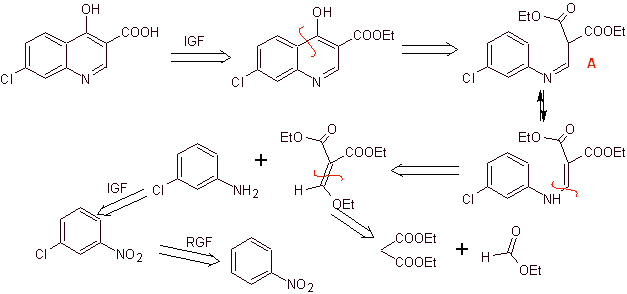
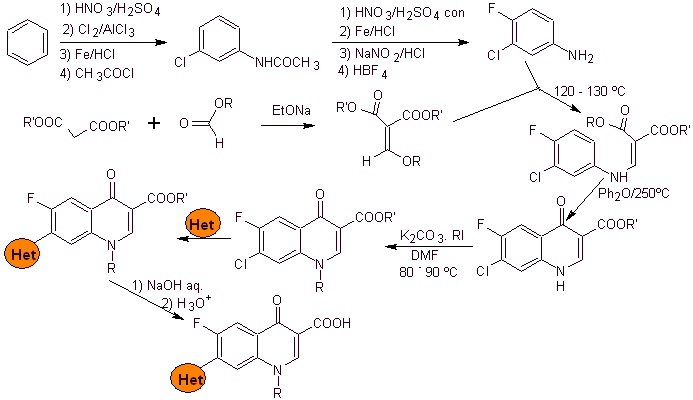
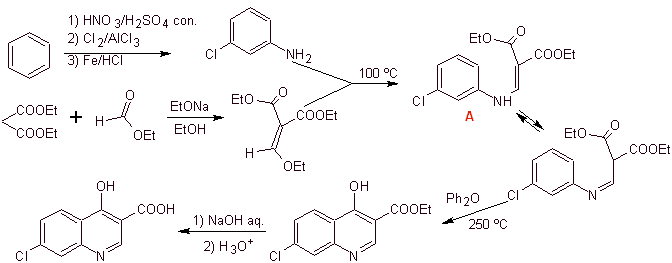
Síntesis: Se parte del benceno, para formar la 3-cloroanilina con el etoximetilenmalonato de dietilo (EMMET) formado a partir
de la condensación del formiato de etilo y el malonato de dietilo en medio
básico, para producir el compuesto A, que posteriormente es calentado en
presencia de un éter difenílico para generar el compuesto cíclico quinolínico,
que se hidroliza fácilmente al ácido correspondiente.
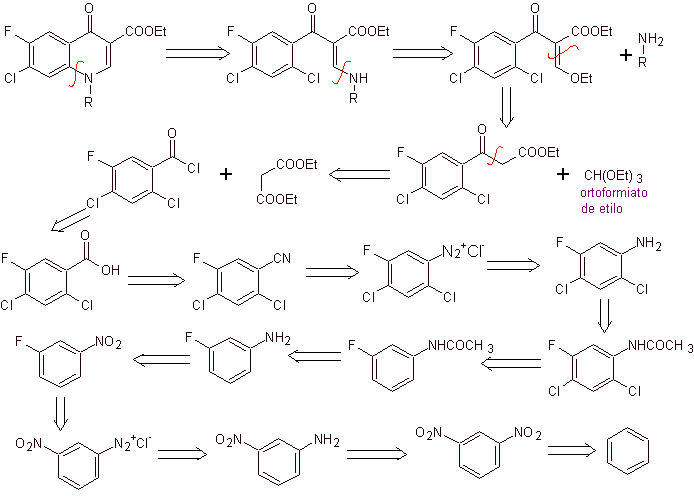
iii) Síntesis reportada por Grohe y Zeiler[2]
Análisis
retrosintético: Se empieza a
desconecta el enlace C-N y se continúa desconectando la amina, para llegar al
compuesto 1,3-diCO, que podría desconectarse como tal, pero se respeta la
reacción propuesta por sus autores y se genera el malonato de dietilo como
intermediario, así como el derivado multihalogenado del cloruro de benzoilo.
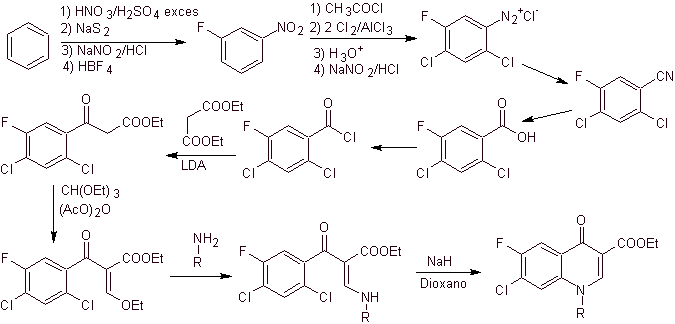
Síntesis. A partir del benceno se puede obtener el el benzoiloacetato de etilo sustituido con flúor y cloro en las
posiciones correspondientes. Este compuesto se hace reaccionar con
orto-formiato de trietilo para producir el etoxialqueno correspondiente, en
donde es posible sustituir el grupo etoxi por un grupo amino para producir la
amina respectiva, el cual es ciclado con una base fuerte a la fluoroquinolona.
Como puede observarse en la reacción de
ciclación participan como posibles grupos salientes el flúor, el cloro o el
nitro. Este método ha resultado muy versátil, y ha sido utilizado en la
síntesis de N-aril y N-alquil fluoroquinolonas.
iv) Síntesis reportada por Grohe y Heitzer[3]
Análisis
retrosintético.
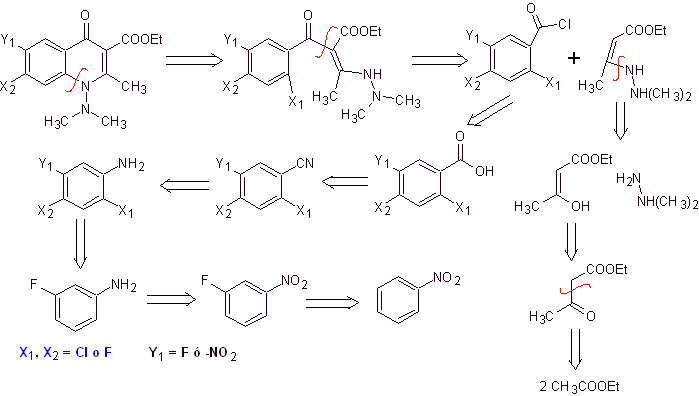
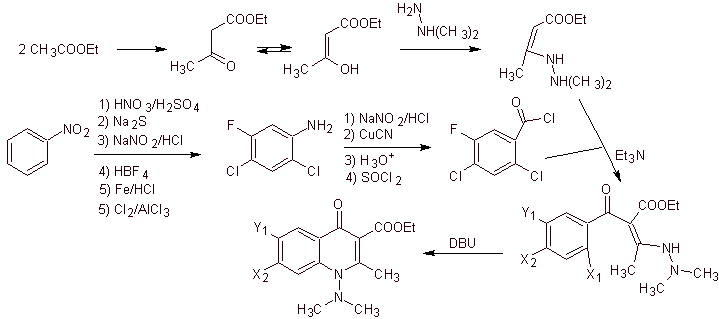
Síntesis. Se plantea una
ruta de síntesis convergente. Una de las cuales parte de la condensación de
Claisen de dos moles de acetato de etilo, para producir el acetoacetato de
etilo, que se combina con el derivado metilado de la hidrazina, que forma la
diamina viníloga, que será utilizada en la reacción con el derivado del cloruro
de benzoilo, formado a partir del nitrobenceno debido a la acción catalítica de
una amina terciaria.
El compuesto formado se cicla por la catálisis del DBU (1,8-Diazabicilo[5.4.0]undec-7-en), para producir una fluoroquinolona.
v) Síntesis reportada por Torii y cols[4]
Análisis
retrosintético.
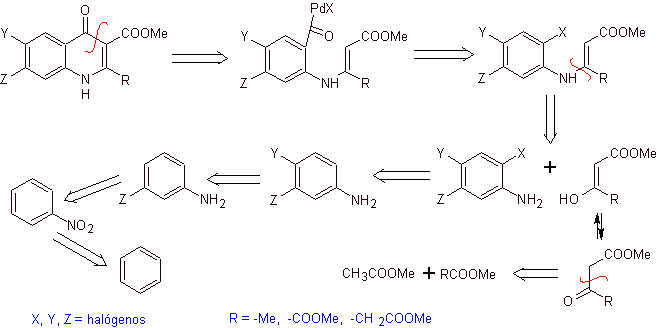
Torii y sus colaboradores en 1990, han reportado la síntesis de quinolonas
fluoradas por medio de un proceso de ciclación carbonilativa, catalizado por
Pd. Este método resulta muy adecuado para la síntesis de fluoroquinolonas,
sustituidas en la posición 2 (R = –Me, -CH2COOMe, –COOMe). Un análisis retrosintético de este
método parte por desconectar en el enlace acílico y proponer un organocadmio
como molécula precursora o equivalente sintético. El resto de desconecciones,
conducen a la anilina multisustiuída con
halógenos, como se indica a continuación:
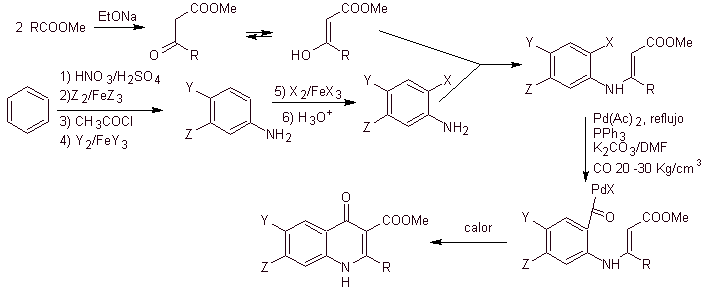
Síntesis. El diseño de síntesis se puede bosquejar nuevamente a través, de una ruta convergente. La primera ruta se refiere a la formación del acetoacetato de etilo y la segunda, partiendo del benceno a la anilina multihalogenada, que se ciclará en condiciones de carbonización catalítica por la presencia de paladio. Un calentamiento final del sistema permite la ciclación y formación de la fluoroquinolona.
vi) Síntesis reportada por Miyamoto y cols[5]
Análisis
retrosintético:
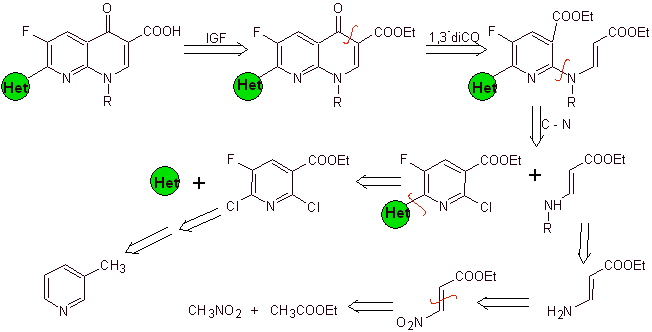
Síntesis. Como los halógenos en las posiciones
2 y 6 de la piridina son muy reactivos, es posible preparar quinolonas por el
procedimiento que se muestran Miyamoto y sus cols, en el cual el éster
2,6-dicloropiridínico se hace reaccionar con una amina cíclica para dar un
intermediario que se hace reaccionar con la amina viníloga, para luego ciclar
en medio básico. Hidroilizado el éster se forma
la fluoroquinolona.
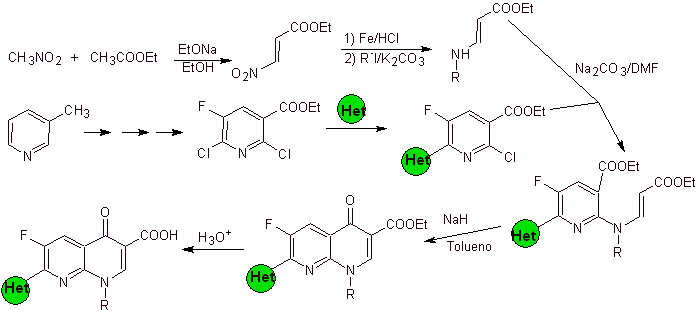
En todo caso, la formación del éster halogenado en las posiciones 2, 6 con cloro y F en la 5. Es la parte crítica
de esta síntesis. El éster piridínico multihalogenado, puede prepararse a
partir de la 3-metilpiridina (beta-picolina), que se obtiene de la destilación
del alquitrán de hulla.
vii) Síntesis reportada por Hayakawa[6]
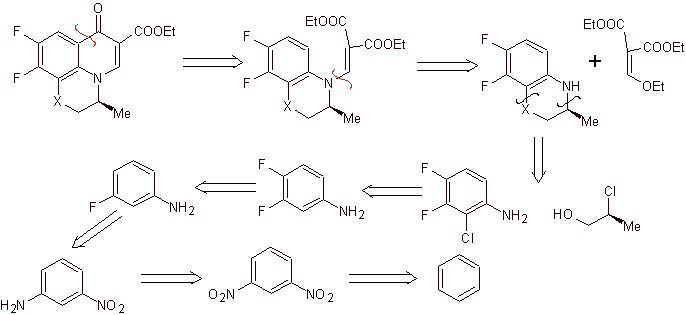
Análisis
retrosintético: Compuestos
tales como la flumequina y la ofloxacina, tienen una estructura tricíclica. La
síntesis de los mismos se realiza según Hayakawa y colaboradores, a partir de
una estructura que ya contiene el anillo heterocíclico nitrogenado.
Consiguientemente
se inicia la desconexión por el enlace C-O, resultado de la acilación del
anillo bencénico, se continúa con la desconexión C-N, lo que deja como
equivalentes sintéticos, a una estructura bicíclica y al EMME (etoximetilenmalonato de dietilo). La continuidad de la
desconexión depende de la naturaleza de X (-CH3, O, S). en el caso de ser O o S, la
desconexión puede ser simultánea como se indica. Las siguientes operaciones son
IGFs que permiten vislumbrar al benceno como material de partida.
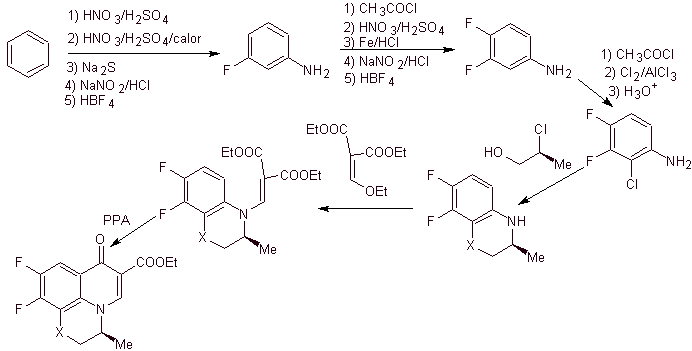
Síntesis. Se puede
combinar adecuadamente, las reacciones de Sandmeyer, para introducir el F y
crear condiciones estructurales para introducir el cloro. La formación del
heterociclo, puede efectuarse con 2-cloropropanol, formado a partir de la
apertura de un epóxido adecuado. El resto de reacciones que incluye el uso del
EMME, ya son conocidos por los métodos anteriormente vistos para la síntesis de
fluoroquinolonas.
viii) Síntesis reportada por Egawa y cols.
Análsis
retrosintético. El compuesto
tricíclico, se empieza a desconecta por el enlace C- O, aspecto que permite ver
que ese enlace fue resultado de una ciclación intramolecular de un compuesto
–OH con el F del benceno. Una segunda desconexión C-N, genera una molécula
precursora amínica del EMME. Las desconexiones siguientes son suficientemente
conocidas.
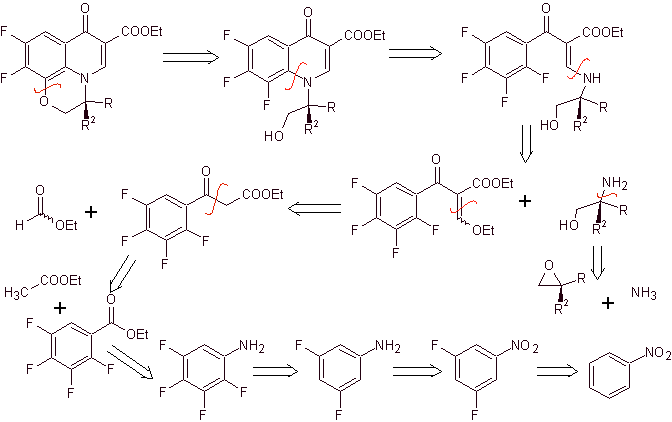
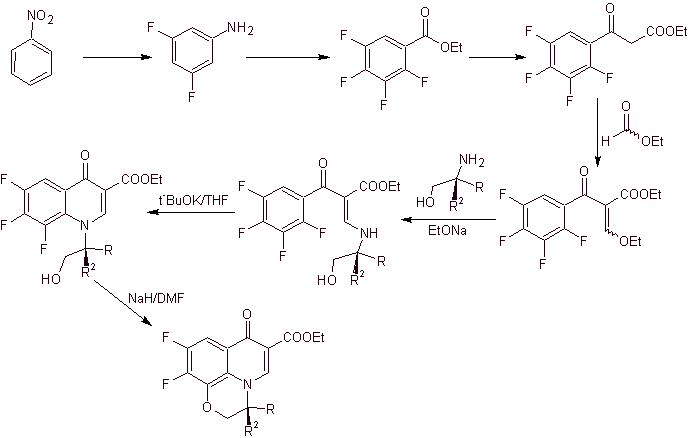
Síntesis. La fluoruración exhaustiva, por métodos indirectos del
benceno, se consigue primero utilizando el nitrobenceno como material de
partida, luego transformándolo en amina o amida, para lograr ocupar las otras
posiciones.
ix) Síntesis reportada por Matsumoto y cols
Análisis
retrosintético.
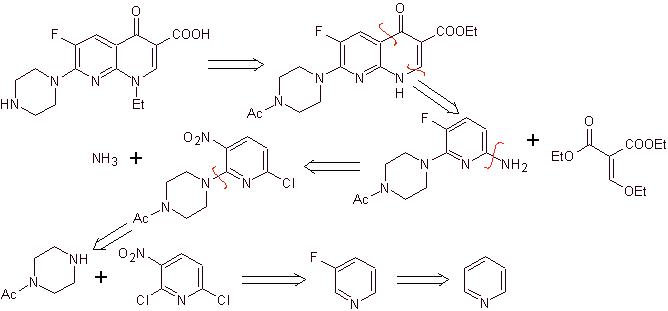
Síntesis: En el procedimiento reportado por
Matsumoto et al. se utilizó de nuevo la reacción de Gould-Jacobs; partiendo de
una nitropiridina diclorada se sintetizaron los intermediarios, primero con
El
tercer ciclo se consigue utilizando el EMME y alquilando la amina con yoduro de
etilo, para finalizar se hidroliza los grupos amida y éster.
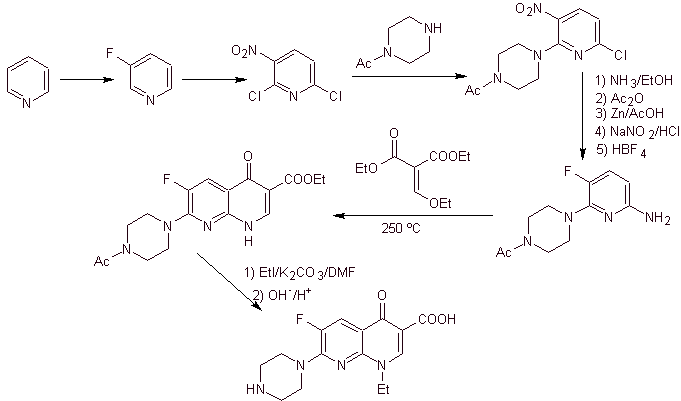
X) Síntesis reportada por Chu y colaboradores[7]
Análisis retrosintético: Se inicia desconectando el enlace C-N del heterociclo y se continua con el C-N de la amina viníloga. En el EMME, se desconecta por el doble enlace, para producir el formiato de etilo como molécula precursora, la siguiente desconección es del tipo 1,3-diCO, que nos vinculará a la condensación de Claisen.. Luego el éster aromático resultante, se somete a varios IGF, hasta llegar al nitrobenceno como material de partida
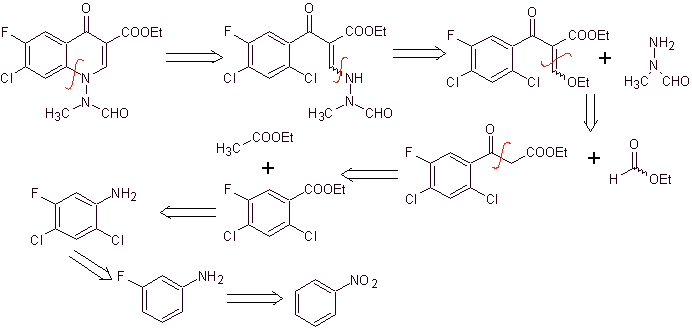
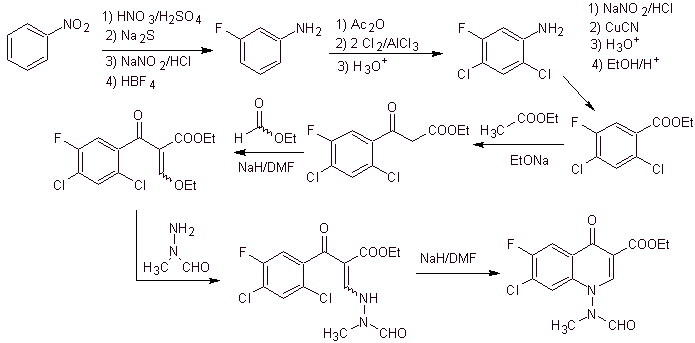
Síntesis. Se puede partir
del nitrobenceno, y con las reacciones necesarias llegar hasta el benzoati de
etilo sustituido adecuadamente con F y Cl, a partir de ello se utiliza la
condensación de Claisen seguida de otra condensación de Knoevenagel con el
formiato de etilo. Seguidamente se hace
reaccionar este intermediario con el N-formil-N-metilhidrazina y con la adición
de NaH, se logra ciclar para arribar al compuesto final.
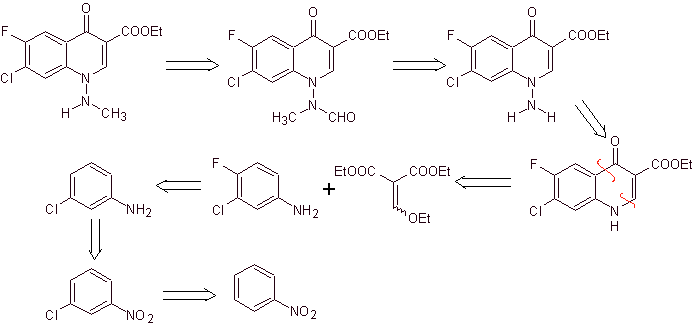
xi) Síntesis reportada por Wenthand y colaboradores
Análisis
retrosintético
Las quinolonas con un grupo amino sustituido en la posición 1, como la
amifloxacina, se pueden sintetizar siguiendo la metodología descrita por
Wentland. Por tal razón se inicia las desconexiones por el enlace N –C y luego se continúa con el enlace N-N y el
cierre del anillo, sigue la reacción de Gould – Jacobs.
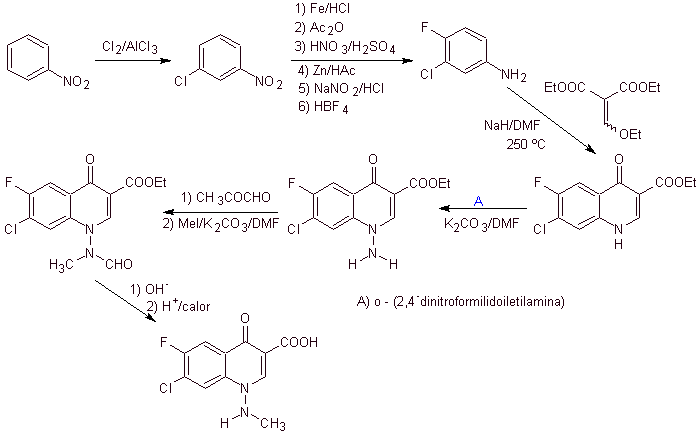
Síntesis. En este caso, se hace reaccionar el
grupo amino de la quinolona con un reactivo que transfiere otro grupo amino,
que posteriormente es convertido a un derivado de la formamida a fin de
transformarlo después al compuesto 1-(N
-metil)-7-cloro-6-flúor-1,4-dihidro-4-oxo-quinolina-3-ácido carboxílico.
[1] PRICE,
C.; ROBERTS, R.M. J. Am. Chem. Soc.
1946 68, 1204-1208
[2] GROHE,
K.; ZEILER, H.J. (Bayer, A.G.), DE, 3, 142, 854 A1
[3] GROHE,
K.; HEITZER, H.; Liebigs Ann. Chem.
1987, 29 - 37.
[4] TORII,
S.; Okumoto, H.; Xu, L.H. Tetrahedron
Lett. 1990, 31, 7175-7178
[5] MIYAMOTO,
t; Egawa, H. Shibamori, K.; Matsumoto, J. J.
Heterocycl. Chem. 1987, 24, 1333
– 1339.
[6] Citado por Leyva S. et al. Bol, Soc. Quím. Méx. Vol. 43, Num.
2 (1999) 63-68
[7] CHU, D.T.W.: et al. Drugs Exptl. Clin. Res. 1988, 14, 379-383