La quiralidad es sinónimo de asimetría, los objetos quirales se caracterizan por la ausencia de simetría, obsérvese las manos.
Los elementos de asimetría que conducen a moléculas quirales son: centros quirales, ejes de quiralidad, planos de quiralidad y hélices.
a) Centro quiral o estereogénico: es un átomo que une a cuatro grupos diferentes, uno de estos cuatro grupos puede ser un par libre.
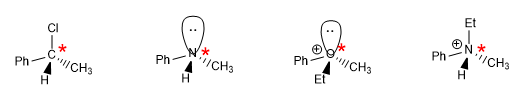
No sólo el carbono puede ser centro estereogénico, también el nitrógeno de aminas o sales de amonio, el oxígeno en los cationes oxonio, fosforo en fosfinas......
b) Los alenos son moléculas quirales, a pesar de no tener un centro estereogénico, debido a la presencia de un eje de quiralidad.
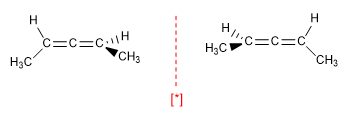
[*] Pareja de enantiómeros
El eje de quiralidad precisa de grupos diferentes unidos a cada carbono y que los grupos de un lado estén perpendiculares a los del otro lado.
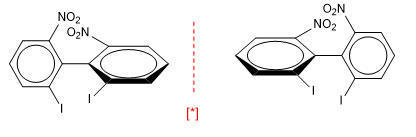
Los bifenilos también presentan ejes de quiralidad.

[*] Pareja de enantiómeros
c) Planos de quiralidad. Surgen en moléculas planas como los bencenos, cuando una cadena conecta dos posiciones del anillo bien por la parte de arriba o de abajo. Además, el benceno necesita de algún sustituyente que rompa la simetría.
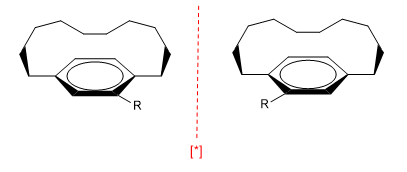
La cadena no puede ser muy larga, en caso contrario los enantiómeros se interconvierten.

[*] Pareja de enantiómeros
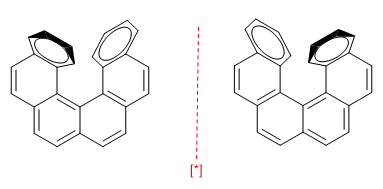
d) Hélices. Las moléculas helicoidales también pueden presentar quiralidad.

[*] Pareja de enantiómeros
En este caso la quiralidad se debe a la repulsión de los dos anillos superiores, que obliga a uno de ellos a retorcese hacia nosotros mientras el otro se mete hacia el fondo.
 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?