Il controllo nella sintesi organica è uno dei compiti più importanti per ottenere la trasformazione richiesta o pianificata. e/o da evitare la formazione di quei sottoprodotti che compromettono sostanzialmente lo sviluppo ottimale della sintesi organica in questione. Parimenti, da una prospettiva più generale, il controllo può includere o coprire anche gli aspetti di simmetria e selettività.
Quindi, il controllo dovrebbe essere inteso come una serie di operazioni sintetiche che consentono al chimico di formare lo scheletro di carbonio con la funzionalità prevista o di "collocare" un gruppo o un atomo nel luogo o nella posizione richiesta.
Di conseguenza, queste operazioni possono essere di una vasta gamma di routine con un'intenzione riflessa dal chimico e che richiedono determinate capacità e abilità cognitive simili a quelle artistiche, per la costruzione (sintesi) di molecole organiche.
Pertanto, nelle reazioni di condensazione, come in altre, le operazioni di controllo possono essere incluse in una delle seguenti categorie.
![]() Reazioni concorrenti (autocondensazione e/o condensazione incrociata)
Reazioni concorrenti (autocondensazione e/o condensazione incrociata)
![]() Attivazione – disattivazione
Attivazione – disattivazione
![]() Selettività e specificità
Selettività e specificità
![]() Protezione-deprotezione
Protezione-deprotezione
Nelle reazioni di condensazione dei composti carbonilici è fondamentale stabilire in anticipo l'ordine degli eventi per minimizzare o, se necessario, sopprimere le possibilità di autocondensazione e il verificarsi di condensazione incrociata, che purtroppo rappresentano una minaccia evidente in queste reazioni .
autocondensazione
Tutti i composti carbonilici che hanno uno o più idrogeni alfa, sui carboni adiacenti al gruppo carbonilico, corrono il rischio di subire una reazione di autocondensazione se non si segue il corrispondente rigore.
Così, per esempio, se una base non idrossilata come EtONa viene aggiunta a un 2-butanone, si formerà un enolato che potrebbe eventualmente combinarsi con un'altra molecola dello stesso chetone. Allo stesso modo, se si aggiunge H+, può verificarsi anche l'autocondensazione, come si può vedere nel seguente schema: Questo può essere minimizzato aggiungendo alla stessa velocità, da alimentatori separati, la base o l'acido al composto che fornirà l'enolo o enolato e il composto carbonilico che sarà attaccato sul carbonio carbonilico . È possibile utilizzare un pallone a tre colli e l'agitazione magnetica.
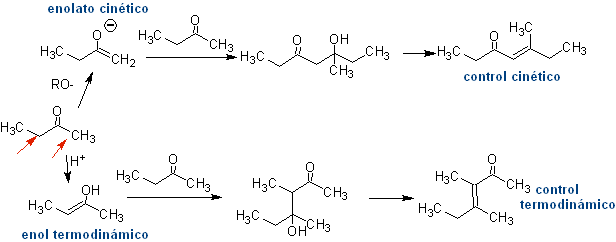
condensazione incrociata
Idealmente, nelle reazioni di condensazione di composti carbonilici, una delle molecole reagenti dovrebbe enolizzarsi rapidamente, mentre l'altra dovrebbe preferibilmente non avere Hα. , per garantire che non si formino altri sottoprodotti
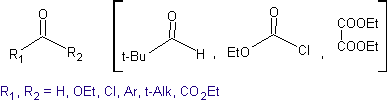
La retrosintesi che si analizza di seguito è un buon esempio di quanto precedentemente indicato.
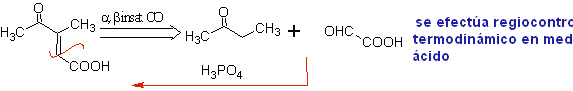
Condensazione intramolecolare .
Quando in una molecola sono presenti due gruppi funzionali che influenzano direttamente i carboni alfa rispetto al carbonile, è molto probabile che vi sia un'autocondensazione intramolecolare e i cicli che si formano devono avere un'elevata stabilità, come nel caso degli anelli di cinque e sei maglie. Anelli con un maggior numero di maglie difunzionalizzate (7, 8 ecc.), non sono prodotti probabili a causa della labilità di questi cicli.
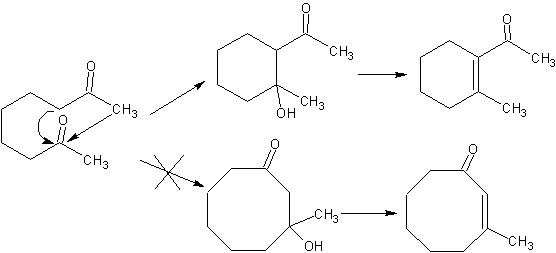
Utilizzando la reazione di Mannich.
Nelle reazioni di addizione coniugata su substrati carbonilici alfa, beta-insaturi ( α, β-inssatCO), caratteristici della reazione di Michael, appare la necessità di utilizzare vinilchetoni. Ma quando si cerca di prepararlo dalla condensazione del chetone e della formaldeide, si formano altri prodotti di polimerizzazione dell'aldeide che ne rendono difficile la preparazione.
La reazione di Mannich consente di ottenere vinilchetoni durante la sintesi e al momento necessario, che per altri mezzi presenta serie difficoltà nella sua preparazione. Questo aspetto è illustrato nella sintesi di MOb 25
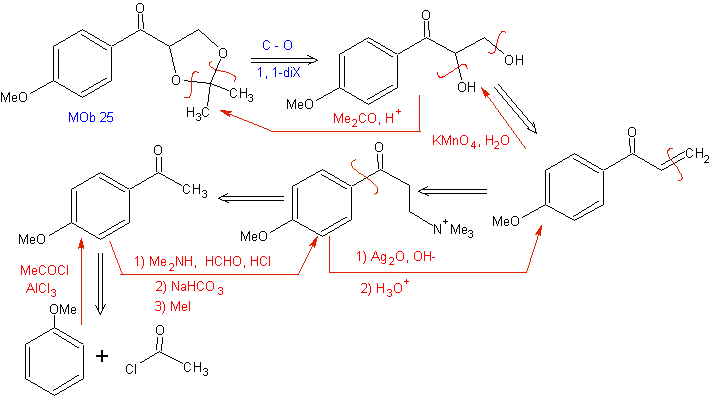
Attivazione dei gruppi
Sistema non attivato:
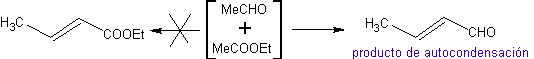
sistema attivato
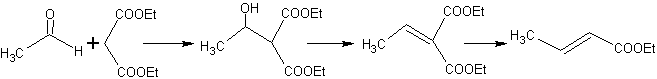
¨ enammini
È già stato detto che un modo per avere un enolato attivato è la formazione di un'enammina, tra il composto carbonilico e un'ammina secondaria. Questo aspetto è mostrato nel seguente esempio di sintesi.
Analisi retrosintetica: Nella sintesi di MOb 26, si osserva l'uso corretto di enammine per garantire la formazione del composto 1,3 diCO.
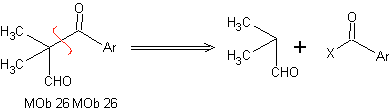
Sintesi: L'enamina formata, permette alla sua rispettiva acilazione, di raggiungere il Mob26
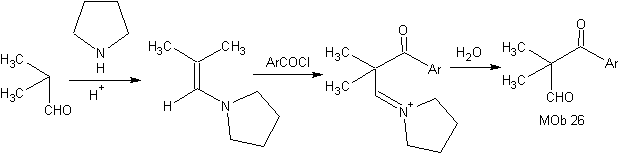
¨ riduzione della betulla
Questa riduzione costituisce una buona alternativa per preparare i cicloesenoni, come si può vedere nella sintesi di MOb 27:
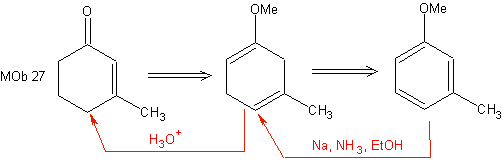
Tuttavia, va ricordato che alcuni composti α, β -carbonil insaturo, può anche essere preparato dalla reazione di Wittig e attraverso la reazione di Reformatsky.
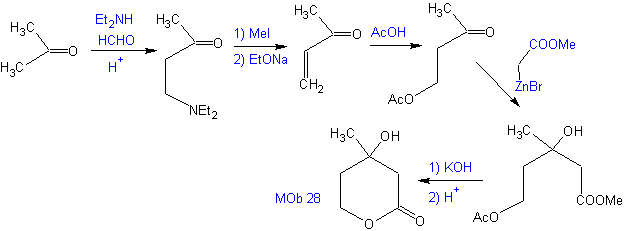
Proporre un piano di sintesi, da materiali semplici per MOb 28.
Analisi retrosintetica: Inizialmente il lattone è disconnesso, seguito dalla disconnessione come modello 1,3-diO. Il composto carbonilico α,β-insaturo (α,β- insat. CO) generato potrebbe essere stato ottenuto per eliminazione di Hoffmann e chetoammina, per reazione di Mannich
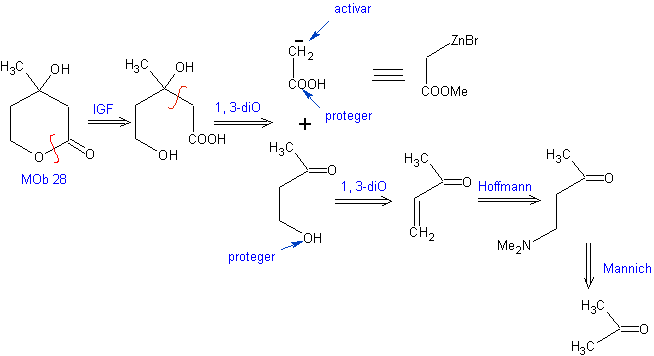
Sintesi: Il sintesi di Mob 28, è molto appropriato per mostrare il controllo che deve essere esercitato su alcuni centri di reazione per ottenere le trasformazioni desiderate e necessarie.