Kontrol dalam sintesis organik adalah salah satu tugas terpenting untuk mencapai transformasi yang diperlukan atau direncanakan. dan/atau untuk menghindari pembentukan produk sampingan yang secara substansial mengganggu perkembangan optimal sintesis organik yang bersangkutan. Demikian pula, dari perspektif yang lebih umum, kontrol juga dapat mencakup atau mencakup aspek simetri dan selektivitas.
Kemudian, kontrol harus dipahami sebagai serangkaian operasi sintetik yang memungkinkan ahli kimia membentuk kerangka karbon dengan fungsi yang dimaksudkan atau untuk "menempatkan" suatu kelompok atau atom di tempat atau posisi yang diperlukan.
Konsekuensinya, operasi ini mungkin dari berbagai rutinitas dengan maksud yang dicerminkan oleh ahli kimia dan yang menuntut kemampuan dan keterampilan kognitif tertentu yang serupa dengan yang artistik, untuk konstruksi (sintesis) molekul organik.
Oleh karena itu, dalam reaksi kondensasi, seperti yang lainnya, operasi kontrol dapat dimasukkan dalam salah satu kategori berikut.
![]() Reaksi bersaing (self-kondensasi dan/atau kondensasi silang)
Reaksi bersaing (self-kondensasi dan/atau kondensasi silang)
![]() Aktivasi – penonaktifan
Aktivasi – penonaktifan
![]() Selektivitas dan spesifisitas
Selektivitas dan spesifisitas
![]() Proteksi-deproteksi
Proteksi-deproteksi
Dalam reaksi kondensasi senyawa karbonil, penting untuk menetapkan urutan kejadian terlebih dahulu untuk meminimalkan atau, jika perlu, menekan kemungkinan kondensasi sendiri dan terjadinya kondensasi silang, yang sayangnya merupakan ancaman nyata dalam reaksi ini. .
kondensasi diri
Semua senyawa karbonil yang memiliki satu atau lebih hidrogen alfa, pada karbon yang berdekatan dengan gugus karbonil, berisiko mengalami reaksi kondensasi sendiri jika kekakuan yang sesuai tidak diikuti.
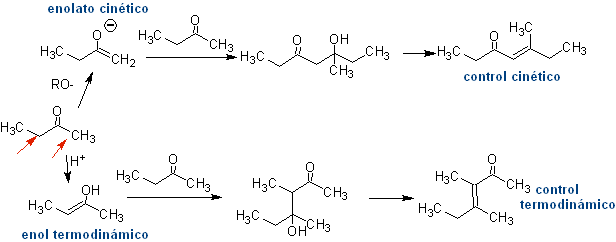
Jadi, misalnya, jika basa non-hidroksilasi seperti EtONa ditambahkan ke 2-butanon, enolat akan terbentuk yang pada akhirnya dapat bergabung dengan molekul lain dari keton yang sama. Demikian pula, jika H+ ditambahkan, kondensasi diri juga dapat terjadi, seperti dapat dilihat pada skema berikut: Hal ini dapat diminimalkan dengan menambahkan pada tingkat yang sama, dari pengumpan terpisah, basa atau asam ke senyawa yang akan menghasilkan enol atau enolat dan senyawa karbonil yang akan diserang pada karbon karbonil. . Labu berleher tiga dan pengaduk magnet dapat digunakan.
kondensasi silang
Idealnya, dalam reaksi kondensasi senyawa karbonil, salah satu molekul yang bereaksi harus mengalami enolisasi dengan cepat, sedangkan yang lain sebaiknya tidak memiliki Hα. , untuk memastikan bahwa tidak ada produk sampingan lain yang terbentuk
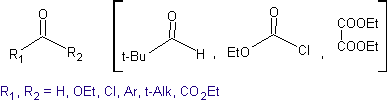
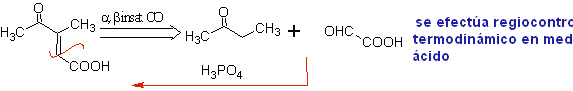
Retrosintesis yang dianalisis di bawah ini adalah contoh yang baik dari apa yang ditunjukkan sebelumnya.
Kondensasi intramolekul .
Ketika ada dua gugus fungsional dalam sebuah molekul yang secara langsung mempengaruhi karbon alfa dalam kaitannya dengan karbonil, kemungkinan besar terjadi kondensasi diri intramolekul dan siklus yang terbentuk harus memiliki stabilitas tinggi, seperti halnya cincin. dari lima dan enam link. Cincin dengan jumlah tautan yang difungsikan lebih banyak (7, 8 dst.), bukanlah produk yang mungkin karena labilitas siklus ini.
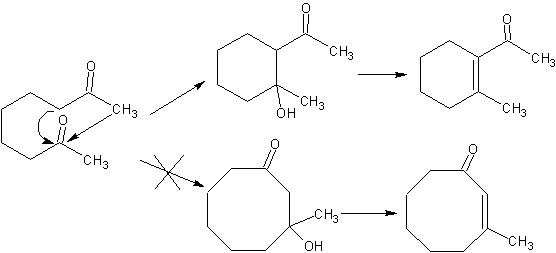
Menggunakan reaksi Mannich.
Dalam reaksi adisi konjugasi pada substrat karbonil alfa, beta-tak jenuh ( α, β-insatCO), karakteristik reaksi Michael, kebutuhan untuk menggunakan vinil keton muncul. Tetapi ketika dicoba dibuat dari kondensasi keton dan formaldehida, produk polimerisasi aldehida lainnya terbentuk yang membuat pembuatannya sulit.
Reaksi Mannich memungkinkan vinil keton diperoleh selama sintesis dan pada saat yang diperlukan, yang dengan cara lain menghadirkan kesulitan serius dalam persiapannya. Aspek ini diilustrasikan dalam sintesis MOb 25
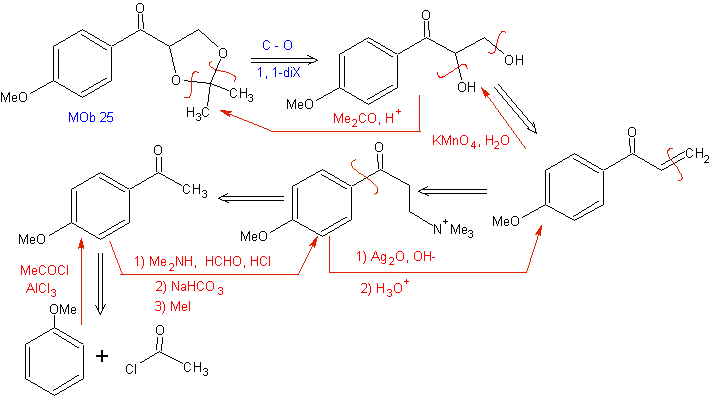
Aktivasi grup
Sistem tidak diaktifkan:
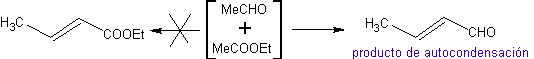
sistem diaktifkan
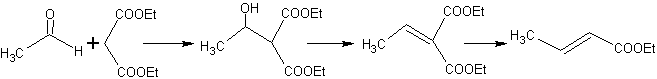
¨ enamina
Telah dikatakan bahwa salah satu cara untuk mengaktifkan enolat adalah pembentukan enamina, antara senyawa karbonil dan amina sekunder. Aspek ini ditunjukkan dalam contoh sintesis berikut.
Analisis retrosintetik: Dalam sintesis MOb 26, penggunaan enamina yang tepat diperhatikan untuk menjamin pembentukan senyawa 1,3 diCO.
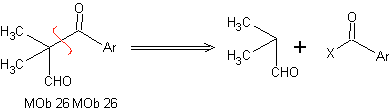
Sintesis: Enamina terbentuk, memungkinkan asilasinya masing-masing, untuk mencapai Mob26
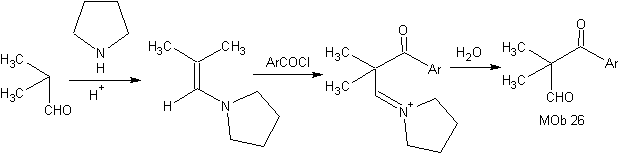
¨ pengurangan birch
Reduksi ini merupakan alternatif yang baik untuk membuat siklohekson, seperti yang dapat dilihat pada sintesis MOb 27:
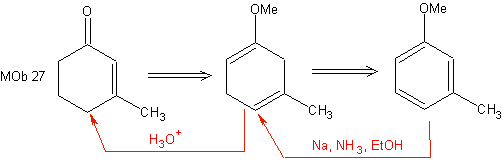
Namun, harus diingat bahwa senyawa α, β tertentu -karbonil tak jenuh, juga dapat dibuat dengan reaksi Wittig dan melalui reaksi Reformatsky.
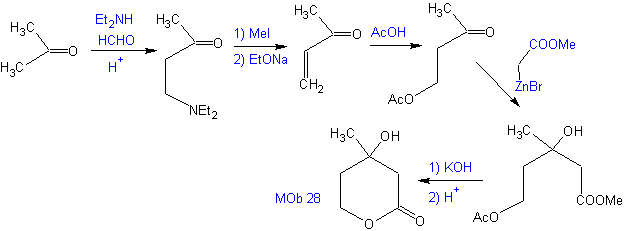
Usulkan rencana sintesis, dari bahan sederhana untuk MOb 28.
Analisis retrosintetik: Awalnya lakton terputus, diikuti dengan pemutusan sebagai pola 1,3-diO. Senyawa karbonil tak jenuh α,β (α,β- insat. CO) yang dihasilkan dapat diperoleh dengan eliminasi Hoffmann dan ketoamina, dengan reaksi Mannich
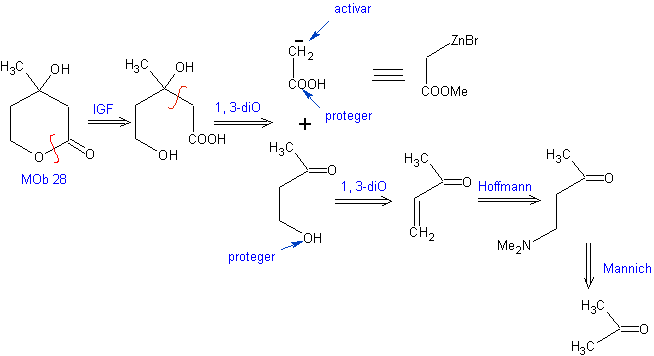
Sintesis: The sintesis Mob 28, sangat tepat untuk menunjukkan kontrol yang harus dilakukan pada pusat reaksi tertentu untuk mencapai transformasi yang diinginkan dan diperlukan.