Las vibraciones moleculares pueden estudiarse con el modelo del oscilador armónico cuántico. La energía viene dada por:
\begin{equation}\label{energia-oscilador} E_v=\left(v+\frac{1}{2}\right)h\nu \end{equation}
Los distintos niveles de energía vienen dados por el número cuántico v, que toma valores 0.1.2.3.4.....
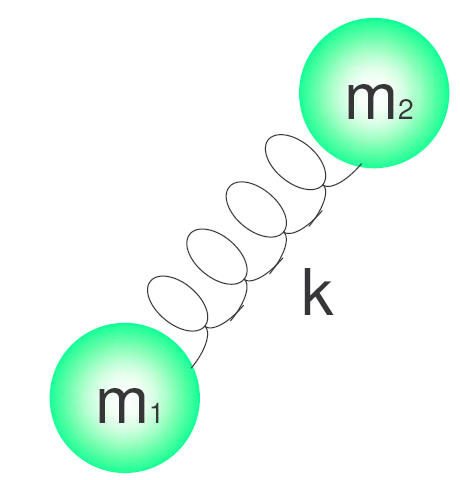
h es la constante de Planck y $\nu$ la frecuencia del oscilador que viene dada por la expresión:\begin{equation} \nu=\frac{1}{2\pi}\sqrt{\frac{k}{\mu}} \end{equation} Donde k es la constante de fuerza del muelle y $\mu$ la masa reducida del sistema. $\mu=\frac{m_1m_2}{m_1+m_2}$.
Dividiendo la frecuencia entre la velocidad de la luz se obtiene número de ondas $\bar{\nu}$ \begin{equation}\label{numero-ondas} \bar{\nu}=\frac{1}{2\pi c}\sqrt{\frac{k}{\mu}} \end{equation} El estudio de la ecuación (\ref{numero-ondas}) nos permitirá predicir a qué número de ondas absorben radiación infrarroja los enlaces de una molécula. Esta ecuación sólo es aplicable a las vibraciones de tensión.
Frecuencias de absorción altas
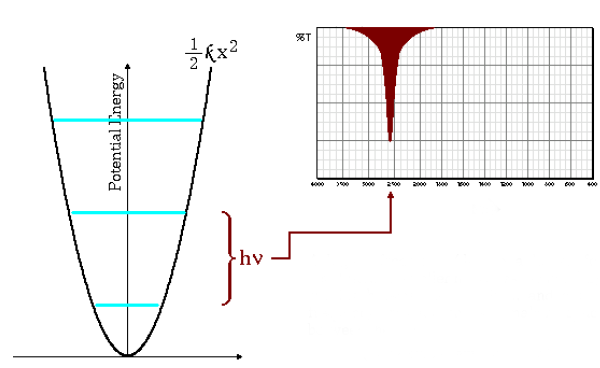
La ecuación (\ref{numero-ondas}) indica que masas reducidas pequeñas (átomos de poca masa) y constantes de fuerza altas (enlaces fuertes) conducen a frecuencias altas. En estas condicionees las bandas de absorción salen a numeros de onda altos.
Como puede observarse en el gráfico las frecuencias altas dan lugar a un mayor espaciado entre los niveles energéticos.
Frecuencias de absorción bajas
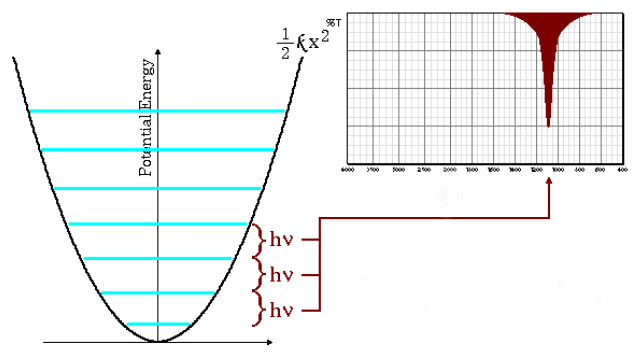
La ecuación (\ref{numero-ondas}) indica que masas reducidas grandes y constantes de fuerza pequeñas (enlaces débiles) conducen a frecuencias bajas. En estas condicionees las bandas de absorción salen a numeros de onda bajos.
Como puede observarse en el gráfico las frecuencias bajas dan lugar a un menor espaciado entre los niveles energéticos.
 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?