Нуклеофилы представляют собой основания Льюиса, которые атакуют углерод, вытесняя уходящую группу. Ионные нуклеофилы распространены, но есть также многочисленные примеры нейтральных нуклеофилов. Общей характеристикой всех нуклеофилов является наличие неподеленных пар у атакующего атома.
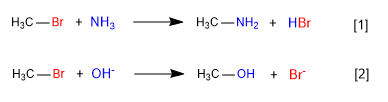
[1] Медленно
[2] Быстро
В первой реакции аммиак действует как нуклеофил-нейтральная частица, но с неподеленными парами на азоте, вытесняя бром из углерода и образуя амин.
Во второй реакции гидроксид-ион действует как нуклеофил, вытесняя бром и образуя спирт. Замечено, что первая реакция протекает медленнее второй, и в заключение аммиак является худшим нуклеофилом, чем гидроксид-ион.
Способность нуклеофила атаковать субстрат известна как нуклеофильность.Нуклеофильность зависит от нескольких факторов: положения атакующего атома в периодической таблице, заряда и резонанса.
Заряд - заряженные частицы являются лучшими нуклеофилами, чем нейтральные.
OH ->> H 2 O гидроксид-ион (заряженные частицы) лучший нуклеофил, чем вода (нейтральные частицы)
NH 2 ->> амид-ион NH 3 (заряженные частицы) лучший нуклеофил, чем аммиак (нейтральные частицы)
PH 2 ->> PH 3 фосфид-ион (заряженные частицы) лучший нуклеофил, чем фосфин (нейтральные частицы)
Положение в таблице Менделеева - нуклеофильность увеличивается при движении вниз по таблице Менделеева и влево.
NH 3> H 2 O аммиак является лучшим нуклеофилом, чем вода, потому что азот находится левее кислорода
I -> Cl - йодид является лучшим нуклеофилом, чем хлорид, потому что он расположен ниже.
PH 3> NH 3 фосфин является лучшим нуклеофилом, чем аммиак, потому что фосфор ниже азота.
Резонанс - Резонанс снижает нуклеофильность. Делокализация неподеленных пар снижает способность нуклеофила к атаке.
OH -> CH 3 COO - Ион ацетата менее нуклеофилен, чем ион гидроксида, из-за делокализации заряда на обоих атомах кислорода.









