Hola usuario pregunton,
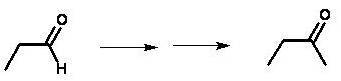
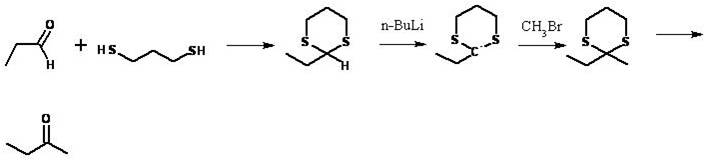
por un lado coincido ampliamente con el usuario Janer, por otro te recomiendo que reveas el concepto de reactivo de Grignard. Tu ruta de síntesis emplea un compuesto con dos funciones tiol, que se usa especialmente para proteger grupos sensibles a una reacción cuando la pretendemos hacer de manera selectiva. En este caso, en el aldehído no tiene ningún grupo sensible, por lo tanto es inútil recurrir esa mecanismo. Además, otra de sus utilidades es que el hemitiol cíclico reacciona sólo en condiciones ácidas (con H+), ni con el reactivo de Gilman ni nada por el estilo.
Uno de los tantos casos en los que sirve el uso de ditioles es para convertir ciclocetohexanal a hidroxiciclohexanal con el reductor NaBH4, puesto que si no usaras la protección podría también reducirse la cetona.