¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp. .
Más información en www.foroquimico.com
Si prefieres un curso de química orgánica tanto básica como avanzada te invito a acceder al canal: https://www.youtube.com/channel/UC_RiUaA2326jO9XozAA4q2g , en el que encontrarás más de 750 vídeos de teoría y ejercicios.
Espectroscopía visible-Ultravioleta
ESPECTROSCOPÍA VISIBLE-ULTRAVIOLETA
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA VISIBLE-ULTRAVIOLETA
- Visto: 28008
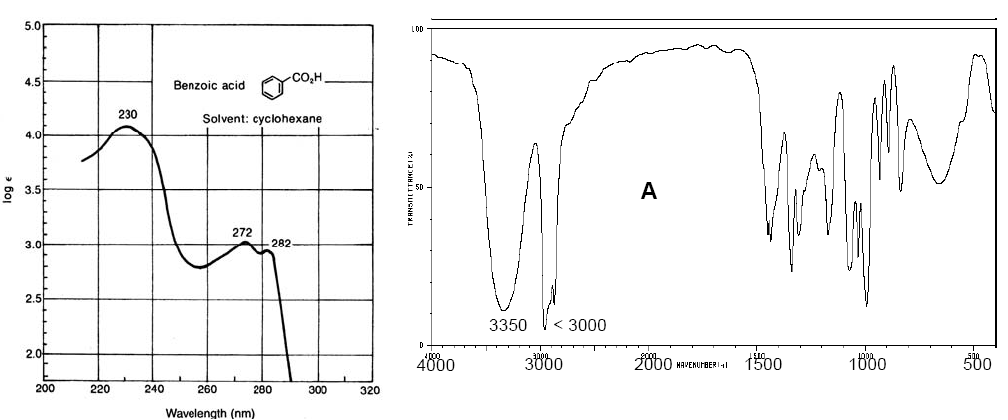 Espectro vis-UV del ácido benzoico (izq). Espectro IR del ciclopentanol (dcha)
Espectro vis-UV del ácido benzoico (izq). Espectro IR del ciclopentanol (dcha)
Los espectros vis-UV tienen una resolución más baja que los de IR debido a que cada nivel electrónico se divide en niveles vibracionales y estos a su vez en niveles rotacionales, de manera que una transición electrónica consta de un amplio conjunto de transiciones roto-vibracionales. Los espectros de IR también poseen bandas de una amplitud considerable debido a las transiciones rotacionales que se producen simultáneamente a las transiciones vibracionales.
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA VISIBLE-ULTRAVIOLETA
- Visto: 100865
Los grupos cromóforos son los grupos funcionales de la molécula responsables de la absorción. Principalmente son: dobles y triples enlaces carbono-carbono, sistemas aromáticos, grupo carbonilo, imino (C=N), diazo (N=N), nitro y enlaces C-Y (Y es un átomo con pares libres).
Los grupos auxocromos son sustituyentes del cromóforo y alteran $\lambda_{max}$ y/o $\epsilon_{max}$. Son auxocromos los grupos metilo, halógenos, hidroxi, alcoxi, amino.
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA VISIBLE-ULTRAVIOLETA
- Visto: 47134
- Alcanos. Sus bandas de absorción son debidas a transiciones $\sigma\rightarrow\sigma^{\ast}$ de enlaces C-C y C-H. Estas transiciones son de elevada energía y tienen lugar a longitudes de onda inferiores a los 150 nm, no observables por tanto en espectrofotómetros convencionales. Esta característica permite utilizarlos como disolventes de la muestar a anlizar, ya que no interfieren con sus señales.
- Alquenos y alquinos. Presentan bandas de absorción debidas a las transiciones $\pi\rightarrow\pi^{\ast}$ del triple enlace C-C. Esta transición es de menor energía que en el caso de los alcanos y aparece a longitudes de onda mayores (alquenos:175 nm; alquinos: 170 nm). El doble y triple enlace son los grupos cromóforos de estas moléculas.
- Éteres, tioles, sulfuros, aminas: En este caso el grupo cromóforo está formado por el heteroátomo (O,S,N) y los átomos que le enlazan. El heteroátomo presenta pares libres y la transición que produce la absorción es $n\rightarrow\sigma^{\ast}$. Esta banda de absorción aparece sobre 175-200 nm para alcoholes, éteres y aminas, desplazándose a 200-220 nm para los sulfuro.
- Aldehídos, cetonas, ácidos y derivados. El grupo cromóforo de estos compuestos es el carbonilo (C=O). Dado que el oxígeno posee pares libres, la transición de menor energía es la $n\rightarrow\pi^{\ast}$, pero es una transición prohibida ($\epsilon_{max}=15$), al no existir solapamiento entre los orbitales implicados. La siguiente transición de menor energía es la $\pi\rightarrow\pi^{\ast}$, observable a $\lambda_{max}=188\;nm$, con absortividad molar de 900.
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA VISIBLE-ULTRAVIOLETA
- Visto: 30686
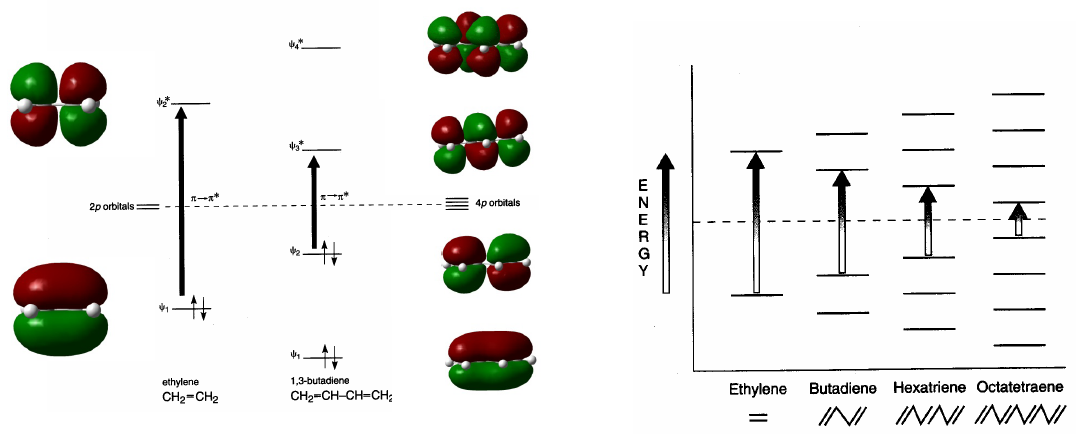
Los sistemas conjugados absorben a mayores longitudes de onda que los no conjugados. A medida que la conjugación aumenta decrece la diferencia energética entre HOMO y LUMO y la radiación necesaria para producir la transición $\pi \rightarrow \pi^{\ast}$ disminuye su longitud de onda.
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA VISIBLE-ULTRAVIOLETA
- Visto: 20173
El diagrama de orbitales moleculares del $\alpha,\beta$-insaturado se construye a partir de los orbitales moleculares del eteno y del carbonilo
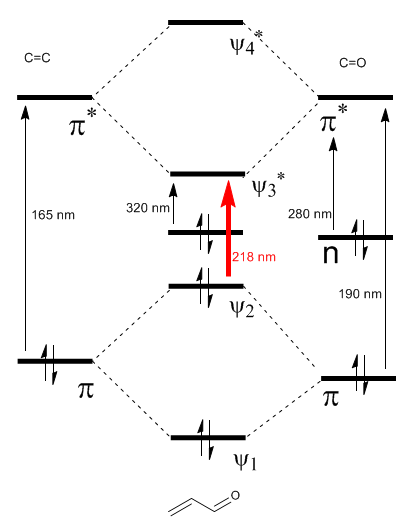
Leer más: Efecto batocrómico en carbonilos $\alpha,\beta$-insaturados
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA VISIBLE-ULTRAVIOLETA
- Visto: 18973
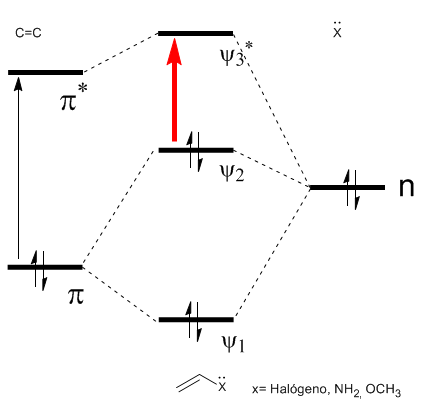
Como puede observarse en el diagrama la conjugación con los pares libres del grupo X produce un acercamiento entre los orbitales HOMO y LUMO, dando lugar a una transición de menor energía (mayor longitud de onda) que en el eteno.
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA VISIBLE-ULTRAVIOLETA
- Visto: 32577
El espectro de absorción del benceno consta de tres bandas a 184, 204 y 256 nm, que suelen denominarse $\alpha$, p y $\beta$. Las bandas $\alpha$, p tambien se conocen como primarias y la $\beta$ banda secundaria. La banda secundaria es amplia debido a su estructura vibracional.