TEORÍA DE INDOL
- Detalles
- Germán Fernández
- TEORÍA DE INDOL
- Visto: 2150
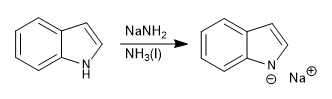
El indol presenta un hidrógeno ácido sobre el átomo de nitrógeno, con pKa= 17. Empleando bases fuertes se puede desprotonar formando el anión indolio.
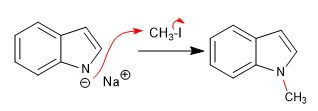
Reacción del indolio con diferentes electrófilos:
a) Alquilación:
b) Apertura de epóxidos:
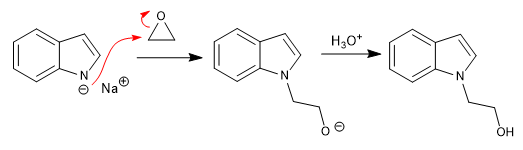
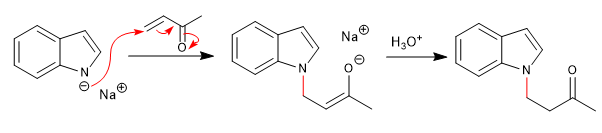
c) Ataque a a,b-insaturados:
- Detalles
- Germán Fernández
- TEORÍA DE INDOL
- Visto: 1735
El ataque a los electrófilos se produce desde la posición 3, debido a que el anillo pirrol es más rico en densidad de carga que el carbociclo. Dicho ataque se ve favorecido por la cesión del par libre del nitrógeno.
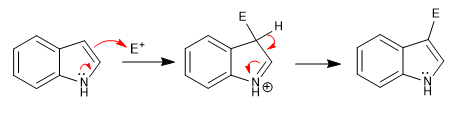
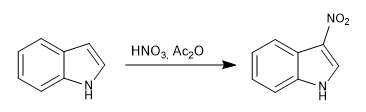
a) Nitración:
El indol se nitra con la mezcla nítrico en anhídrido acético.
- Detalles
- Germán Fernández
- TEORÍA DE INDOL
- Visto: 1295
Los indoles 3-sustituidos adicionan el electrófilo a la posición 3, transponiéndolo a la posición 2 en una etapa posterior.
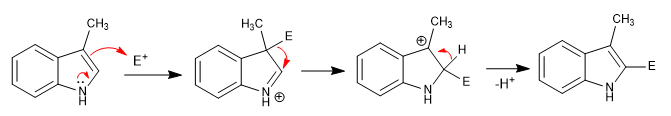
Leer más: Sustitución electrófila con la posición 3 del indol ocupada
- Detalles
- Germán Fernández
- TEORÍA DE INDOL
- Visto: 2071
a) Grupos salientes en posición vecina al anillo
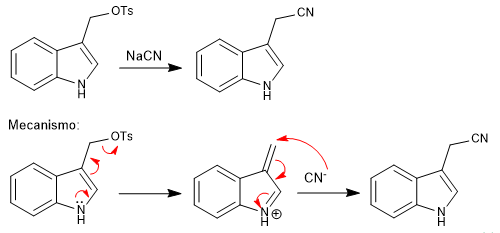
- Detalles
- Germán Fernández
- TEORÍA DE INDOL
- Visto: 1520
El anillo indol se expande a una quinolina halogenada en posición 3 por reacción con cloroformo en medio básico. La mezcla HCCl3/NaOH genera un carbeno, que reacciona con el doble enlace del anillo pirrol. El intermedio se abre ayudado por la cesión del par libre del nitrógeno, rindiendo una quinolina.
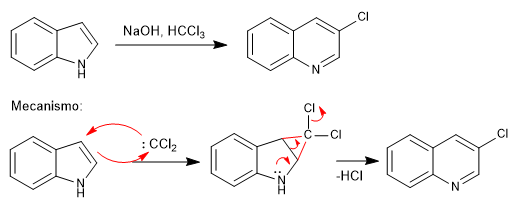
- Detalles
- Germán Fernández
- TEORÍA DE INDOL
- Visto: 1684
Podemos reducir de forma selectiva el carbociclo o el anillo pirrol.
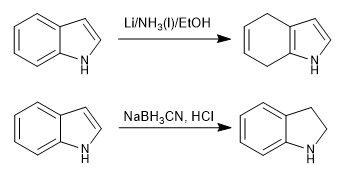
- Detalles
- Germán Fernández
- TEORÍA DE INDOL
- Visto: 5381
Es una de las síntesis más importantes del indol. Parte de fenilhidrazina y de un carbonilo con hidrógenos alfa, que generan una hidrazona. Después de una tautomería, se produce una sigmatrópica que rinde el indol previa ciclación.
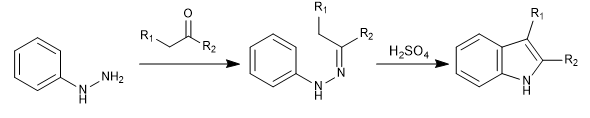
La etapa de formación de la hidrazona tiene un mecanismo muy conocido (el mismo que forma iminas) y no vamos a comentarlo. Nos centraremos en las etapas que transforman la hidrazona en indol.
Etapa 1. Tautomería.
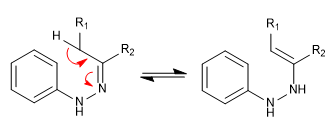
- Detalles
- Germán Fernández
- TEORÍA DE INDOL
- Visto: 4386
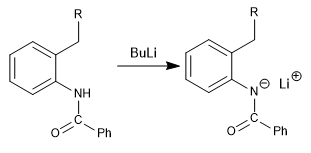
La síntesis de Madelung se basa en la formación de un carbanión bencílico, que ataca al sustituyente amida generando el ciclo pirrol.
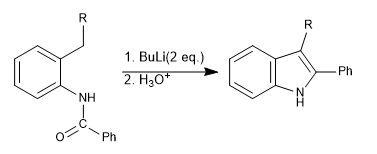
Mecanismo:
Etapa 1. Desprotonación de la amida