 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?
Cursos de Química Orgánica para los Grados en Química, Ingeniería Química, Biotecnología y Farmacia de las Universidades españolas.
Material específico para cada Universidad con teoría, ejercicios y exámenes resueltos en vídeo, creado por Germán Fernández. Soporte para dudas por WhatsApp. .
Más información en www.foroquimico.com
Si prefieres un curso de química orgánica tanto básica como avanzada te invito a acceder al canal: https://www.youtube.com/channel/UC_RiUaA2326jO9XozAA4q2g , en el que encontrarás más de 750 vídeos de teoría y ejercicios.
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA VISIBLE-ULTRAVIOLETA
- Visto: 120455
La espectroscopía estudia la interacción entre la radiación electromagnética y la materia. En esta interacción la radiación electomagnética puede comportarse como onda o como partícula, aunque no se ha observado ningún fenómeno físico en el que ambos comportamientos se den simultáneamente.
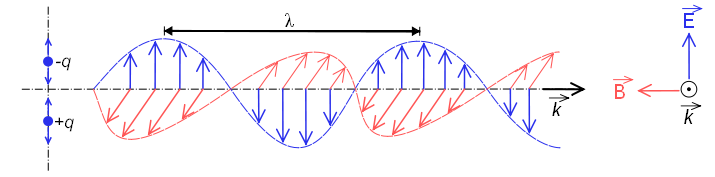
Cuando se comporta como onda, está constituida por un campo eléctrico y otro magnético que oscilan perpendiculares y se propagan a la velocidad de la luz $c=300000\;km/s$
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA VISIBLE-ULTRAVIOLETA
- Visto: 24213
Existen tres zonas del espectro electromagnético con especial interés en la determinación de compuestos químicos:
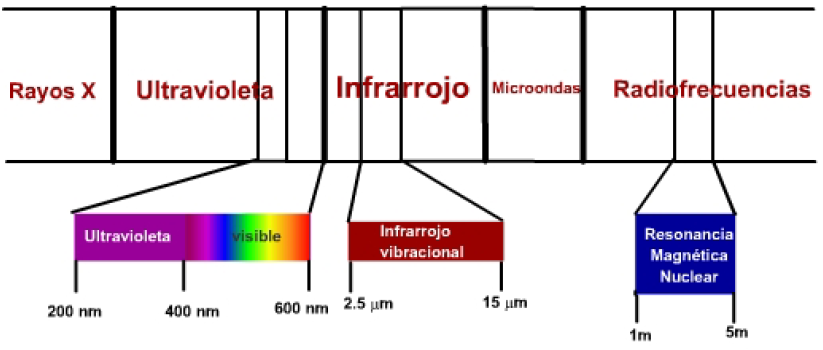
- La radiación visible-ultravioleta posee una energía adecuada para producir transiciones de electrones moleculares a niveles de energía superior. Es la denominada espectroscopía UV, cuya utilidad se limita principalmente a la determinación de moléculas con insaturaciones.
- La radiación infrarroja produce transiciones entre niveles vibracionales de una molécula. Los enlaces entre los átomos de una molécula no son rígidos, sino que vibran en torno a una posición de equilibrio y la radiación infrarroja es capaz de llevar estos enlaces a niveles de energía vibracional superiores. Es la denominada espectroscopía infrarroja (IR).
- Las ondas de radio poseen la energía adecuada para para hacer que los núcleos atómicos, sometidos a un campo magnético, entren en resonancia. Esta técnica se denomina espectroscopía de resonancia magnética nuclear (RMN).
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA VISIBLE-ULTRAVIOLETA
- Visto: 54503
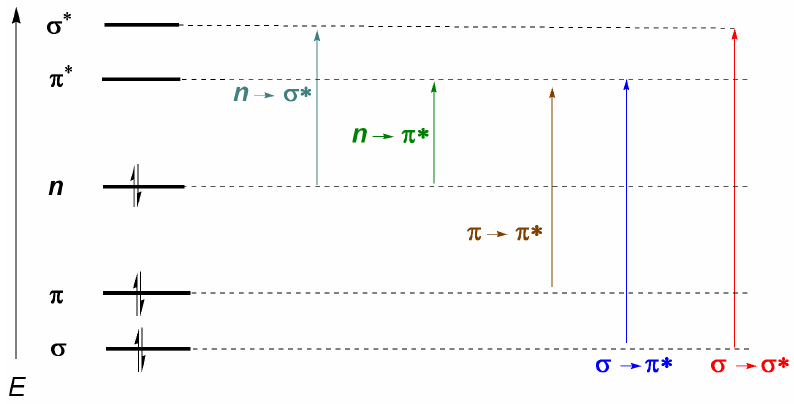
Las moléculas orgánicas distribuyen sus electrones en diferentes niveles electrónicos llamados orbitales moleculares. Los orbitales moleculares de menor energía son los $\sigma$, a continuación siguen los orbitales $\pi$. Cuando en la molécula existen átomos con pares electrónicos libres (oxígeno, azufre, nitrógeno, halógenos) tendremos niveles no enlazantes n. Estos niveles electrónicos se disponen en la región enlazante del diagrama. En la región antienlazante nos encontramos con los orbitales moleculares $\pi^{\ast}$ y $\sigma^{\ast}$. Una molécula en su estado fundamental tiene ocupados los orbitales enlazantes y no enlazantes y desocupados los antienlazntes.
De lo comentado anteriormente se deduce que las transiciones electrónicas deben partir de los orbitales enlazantes y no enlazantes terminando en los antienlazantes. Así podemos tener los 5 tipos de transiciones electrónicas que se muestran en el siguiente diagrama.
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA VISIBLE-ULTRAVIOLETA
- Visto: 39675
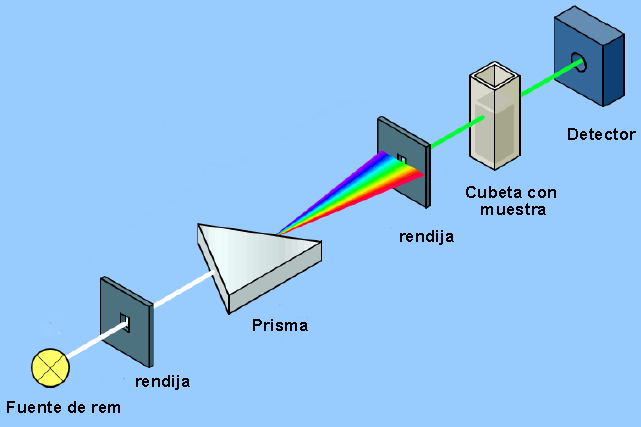
El instrumento que permite detectar la interacción entre la radiación electromagnética y la materia recibe el nombre de espectrofotómetro y su estructura básica puede observarse en el siguiente esquema.
- Detalles
- Germán Fernández
- ESPECTROSCOPÍA VISIBLE-ULTRAVIOLETA
- Visto: 59272
La Ley de Lambert-Beer introduce el concepto de absorbancia (A) de una muestra como $A=log\frac{I}{I_0}$. Donde $I_0$ representa la intensidad de la luz incidente e I la intensidad de la luz que atraviesa la celda. También podemos expresar la absorbancia en función de la longitud de la cubeta y de la concentración de soluto. \begin{equation} A=log\frac{I_0}{I}=\epsilon\cdot c\cdot l \end{equation} Donde $l$ es la longitud de la cubeta en cm, $c$ representa la concentración de soluto en mol/l y $\epsilon$ es la absortividad molar (coeficiente de extinción molar) medido en l/mol.cm.