DÉCONNEXIONS DE COMPOSÉS DE 1,3-DIOXYGÈNE
Les composés organiques oxygénés sont les plus abondants dans la nature et particulièrement les dioxygénés, c'est pourquoi de nombreux chercheurs en chimie ont modélisé la déconnexion rétrosynthétique de ces molécules, aspect qui sera étudié dans les paragraphes suivants.
Pour commencer, les modèles de déconnexion des molécules dioxygénées ont été divisés en deux grands groupes, basés sur la nature des synthons qui sont générés avec l'application d'une opération de synthèse de base appelée " DÉCONNEXION " à la molécule à synthétiser et que généralement elle est appelée molécule cible (MOb) .
Ces grands groupes sont :
![]() Modèles de déconnexion « logiques », et
Modèles de déconnexion « logiques », et
![]() Modèles de déconnexion « anormaux » ou « illogiques »
Modèles de déconnexion « anormaux » ou « illogiques »
Les modèles de déconnexion dits « logiques » sont ceux qui, en appliquant une « déconnexion » d'une ou plusieurs liaisons chimiques dans
Les composés pouvant être classés en 1,3-dioxygène et 1,5-dioxygène, lorsqu'ils sont soumis à une rétrosynthèse, forment généralement des synthons considérés comme "logiques". En revanche, les molécules organiques apparentées aux 1,2-dioxygénés, 1,4-dioxygénés et 1,6-dioxygénés, génèrent des synthons
considéré comme "illogique"
Modèle de coupure 1,3-dioxygène
![]() Composés β-dicarbonyle
Composés β-dicarbonyle
Les composés 1,3-dicarbonyles sont obtenus avec de bons rendements par des réactions de condensation de type Claisen, qui impliquent la réaction entre des esters et des composés à hydrogènes actifs, tels que : esters, cétones, aldéhydes, nitriles, dérivés nitrés et certains hydrocarbures en présence de réactifs alcalins.
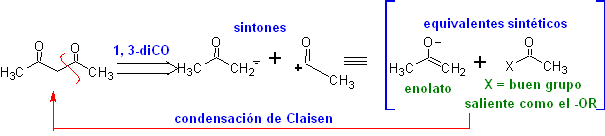
Les β-dicétones et β-cétoaldéhydes sont obtenus par la condensation croisée de Claisen, en utilisant une cétone et un ester appropriés. Dans la condensation croisée de Claisen des cétones et des esters, on obtient de bons rendements car les cétones sont notablement plus acides que les esters, donc, en milieu basique, la cétone est plus déprotonée que l'ester.
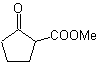
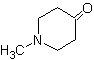
Exemples : Proposer un design de synthèse à partir de matériaux simples, pour les molécules suivantes :
Mob 16
| foule 17
| Mob 18
|
Solution:
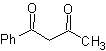
MOb 16 . Apparemment, les deux alternatives de déconnexion (a) et (b), montrées dans
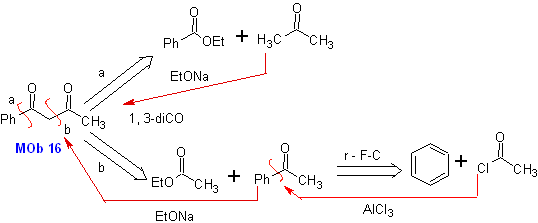
Cependant, l'alternative (b) s'avère la plus adaptée, car, dans le milieu réactionnel basique, le carbanion formé PhCOCH 2 - serait mieux stabilisé, du fait des effets de résonance et inductifs.
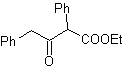
MOb 17. Déconnexion (a), dans
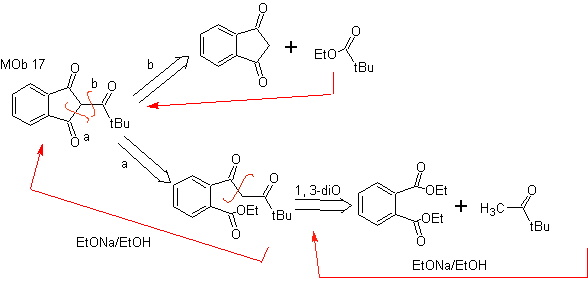
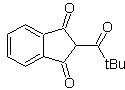
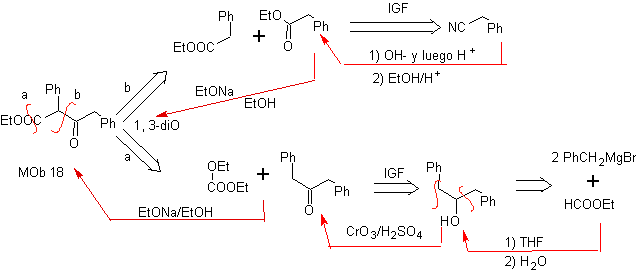
MOb 18. La meilleure alternative de déconnexion dans ce MOb est (b), car elle conduit à des équivalents synthétiques symétriques. l'alternative (a) n'est pas sans importance, dans l'utilisation du formiate d'éthyle.
![]() Composés β-dicarbonyles par condensations intramoléculaires
Composés β-dicarbonyles par condensations intramoléculaires
Proposer un plan de synthèse réalisable pour les molécules suivantes : | foule 19
| Mob 20
|
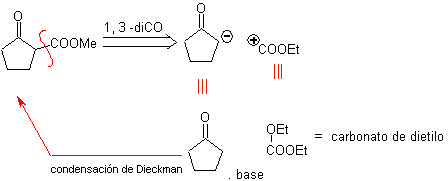
MOb 19. La déconnexion 1,3–diCO, conduit à un diester en relation 1,6. Ils sont faciles à reconnecter à un hexacycle d'alcène, modèle qui sera étudié un peu plus loin. Pour cette raison, une conception de synthèse alternative est proposée, basée sur des réactions connues.
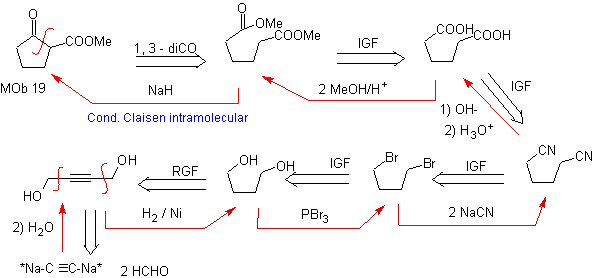
Conception qui ne peut être remise en cause que par le grand nombre d'étapes, ce qui diminue généralement le rendement de la synthèse.
Il est possible de penser à une autre déconnexion 1, 3 – diCO pour
Mob 20 . Parfois, il est nécessaire d'exercer un contrôle sur la structure de
Donc,
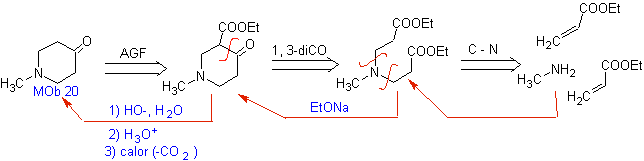
![]() Composés bêta -hydroxy
Composés bêta -hydroxy
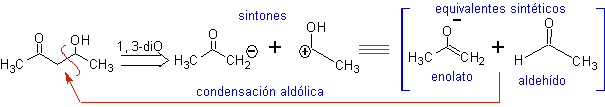
MOb21 . La meilleure déconnexion dans les composés bêta-hydroxy est par la liaison formée entre C et
et C b , par rapport au groupe carbonyle. Ces types de composés sont des produits typiques des réactions de condensation d'aldol et similaires, c'est pourquoi une bonne conception de synthèse pour
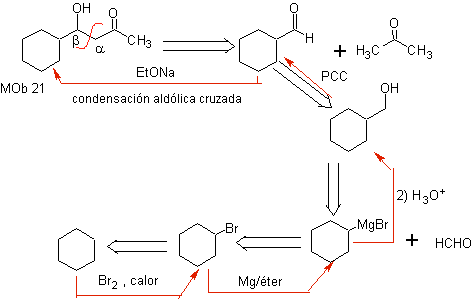
La base à utiliser pour former les b -hydroxycarbonyles doit être faible, pour éviter la déshydratation de la fonction alcool et produire ainsi un composé carbonyle a , b insaturé, qui fera l'objet de notre étude dans le paragraphe suivant.
La réaction entre le formal-cyclohexanone et l'acétone en milieu basique est une réaction de condensation de type aldol. Le groupe aldéhyde est le plus réactif et il n'y a pas de risque d'auto-condensation de l'aldéhyde par effets stériques.
![]() a , b composés carbonylés insaturés ( a , b insat.CO )
a , b composés carbonylés insaturés ( a , b insat.CO )
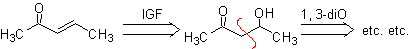
Les composés carbonylés α,β-insaturés sont faciles à préparer par déshydratation des composés β-hydroxycarbonylés, c'est pourquoi leur déconnexion implique de fonctionnaliser la molécule insaturée en un alcool. La liaison oléfinique pourrait également être préparée en utilisant la réaction de Wittig.
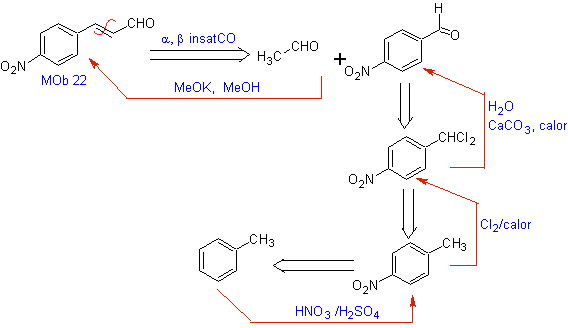
MOb 22. Puisqu'un composé carbonyle insaturé a,b , MOb 22 , peut être fonctionnalisé en l'alcool correspondant, pour obtenir un modèle 1,3-dioxygéné, il est possible de déconnecter la molécule directement par la double liaison, en formulant un C= un groupe O sur le carbone b et un groupe -CH 3 sur le carbone a .
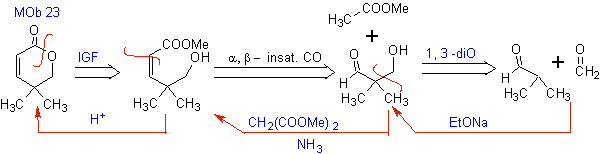
MOb 23. La déconnexion de cette molécule commence par l'ester cyclique (lactone), car c'est le point le plus critique, ce qui permet ensuite de la déconnecter en tant que composé carbonylé a , b insaturé .
MOb 24. La déconnexion classique par la double liaison de