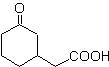
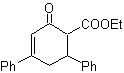
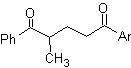
Los compuestos 1,5-dioxigenados generalmente son resultado de
reacciones de adición conjugada de nucleófilos provenientes de compuestos
carbonílicos, con Hα acídicos (enoles,
enolatos, enaminas, etc.), al igual que nitrilos y nitratos, sobre sustratos
alfa beta insaturado respecto a grupos carbonílicos y similares, conocida como
reacción de Michael, siendo opciones complementarias, la reacción de Nef y la
reacción de anelación (anillación) de Robinson.
Modelo de desconexión 1, 5 dioxigenado
(1,5-diO)
El modelo de desconexión 1,5-diO, puede ser aplicado, luego
de la funcionalización necesaria, a compuestos como: 1,5-dihidroxilos,
1,5-hidroxialdehidos, 1,5-hidroxicetonas, 1,5-hidroxiésteres,
1,5-cetoaldehidos, 1,5-dicetonas, 1,5-cetoésteres, 1,5-dialdehidos, etc.
Las posibilidades se incrementan, si además se toma en cuenta
a los nitroderivados y nitrilos, que pueden formar en medio básico, carbaniones
muy reactivos capaces de adicionarse a compuestos a,b-insaturado carbonílicos,
para obtener productos del tipo 1,5-diO.
El análisis fundamental de la desconexión
de los compuestos 1,5-diO es el siguiente:
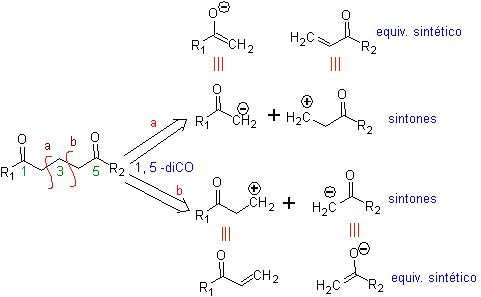
La elección de la desconexión (a) o (b), en torno al C3,
dependerá de la naturaleza de los grupos R1 y R2, que puedan conferir una mayor
o menor estabilidad al sintón o equivalente sintético necesarios para la
formación de
Proponer un diseño de síntesis para las MOb 29, 30 y
|
MOb 29
|
|
MOb 30
|
|
MOb 31
|
Solucion:
MOb 29. Análisis retrosintético:
El carbanión necesario para adicionarse al compuesto a,b-
insaturado CO puede obtenerse a partir
del malonato de dietilo en medio básico. Que posteriormente obligará a una
descarboxilación, para llegar a
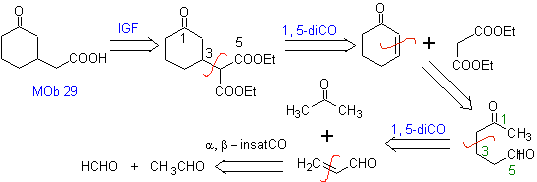
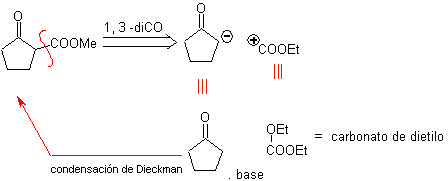
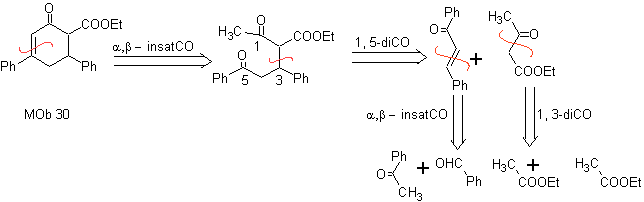
Síntesis. Se procede con una
combinación de Condensaciones de Claisen,
Claisen Schmidt , la reacción de Michael y la anelación de Robinson, para
llegar a
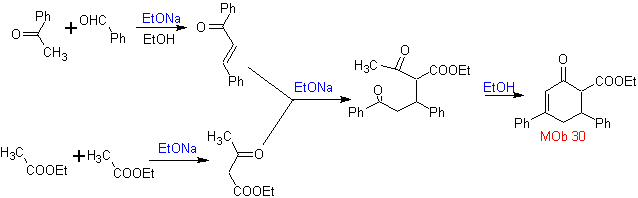
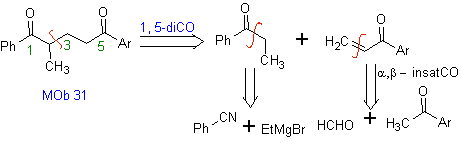
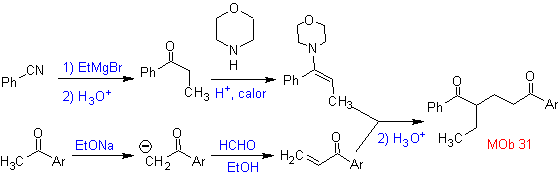
Las cetonas vinílicas son muy reactivas y tienden a
dimerizarse por la reacción de Diels-Alder, razón por la cual, si éstas son
necesarias como sustrato en la reacción de adición de Michael, es necesario
prepararlas “in situ” y una reacción muy útil para ello es la reacción de
Mannich, como puede verse en el siguiente ejemplo.
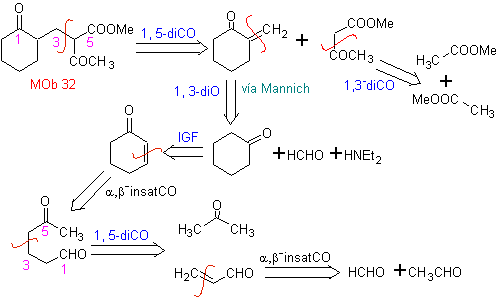
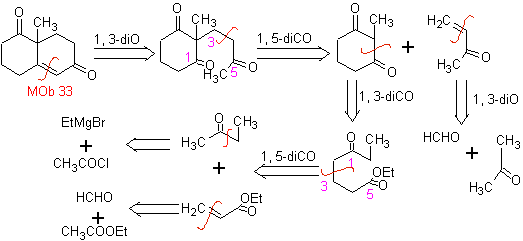
MOb 32. Análisis Retrosintético. La aplicación
inicial del modelo de desconexión 1,5-diCO, genera un precursor como la cetona
vinílica, que deberá formarse por la reacción de Mannich, seguida de la
eliminación de Hoffmann, para combinarse con el cetoéster formado por la
condensación de Claisen
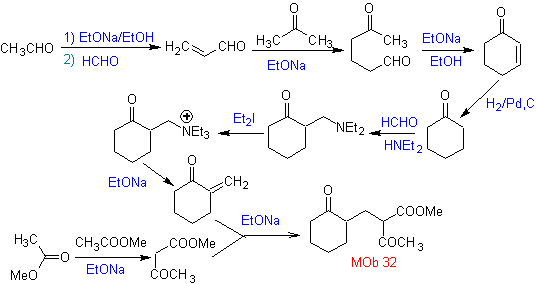
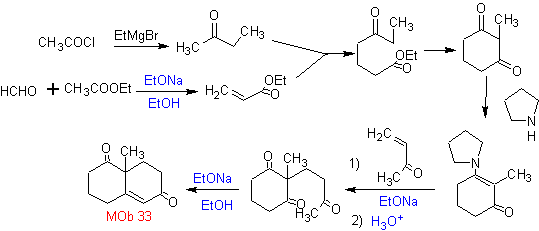
Síntesis. La cetona vinílica necesaria para la
reacción (de Michael) con el cetoéster, se prepara, combinando adecuadamente la
reacción de Mannich y la eliminación de Hoffmann.
Síntesis. Será necesario ejercer control, para
generar el nucleófilo con el C 2º, lo que se consigue por la formación de la
enamina, con un grupo amínico, suficientemente voluminoso. El producto se forma
como se indicó por la anelación ó anillación de Robinson.
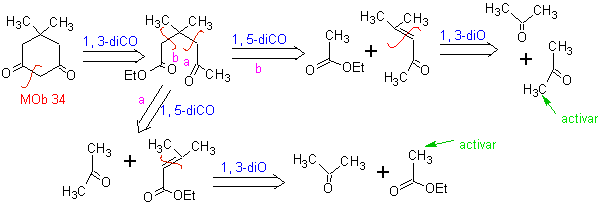
La anelación de Robinsón, también permite obtener compuestos
cíclicos 1, 3-dicetonas.
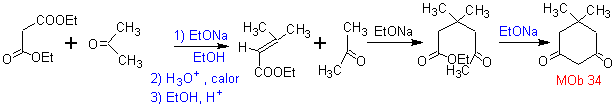
MOb 34. Análisis
Retrosintético. La desconexión 1,3-diCO de
 ¿Te cuesta entender la Química Orgánica?
¿Te cuesta entender la Química Orgánica?