В этом разделе мы собираемся изучить влияние кольцевых напряжений на свойства гетероциклов.
А) Угловое напряжение в малых гетероциклах (3 и 4 члена).
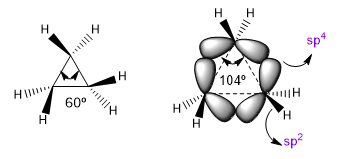
Естественные валентные углы sp 3 углерода составляют 109,5°, однако в трехчленных циклах этот угол уменьшается до 60°, что создает огромное напряжение. Чтобы уменьшить это напряжение, связи между атомами углерода больше не являются прямыми, а изгибаются, что приводит к возникновению изогнутых связей, называемых «банановыми связями». Углы, образованные этими связями, составляют 104°, что является более приемлемым отклонением.
| Гибридизация | валентный угол |
| сп сп 2 сп 3 сп 4 | 180º 120º 109,5º 104 место |
Эта ситуация приводит к тому, что связи CC имеют тенденцию к теоретической гибридизации sp 4 , тогда как связи CH имеют sp 2 . Эти гибридизации позволят нам объяснить различия в спектроскопических и основных свойствах. В инфракрасных спектрах наблюдается, что по мере уменьшения р-характера связи поглощение смещается в сторону большего числа волн. Давайте сравним нециклические амиды со стрессовыми лактамами, чтобы увидеть этот эффект.
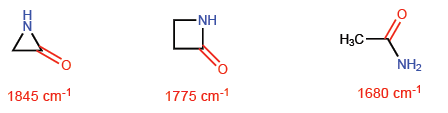
В азетидин-2-оне р-характер связи С=О меньше, чем в других молекулах, и поэтому поглощение инфракрасного излучения смещается в сторону большего числа волн.
Еще одним свойством, на которое влияет штамм этих гетероциклов, является основность. Увеличение р-характера неподеленной пары приводит к уменьшению основности. Таким образом, между циклическим и ациклическим амином циклический является менее основным.
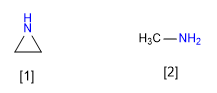
[1] Азиридин
[2] Метиламин
Азиридин менее основный, чем метиламин. Гибридизация неподеленной пары азиридина приближается к sp2, а гибридизация метиламина - к sp3 . Меньший p-характер азиридина делает его менее основным.
B) Кольцевое напряжение в больших кольцах. Известно, что циклооктин является самым маленьким из существующих циклических алкинов. Наименьшие циклоалкины вызывают искажение валентного угла, соответствующее sp-гибридизации, создавая напряжение в молекуле, которое делает ее невозможной.
Однако есть исключение из этого правила, наблюдаемое в тиациклогептинах, что объясняется большей длиной связи CS по сравнению с СС.
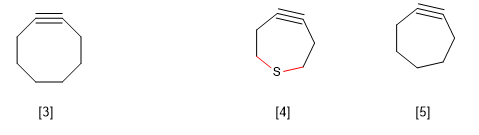
[3] Циклооктин
[4] Большая длина связей CS по сравнению с CC позволяет существование этого циклического алкина.
[5] Не существует
C) Жесткость велосипедов.
Жесткость бицилл, невозможность поворота, предотвращает некоторые резонансы, порождающие аномальные свойства в молекуле. Амиды делокализуют неподеленные пары от азота до карбонильного кислорода, что устраняет основность азота. Однако, когда амид является частью бициклической системы, такое отнесение нецелесообразно, и азот оказывается сильно щелочным.
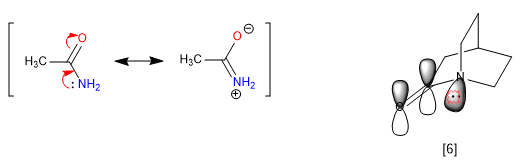
[6] Пара азота не может быть перенесена, потому что ее орбиталь не параллельна орбитали карбонила.
Азот 1-азабицикло[2.2.2]октана обладает замечательной основностью, сравнимой с ароматическими аминами, с pKa для сопряженной с ним кислоты 5,3. Спектроскопические данные для этого амида также уникальны. Таким образом, карбонил поглощает при 1762 см -1 , что более характерно для кетона в стрессовом состоянии, чем для амида. Объяснение опять кроется в невозможности переноса свободной пары азота.
D) Конформационное равновесие в sis-членных кольцах .
Меньшая длина связи СО по сравнению с СС вносит определенные особенности в конформационные равновесия шестичленных гетероциклов с кислородом.
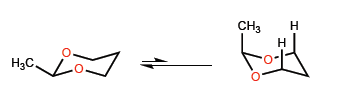
Короткие расстояния CO заставляют метил смещаться ближе к атомам водорода в положении 3, что приводит к 1,3-диаксиальным взаимодействиям, которые сдвигают конформационное равновесие полностью влево.
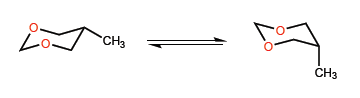
Во втором примере ситуация меняется, так как взаимодействие между неподеленными парами метила и кислорода не очень важно, а трет-бутильная группа может располагаться даже в аксиальном положении.