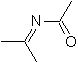
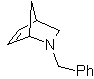
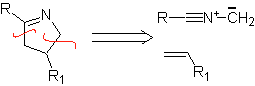
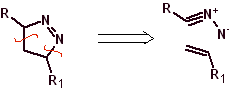
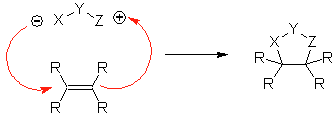
Essas reações normalmente formam anéis heterocíclicos de cinco membros, para os quais é necessária a reação entre um composto dipolar n1,3 e um alceno. A reação é uma [3-2] cicloadição. Os compostos 1,3-dipolares que tiveram mais uso para formar heterociclos pentagonais são:
 |  |
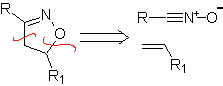 | 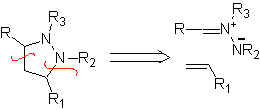 |
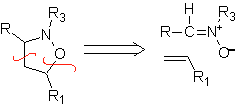 | 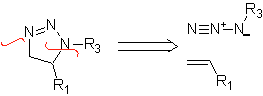 |
| Mb: 86
| . | Mb: 87 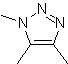 | .. | Mb: 88 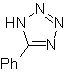 |
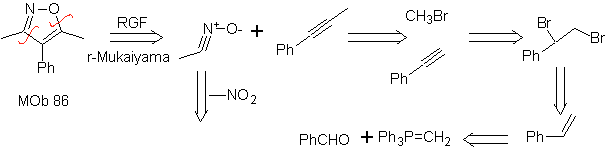
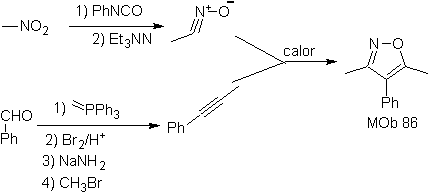
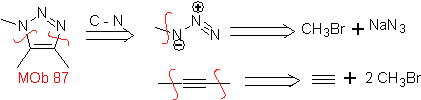
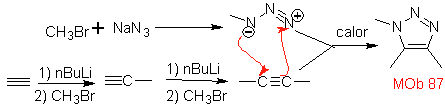
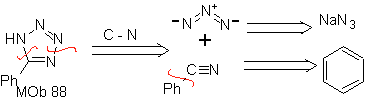
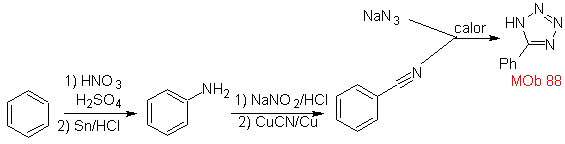
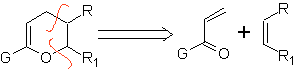
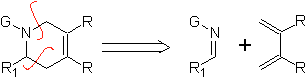
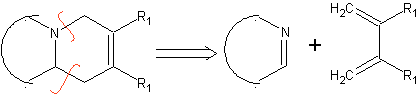
São bons heterodienos, aldeídos e cetonas conjugadas, 1-azadienos e 2-azadienos. Aldeídos e cetonas conjugados produzem anéis pirânicos, a reação é facilitada por ácidos de Lewis ou aumento da pressão, bem como pela presença de um grupo de elétrons. atraente para o alceno.
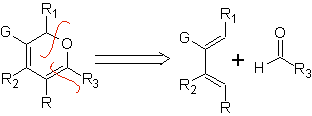
Heterodienófilos mais comuns na reação de Diels-Alder:
| | ||||||
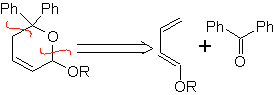
Aldeídos, cetonas e aldeídos, se forem deficientes em elétrons, reagem em condições brandas, caso contrário, requerem condições de alta pressão e temperatura ou catalisadores do tipo ácido de Lewis. Esses heterodienófilos permitem a formação de sistemas pirânicos, úteis na preparação de precursores acíclicos de diversas drogas, como é o caso dos antibióticos macrocíclicos.
 | … |  |
 |  |
 |  | |
| ||
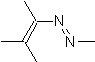 | 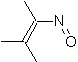 | |
|
MOb 89 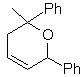 | … | Mb: 90 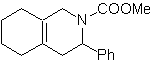 | . | Mb: 91 |
| Mb: 92
| Mb: 93
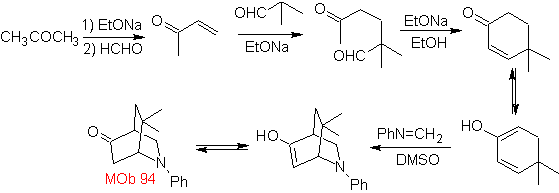
| MOb 94 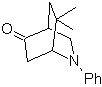 |
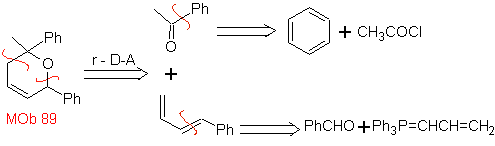
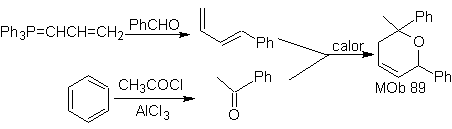
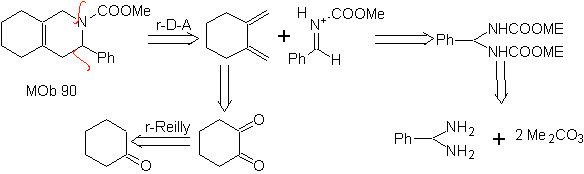
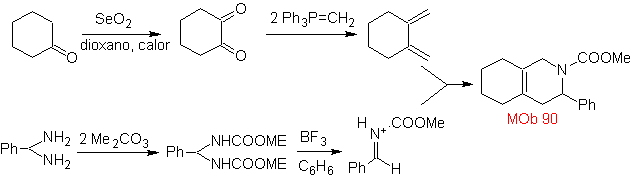
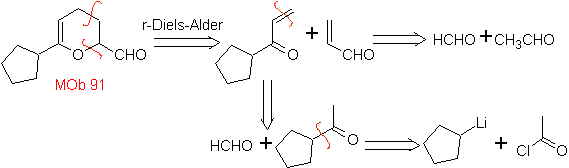
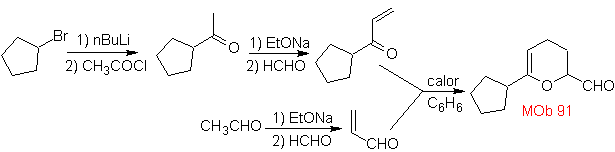
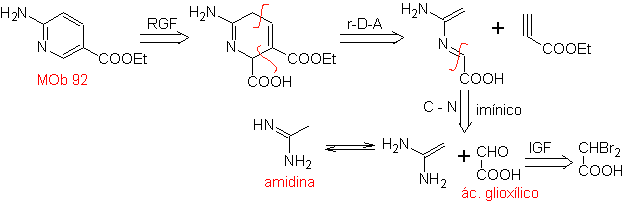
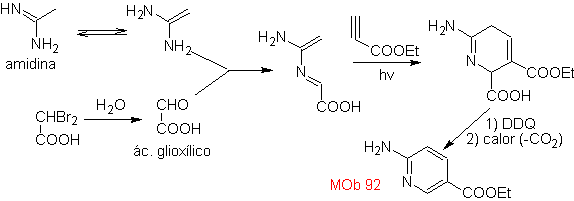
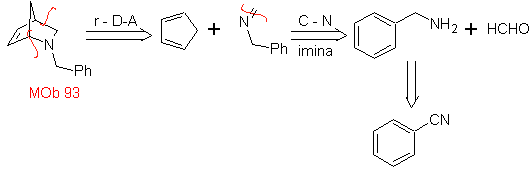
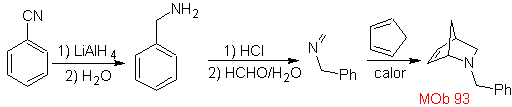
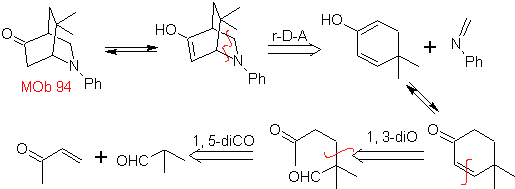
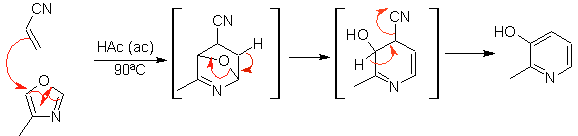
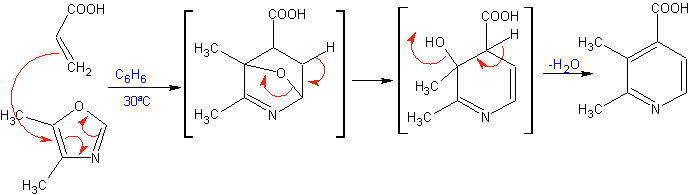
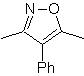
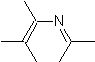
As cicloadições mais estudadas são aquelas que ocorrem entre compostos heterocíclicos pentagonais como os oxazóis e alguns dienófilos, que podem ser combinados com eles por adição eletrocíclica e posterior eliminação de uma pequena molécula, para produzir anéis de piridina. Exemplos: