DESCONEXÃO DE COMPOSTOS DE 1,4-DIOXIGÊNIO
Outro grupo de compostos de grande importância na síntese química é formado por moléculas dioxigenadas que se encontram em uma razão de distância de 1,4. Esses compostos, quando submetidos a uma análise de desconexão retrossintética, geram síntons, onde um deles, o eletrófilo ou nucleófilo, pode ser considerado "anômalo" ou "ilógico", pois a carga atribuída a um dos átomos não pode ser explicada em termos de sua eletronegatividade intrínseca ou induzida.
1. Compostos de 1,4-dioxigênio (1,4-diO)
Neste tipo de compostos, a desconexão conduz também a um sínton lógico e a outro sínton ilógico (não natural), que pode ser um nucleófilo ou um eletrófilo, cujo equivalente sintético ainda tem de ser adequadamente retrabalhado, para poder ser utilizado em a reação química.
1. 1. Compostos 1,4-dicarbonil
1.1.1. compostos de 1,4-dicetona
As alternativas de desconexão deste tipo de compostos ou moléculas a sintetizar (MOb) podem conduzir às seguintes opções:
para. Um sínton de ânion lógico e um sínton de cátion ilógico
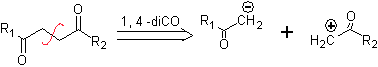
O equivalente sintético do ânion é o íon enolato ou o próprio enol do composto carbonílico. Em vez disso, o equivalente sintético para o carbocátion é o alfa-halocarbonil. (Umpoloung)
b. Um sínton de cátion lógico e um sínton de ânion ilógico
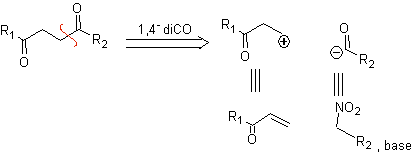
O equivalente sintético do sínton catiônico lógico é o composto carbonílico α,β-insaturado. Um equivalente sintético adequado para o ânion sínton pode ser um ânion nitroalcano. O grupo –NO 2 em alcanos pode ser transformado em C=O, por meio da reação de Nef, ou pelas variantes da reação de McMurry, onde por ação do TiCl 3, o nitroalcano é transformado em uma imina, que é então é hidrolisado em meio ácido ao respectivo composto carbonílico.
1.1.2.
compostos 1,4-cetoéster
γ-cetoésteres, 1,4-diésteres e 1,4-diácidos podem ser desconectados a um sínton catiônico natural, cujo equivalente sintético é um composto carbonílico α,β-insaturado, e ao não natural (“ilógico” ) ânion sínton (-) COOR, cujo equivalente sintético é o íon cianeto.
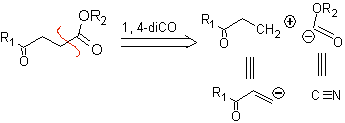
Exemplos: Proponha um projeto de síntese, a partir de materiais simples e acessíveis, para cada uma das seguintes moléculas:
MOb 35
| MOb 36
| |
MOb 37
| MOb 38
|
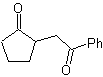
MOb 35 (a). Análise retrossintética . A molécula pode ser desconectada de acordo com o modelo 1,4-diCO. A ciclopentanona precursora gerada deve ser previamente ativada para que seu Cα seja mais nucleofílico, e então ser usado na reação com α.bromoacetona.
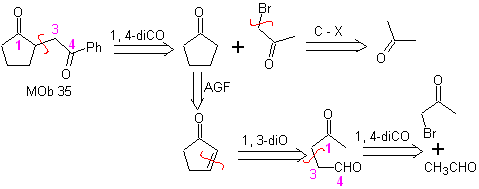 síntese . A nucleofilicidade da ciclopentanona é controlada e garantida, usando LDA, para chegar a
síntese . A nucleofilicidade da ciclopentanona é controlada e garantida, usando LDA, para chegar a
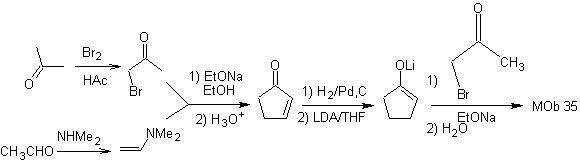
MOb 35 (b). Análise retrossintética . O modelo 1,4-diCO que apresenta
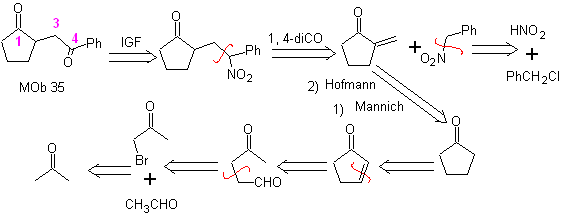
síntese . Da mesma forma, a última etapa, para alcançar
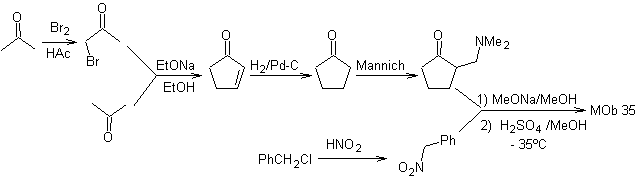
A utilização de nitroalcanos ou nitroarenos secundários gera cetonas como produto, pela reação Nef, razão pela qual esta metodologia só é aplicável a compostos 1,4-cetoésteres, 1,4-cetonas e 1,4-cetoaldeídos.
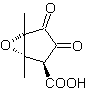
MOb 36. Análise retrossintética. Em primeiro lugar, o grupo carboxílico de
Deve ser entendido que a ligação dupla no anel é mais reativa à epoxidação do que a outra ligação dupla. A posterior desconexão α,β-insat CO, permite formar uma estrutura que é mais fácil de desconectar pelos modelos dioxigenatos gerados nas moléculas intermediárias.
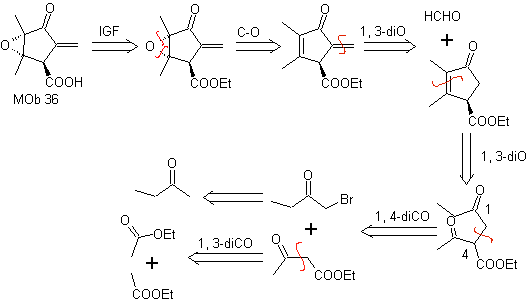
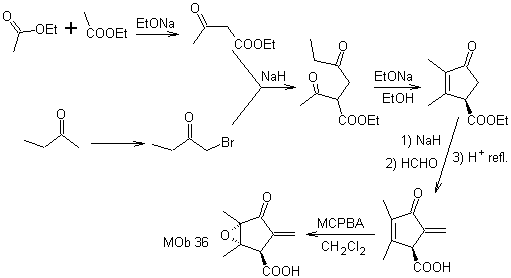
Síntese. O único cuidado que se deve ter nessa síntese é a epoxidação da dupla ligação do anel, mais reativa que a dupla ligação vinílica, então as reações para chegar à síntese de
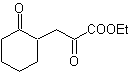
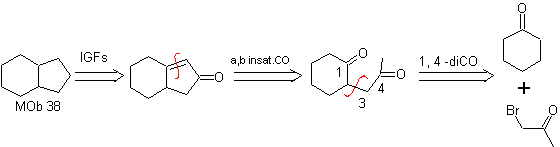
MOb 37. Análise retrossintética: A desconexão de
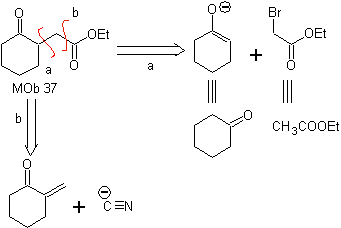
Síntese : Desconexão (a) segue. hidrólise
no final, deve ser controlado, para
não afeta o grupo éster de MOb 37
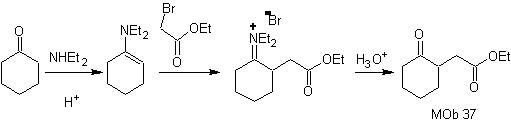
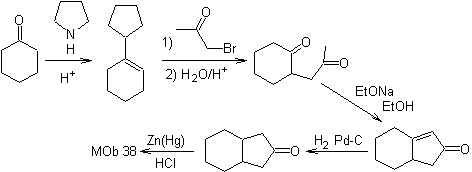
síntese .
A enamina da ciclohexanona é usada novamente para deslocar o halogênio da cetona. O composto 1,4-diCO formado é ciclizado em meio básico.
2.1.2.
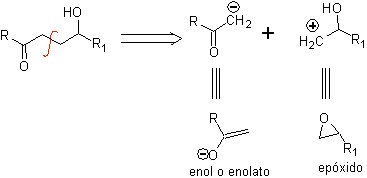
g -Compostos hidroxicarbonílicos
Um composto γ-hidroxicarbonila corresponde ao modelo 1,4-diO, razão pela qual sua desconexão fornece um sínton aniônico lógico e um sínton catiônico ilógico, cujo equivalente sintético pode ser um epóxido.
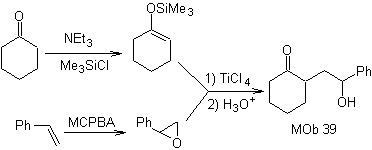
Como a seguinte molécula poderia ser sintetizada? | MOb 39
|
MOb 39. Análise retrossintética.
A desconexão do modelo
γ-hidroxicarbonil, MOb 39, dá origem a ciclohexanona como molécula precursora e um epóxido aromático. Você tem que procurar o enol ou enolato da cetona, que ativa seu Cα, para abrir o epóxido no lado menos impedido.
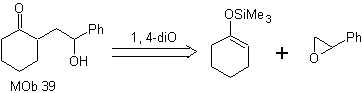
Síntese. O éter de silileno é um poderoso nucleófilo, capaz de atacar um epóxido pelo lado menos protegido, em meio ácido e catalisado por sal de Ti(IV).