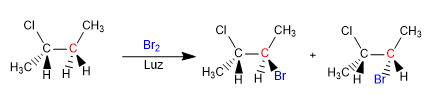
Veremos como as reações químicas podem introduzir quiralidade nas moléculas, obtendo produtos na forma de misturas racêmicas ou misturas de diastereoisômeros.
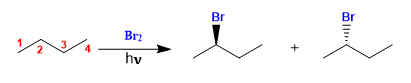
O butano halogena na presença de bromo e luz, no carbono 2, para formar uma mistura de enantiômeros. O radical formado apresenta faces enantiotópicas, que são halogenadas com igual probabilidade, dando origem a uma mistura racêmica (enantiômeros em igual proporção).
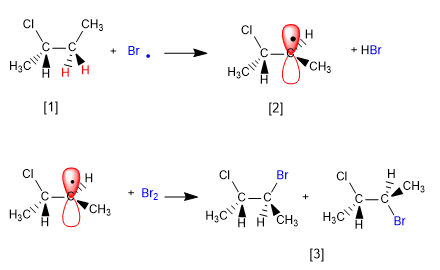
O mecanismo desta reação consiste em três etapas: iniciação, propagação e terminação. A propagação é a etapa que determina a estereoquímica do produto final.
halogenação de butano
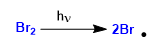
Estágio 1. Iniciação
Estágio 2. Propagação
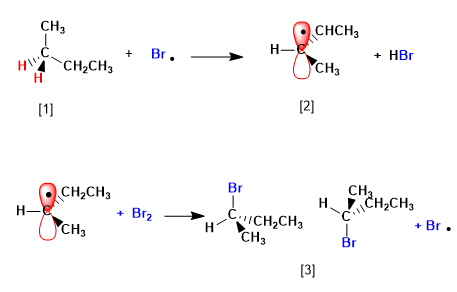
[1] H (hidrogênios enantiotópicos)
[2] Radical com faces enantiotópicas
[3] Par de enantiômeros
O produto é obtido como uma mistura racêmica, devido à formação de um radical planar halogenado em ambas as faces. Os hidrogênios enantiotópicos são quimicamente equivalentes e são subtraídos pelo bromo na mesma taxa.