Les charges positives, négatives ou radicalaires en positions proches des doubles liaisons sont délocalisées par résonance, étant particulièrement stables.
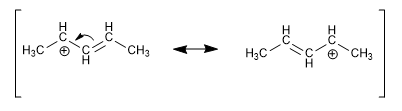
carbocation allylique
Le carbocation formé dans les positions voisines des doubles liaisons est appelé carbocation allylique. Il est stabilisé en délocalisant la charge entre deux carbones, et est donc plus stable qu'un carbocation secondaire normal.
Les diènes conjugués sont des molécules possédant plusieurs doubles liaisons alternant avec des liaisons simples. Ce type de structure permet le mouvement des électrons p dans toute la molécule, permettant leur délocalisation et augmentant la stabilité du composé.
Diénos conjugués :
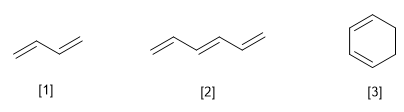
[1] Buta-1,3-diène
[2] Hexa-1,3,5-triène
[3] Cyclohexa-1,3-diène
Diénos non conjugué :
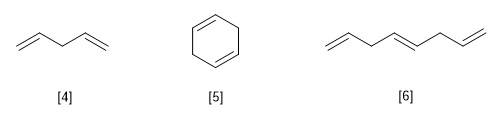
[4] Penta-1,4-diène
[5] Cyclohexa-1,4-diène
[6] Octa-1,4,7-triène
Équilibre conformationnel dans les diènes
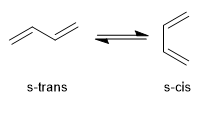
Le 1,3-butadiène peut adopter deux conformations possibles appelées s-cis et s-trans qui s'interconvertissent par rotation. Cet équilibre est important dans la réaction de Diels-Alder puisque seule la conformation s-cis est réactive.

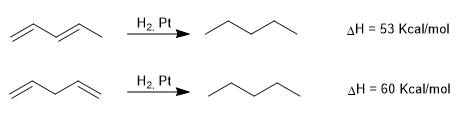
Chaleurs d'hydrogénation dans les diènes conjugués et non conjugués

Comme on peut le voir, le diène conjugué dégage moins de chaleur lorsqu'il est hydrogéné, car il contient moins d'énergie, c'est-à-dire qu'il a une plus grande stabilité.