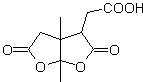
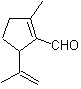
DÉCONNEXION DES COMPOSÉS DE 1,6-DIOXYGÈNE
Les composés 1,6-difonctionnalisés utilisent de préférence la stratégie de reconnexion pour leur synthèse respective ; Cette stratégie peut très bien être combinée avec la réaction de Diels-Alder, qui produit généralement des adduits oléfiniques à six chaînons, ou la réduction de Birch de cycles benzéniques, qui génère également des produits oléfiniques à six chaînons.
1. Composés 1,6-dioxygénés
La réaction qui génère des composés dicarbonylés, de différentes combinaisons possibles : dicétones, cétoacides, cétoaldéhydes, diacides, etc. et à différentes distances les uns des autres, est sans doute la réaction de ozonolyse des composés oléfiniques.
En fonction de la structure du substrat et des conditions de réaction sur l'intermédiaire ozonide formé, une énorme diversité de composés sera obtenue à la suite du clivage de la double liaison oléfinique. Parmi ceux-ci, ceux qui sont dans un rapport 1, 6 - dioxygéné présentent un intérêt particulier, comme on peut le déduire de l'opération de « reconnexion » synthétique suivante :
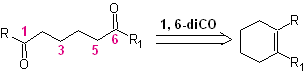
La meilleure façon de comprendre le fonctionnement de cette « opération de reconnexion synthétique » est sera réalisé grâce à la solution de la synthèse des molécules organiques suivantes :
|
Mob 50
|
|
Mob 51
|
|
Mob 52
|
|
|
|
|
|
|
|
Mob 53
|
|
Mob 54
|
|
Mob 55
|
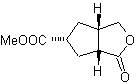
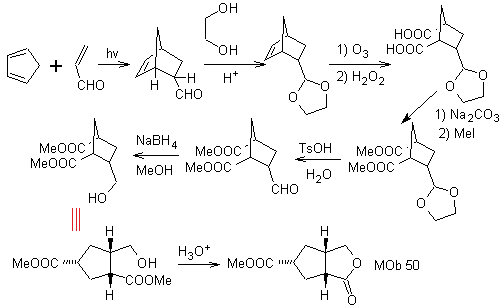
MOb 50 . Analyse rétrosynthétique : Elle est en premier lieu déconnectée par la fonction lactone de la molécule. Sur la molécule précurseur générée, à son tour, on peut affirmer que sa formation peut avoir eu lieu à partir de l'acide diacarboxylique en position 1-6. Qui se reconnectent pour donner naissance à l'alcène qui les a produits par réaction d'ozonolyse oxydative. L'alcène formé est un adduit typique de Diels-Alder entre le cyclopentadiène et le crotonaldéhyde.
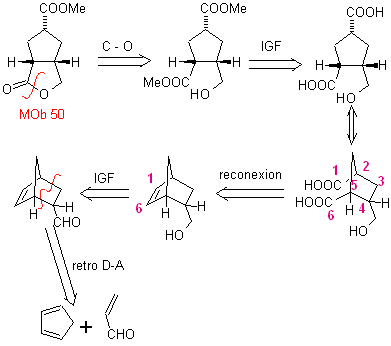
Synthèse : La réaction de Diels-Alder entre cyclopentadiène et l'aldéhyde α,β-insaturé fournit l'adduit alcène, pour son ouverture correspondante par ozonolyse oxydante, préalablement à une réaction de protection du groupement aldéhyde, qui est ensuite déprotégé, à réduire en fonction alcool. Cet alcool réagit avec le groupement ester en milieu acide pour former la lactone souhaitée, MOb 50
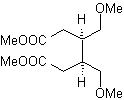
MOb 51
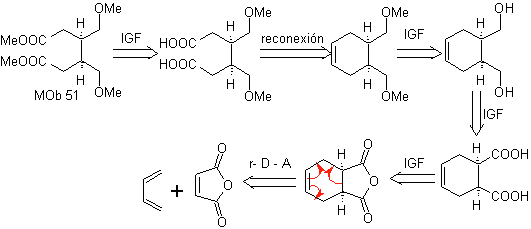
, Analyse rétrosynthétique : Se projette la molécule précurseur de
51, vers un diacide, qui aurait pu être obtenu par ozonolyse oxydative à partir d'une molécule oléfinique à six chaînons. L'éther par IGFs successifs est fonctionnalisé en un composé carboxylique, résultat de l'hydrolyse acide d'une fonction anhydride. adduit typique de la cyclisation de Diels-Alder.
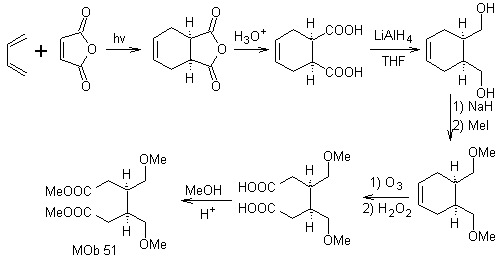
La synthèse. Avec la réaction de Diels-Alder, l'adduit d'anhydride cyclique est formé, qui après avoir été hydrolysé est réduit en alcool respectif, qui par Williamson est transformé en éthers. Le cyclohexène est ouvert par ozonolyse oxydante et les groupements acides réagissent en milieu acide avec l'alcool méthylique pour se transformer en
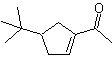
MOb 52 . Analyse rétrosynthétique : initialement déconnectée
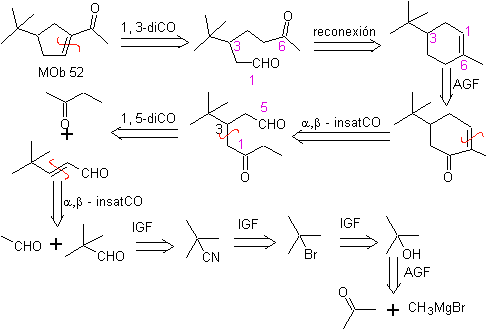
Synthèse : L'acétone permet la formation de l'intermédiaire t-Butylformaldéhyde, qui en milieu basique et éthanol se condense avec l'éthanal. Au produit, α,β-insat CO formé, on ajoute l'énolate de butanone, le même milieu basique permet la cyclisation intramoléculaire. Puis le C=O est transformé en –CH2, par réduction. Le cycloalcène produit est ouvert par ozonolyse dans Me 2 S. Et il est à nouveau cyclisé en milieu basique pour obtenir
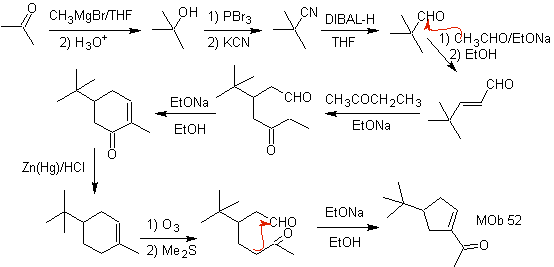
MOb 53 . Analyse rétrosynthétique : Elle commence par la déconnexion simultanée des lactones de
D'autre part, la butanone est préparée à partir d'un acétylène terminal et ce dernier à partir d'un halogénure d'éthyle et d'acétylène de sodium.
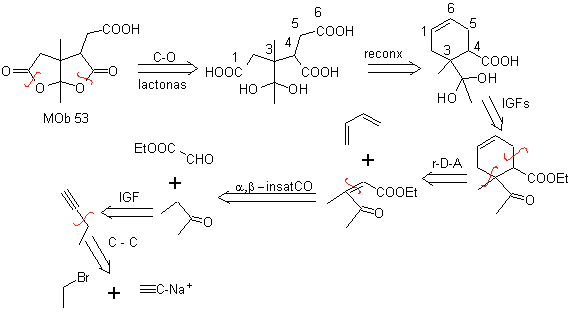
La synthèse. Après l'ouverture du cyclohexène, par ozonolyse oxydante, L'hydrolyse acide du groupe ester restant et la formation correspondante de l'hydrate de cétone sont suffisantes pour la formation des lactones et la fermeture respective du cycle, pour produire
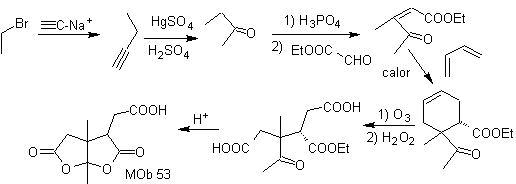
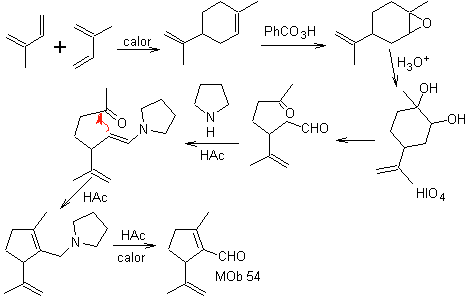
MOb 54 . Analyse rétrosynthétique : La déconnexion par la double liaison de
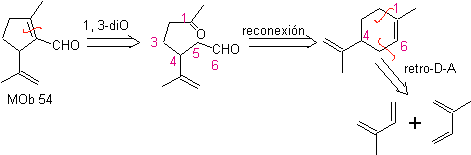
Synthèse : La réaction de Diels-Alder entre deux molécules de 2-méthyl butadiène forme un adduit qui forme avec HMCPBA un époxyde avec le centre le plus réactif.
· Lors de l'hydrolyse acide de l'époxyde, il se forme un diol qui est oxydé par l'acide. périodique, vers un composé 1,6-diCO Le groupement CHO est protégé par une énamine, tout en activant son C alpha, pour une condensation en milieu acide, le système est chauffé et on obtient
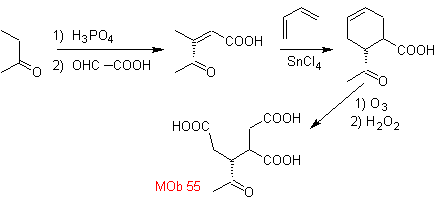
MOb 55. Analyse rétrosynthétique : La synthèse de
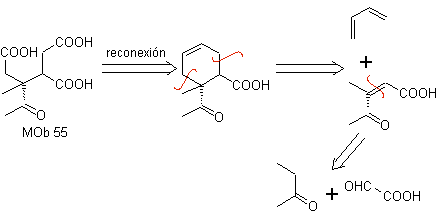
La synthèse. Les réactions indiquées ont déjà été étudiées dans la synthèse de